Clear Sky Science · pt
Transmissão de lactato de células tumorais hipóxicas promove senescência de macrófagos e polarização M2 via o eixo DNMT1-NHE7 para acelerar a progressão do câncer endometrial
Por que privar tumores de oxigênio importa
O câncer endometrial, que se origina no revestimento do útero, está se tornando mais comum em todo o mundo. Muitos tumores avançados são difíceis de tratar porque retornam, se espalham ou resistem às terapias padrão. Este estudo examina o que acontece dentro desses tumores quando ficam com pouco oxigênio — uma característica comum de cânceres de crescimento rápido — e mostra como um subproduto simples, o lactato, pode reprogramar células imunes vizinhas para ajudar o câncer a crescer em vez de combatê‑lo.
Baixo oxigênio transforma tumores em fábricas de lactato
À medida que as células do câncer endometrial se multiplicam, seu suprimento sanguíneo não dá conta, criando bolsões de baixo oxigênio, ou hipóxia. As células respondem ativando um regulador mestre chamado HIF1A que reconfigura sua produção de energia. Em vez de depender principalmente de processos eficientes, as células aumentam a glicólise, um mecanismo rápido porém ineficiente que produz grandes quantidades de lactato. Os pesquisadores analisaram dados tumorais de centenas de pacientes e observaram que níveis mais altos de HIF1A andavam de mãos dadas com maior atividade de muitos genes relacionados à glicólise e transportadores que bombeiam lactato para fora das células cancerosas. Pacientes cujos tumores apresentavam mais HIF1A tendiam a ter prognóstico pior, sugerindo que essa mudança metabólica está intimamente ligada a doenças mais agressivas.
Como o resíduo tumoral remodela células imunes úteis
Macrófagos são células imunes que podem atacar tumores ou apoiá‑los, dependendo do seu estado. Neste trabalho, a equipe mostrou que sob hipóxia, células do câncer endometrial liberam muito mais lactato para o ambiente. Esse lactato é exportado por um transportador chamado MCT3 nas células tumorais e então importado pelos macrófagos via outro transportador, MCT1. Uma vez no interior, o lactato desloca os macrófagos de um modo defensivo para o chamado estado M2, associado à reparação tecidual, supressão da inflamação e, infelizmente, ao apoio ao crescimento tumoral. Em experimentos de laboratório, macrófagos expostos a líquido tumoral rico em lactato exibiram mais marcadores do tipo M2, e o fluido que secretaram, por sua vez, aumentou o crescimento, a motilidade e a invasão das células cancerosas. 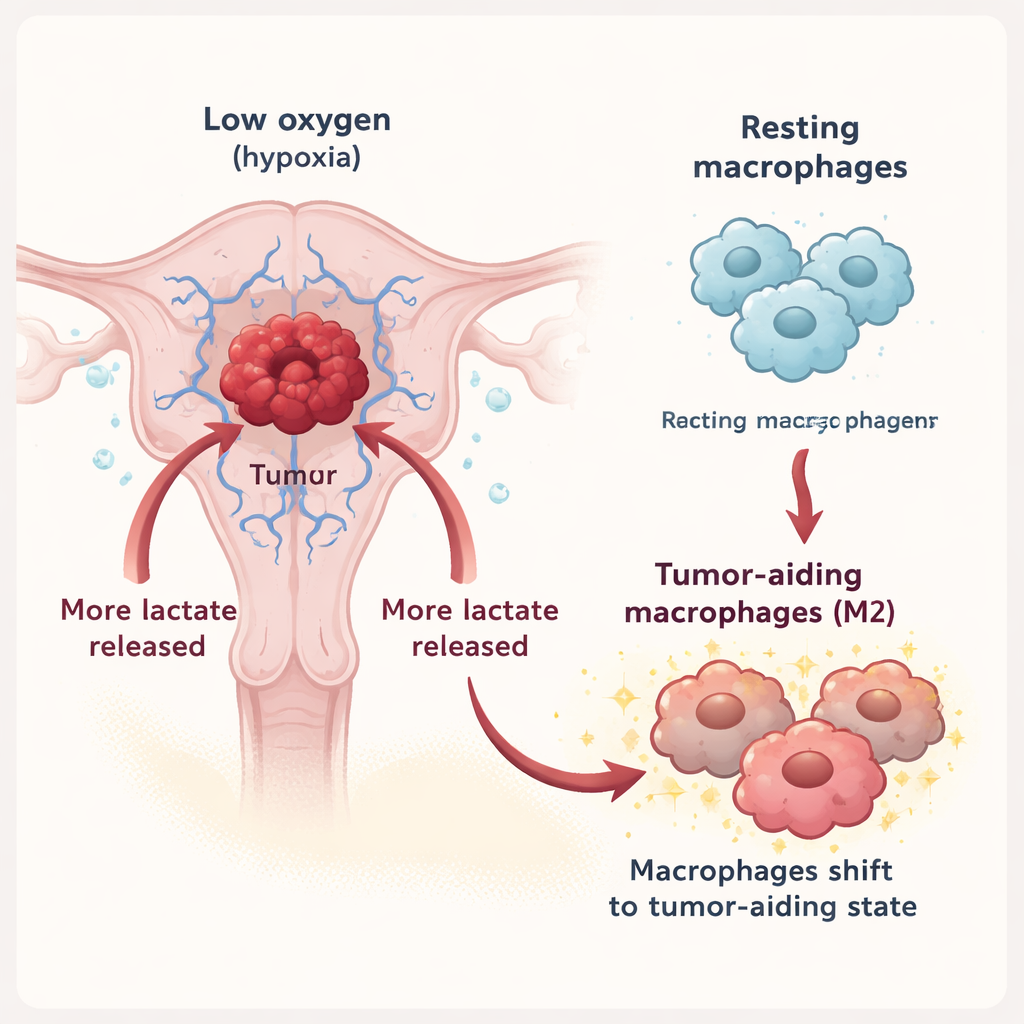
Um interruptor epigenético que silencia uma “válvula de pH” celular
O estudo avançou ao descobrir o interruptor molecular dentro dos macrófagos que conecta o lactato derivado do tumor a esse comportamento nocivo. O lactato não fica apenas flutuando; ele pode modificar proteínas histonas no núcleo — uma marca química conhecida como lactilação — que influencia quais genes são ativados ou silenciados. Os pesquisadores descobriram que o lactato aumenta uma marca específica de histona na região de controle do gene DNMT1, elevando sua atividade. DNMT1 é uma enzima que adiciona grupos metila ao DNA e pode silenciar genes. Um de seus alvos aqui é NHE7, uma proteína que ajuda a controlar a acidez dentro de certos compartimentos celulares. Quando DNMT1 é aumentado, ele eleva a metilação do gene NHE7, reduzindo sua expressão. A diminuição de NHE7 perturba o equilíbrio de pH interno e ativa uma via de sinalização conhecida como MAPK. Essa via, por sua vez, empurra os macrófagos para o estado M2 pró‑tumoral e para uma forma de envelhecimento chamada senescência, que os prende em um modo crônico e favorável ao tumor.
Da reação molecular em cadeia para tumores que crescem mais rápido
Para avaliar se essa sequência de eventos importa em organismos vivos, os cientistas criaram modelos murinos em que células humanas de câncer endometrial foram cultivadas junto com macrófagos semelhantes aos humanos. Quando lactato adicional foi fornecido, os tumores cresceram mais, mostraram mais células em divisão e continham mais macrófagos do tipo M2 senescentes com alto DNMT1 e baixo NHE7. Surpreendentemente, quando os macrófagos foram geneticamente modificados para superexpressar NHE7, isso atenuou o efeito de promoção tumoral do lactato: os tumores ficaram menores, apresentaram mais células em morte e continham menos macrófagos M2 e senescentes. Bloquear a enzima DNMT1 ou a via MAPK também enfraqueceu a capacidade do lactato de reprogramar macrófagos, reforçando a ideia de que essas moléculas formam um eixo conectado. 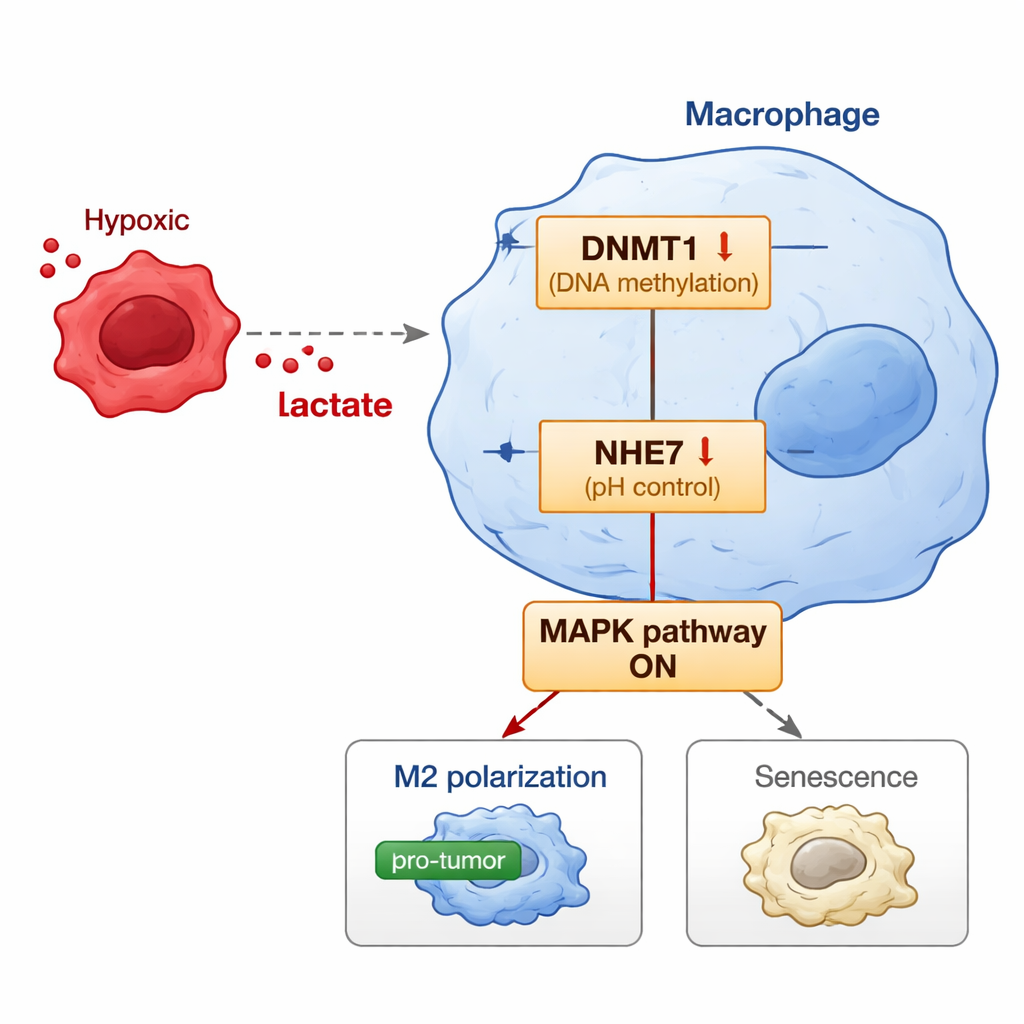
Transformando as artimanhas do tumor em alvos terapêuticos
Para não especialistas, a mensagem central é que tumores endometriais podem usar hipóxia e lactato — antes vistos apenas como restos celulares — para “lavar o cérebro” de células imunes próximas e fazê‑las ajudar o câncer. Eles fazem isso por meio de um retransmissor epigenético: o lactato aumenta DNMT1, que silencia NHE7, o que então ativa sinalização que fixa os macrófagos em um estado envelhecido e favorável ao tumor. Ao interferir em qualquer etapa dessa cadeia lactato–DNMT1–NHE7–MAPK, pode ser possível restaurar atividade imune anti‑tumoral e desacelerar o crescimento do câncer. Este trabalho aponta para futuras terapias que não atacam apenas as células tumorais diretamente, mas também reeducam as células imunes circundantes que o tumor transformou a seu favor.
Citação: Yang, S., Ma, Y., Wu, T. et al. Lactate transmission from hypoxic tumor cells promotes macrophage senescence and M2 polarization via the DNMT1-NHE7 axis to accelerate endometrial cancer progression. Cell Death Dis 17, 185 (2026). https://doi.org/10.1038/s41419-026-08411-y
Palavras-chave: câncer endometrial, microambiente tumoral, metabolismo do lactato, polarização de macrófagos, regulação epigenética