Clear Sky Science · pt
Além do metabolismo: explorando as implicações regulatórias e terapêuticas do lactato e da lactilação na morte celular regulada em câncer
Por que um “resíduo” do açúcar importa para o câncer
Durante décadas, o lactato — a substância que faz músculos sobrecarregados arderem — foi descartado como lixo celular. Esta revisão mostra que, no câncer, o lactato está longe de ser um resíduo. Ele atua como combustível, como sinal químico e até como um interruptor que pode decidir se células tumorais vivem ou morrem. Entender esse papel oculto pode abrir novas maneiras de levar células cancerígenas à autodestruição preservando tecidos saudáveis.
O atalho do açúcar que reprograma células cancerosas
As células cancerosas são notórias por seu “apetite por açúcar”. Mesmo quando o oxigênio é suficiente, elas preferem degradar glicose rapidamente em lactato em vez de oxidá‑la completamente nas mitocôndrias — uma mudança conhecida como efeito Warburg. Essa estratégia permite que tumores gerem energia e blocos de construção em alta velocidade. O afluxo resultante de lactato é bombeado para fora por transportadores específicos, moldando um microambiente tumoral ácido e rico em nutrientes que sustenta o crescimento e ajuda os tumores a se adaptarem ao estresse, como baixa oxigenação ou quimioterapia.
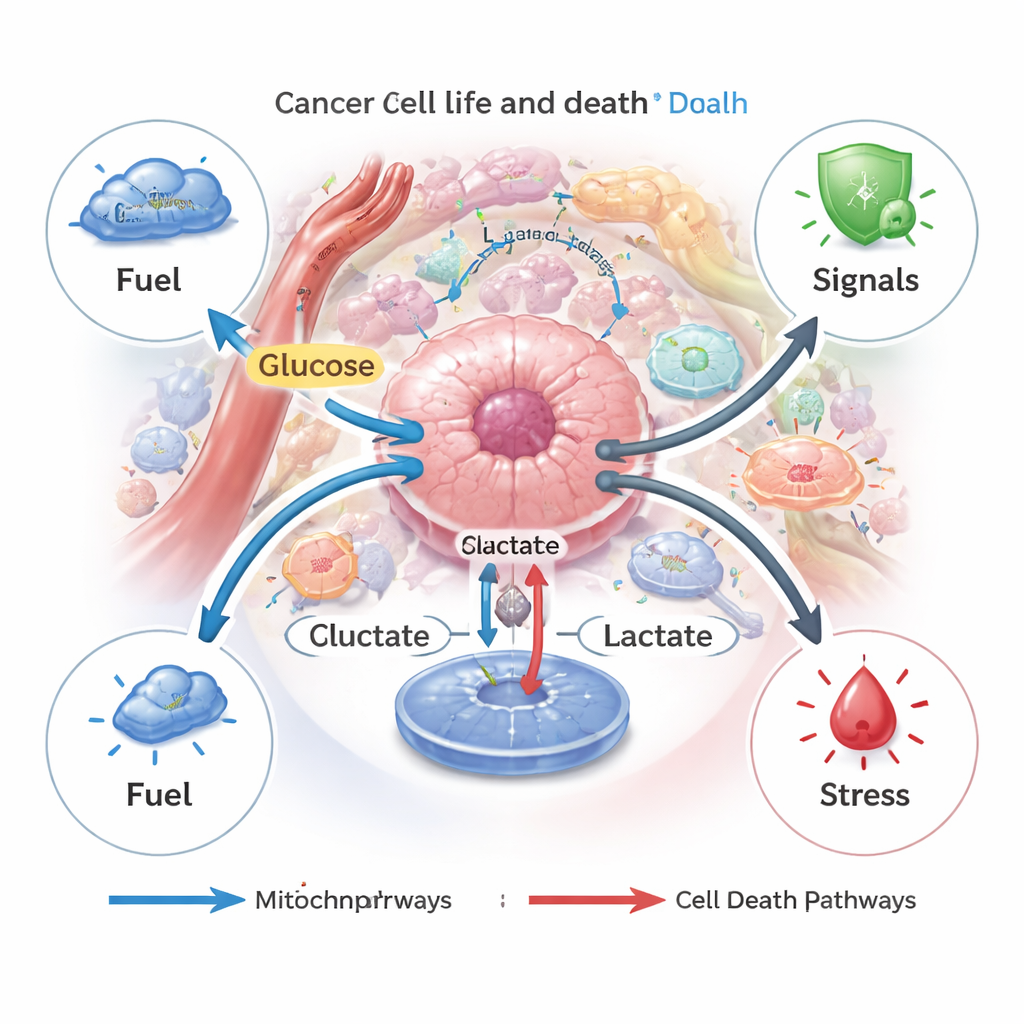
Lactato como regulador de diferentes formas de morte celular
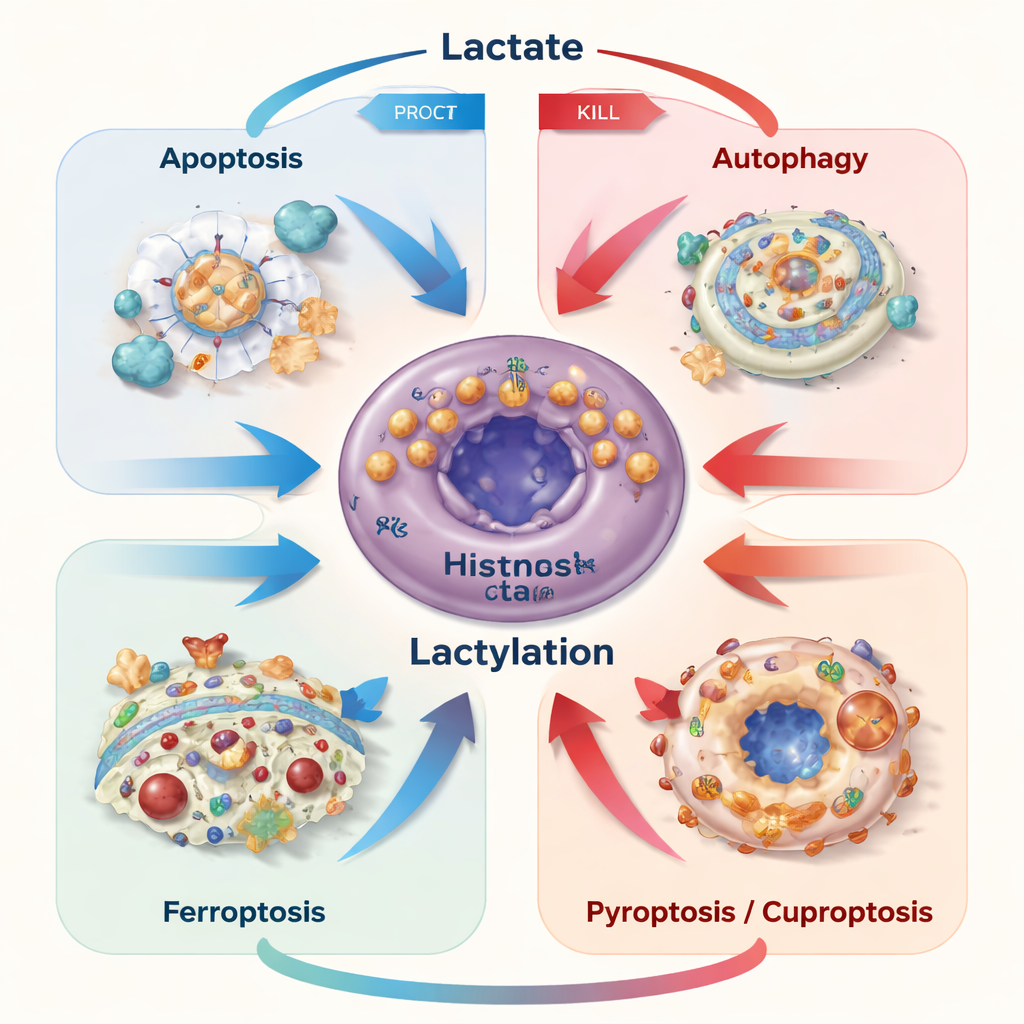
A morte celular em nossos corpos geralmente é rigidamente controlada, ajudando a remover células danificadas ou perigosas. Células cancerosas muitas vezes escapam desses programas. Os autores descrevem como o lactato pode tanto bloquear quanto desencadear várias vias de morte regulada — apoptose ("suicídio" celular), autofagia (autodigestão), ferroptose (lesão de membrana dependente de ferro), piroptose (ruptura inflamatória) e cuproptose (colapso induzido por cobre). Quando células tumorais geram ou importam quantidades moderadas de lactato, tendem a usá‑lo como combustível e sinal de sobrevivência, ativando vias que as protegem contra quimioterapia, escassez de nutrientes ou fármacos direcionados. Mas quando o lactato se acumula dentro das células, por exemplo se sua exportação é bloqueada, o estresse ácido e o dano mitocondrial resultantes podem inverter o interruptor e empurrar as células para a apoptose ou para a ferroptose.
Lactilação: quando o lactato escreve nas proteínas
Uma descoberta recente marcante é que o lactato pode ser convertido em uma pequena marca química e ligada a resíduos de lisina em proteínas, uma modificação conhecida como lactilação. Enzimas atuam como “escritores” e “apagadores” dessas marcas, decorando tanto histonas associadas ao DNA quanto muitas outras proteínas. Esses sinais alteram quais genes são ativados, como as enzimas se comportam e quão estáveis são reguladores-chave. No câncer, a lactilação ajusta finamente o equilíbrio entre sobrevivência e autodestruição. Pode, por exemplo, aumentar proteínas que bloqueiam a apoptose, intensificar a reciclagem via autofagia, proteger células da ferroptose ao controlar melhor o ferro e reforçar antioxidantes, ou modificar novas formas de morte como a cuproptose ao alterar o manejo de proteínas sensíveis ao cobre.
Uma conversa bidirecional entre metabolismo e programas de morte
O relacionamento não é unilateral: vias de morte celular também remodelam como os tumores usam açúcar e produzem lactato. Quando mitocôndrias são danificadas durante apoptose inicial ou mitofagia (remoção seletiva de mitocôndrias), as células frequentemente retornam à glicólise rápida, aumentando a produção de lactato. Células de suporte ao redor, como fibroblastos associados ao câncer, podem sofrer reprogramação semelhante e tornar‑se fábricas de lactato que alimentam células tumorais vizinhas. Outros tipos de morte, como a ferroptose, tendem a suprimir a glicólise e, portanto, reduzir os níveis de lactato. O resultado é um ciclo de retroalimentação dinâmico no qual metabolismo e mecanismos de morte se ajustam continuamente à medida que o tumor evolui e responde ao tratamento.
Transformando uma fraqueza em estratégia terapêutica
Como lactato e lactilação podem tanto proteger quanto matar células cancerosas dependendo do contexto, os autores defendem que as terapias precisam ir além de simplesmente bloquear a produção de lactato. Em vez disso, tratamentos futuros podem redirecionar seletivamente os fluxos de lactato, ajustar seus transportadores ou mirar marcas específicas de lactilação para levar as células tumorais ao colapso enquanto reativam células imunes antitumorais atualmente paralisadas pelo ambiente ácido. Sistemas inteligentes de liberação de fármacos e nanomedicinas que respondem a níveis locais de lactato ou pH surgem como formas de aplicar essa precisão. Em termos simples, a mensagem do artigo é que o que antes parecia lixo metabólico é, na verdade, um poderoso botão de controle do destino das células cancerosas — e aprender a girar esse botão corretamente pode tornar as terapias existentes muito mais eficazes.
Citação: Chen, C., Lin, A., Zhao, J. et al. Beyond metabolism: exploring the regulatory and therapeutic implications of lactate and lactylation in cancer-regulated cell death. Cell Death Dis 17, 184 (2026). https://doi.org/10.1038/s41419-026-08410-z
Palavras-chave: lactato, lactilação, morte de células cancerígenas, metabolismo tumoral, ferroptose