Clear Sky Science · pt
Espectro e funções de canais iônicos e transportadores em osteoclastos
Por que nossos ossos precisam de pequenos porteiros
Nosso esqueleto parece sólido e imutável, mas está constantemente sendo demolido e reconstruído. Células especializadas chamadas osteoclastos atuam como a equipe de demolição, dissolvendo osso antigo para que osso novo possa se formar. Este artigo de revisão explora um elenco oculto de proteínas microscópicas “porteiras” — canais iônicos e transportadores — que permitem que átomos carregados e nutrientes entrem e saiam dos osteoclastos. Ao entender como esses minúsculos portões controlam a degradação óssea, os cientistas esperam projetar tratamentos melhores para a osteoporose e outras doenças ósseas.
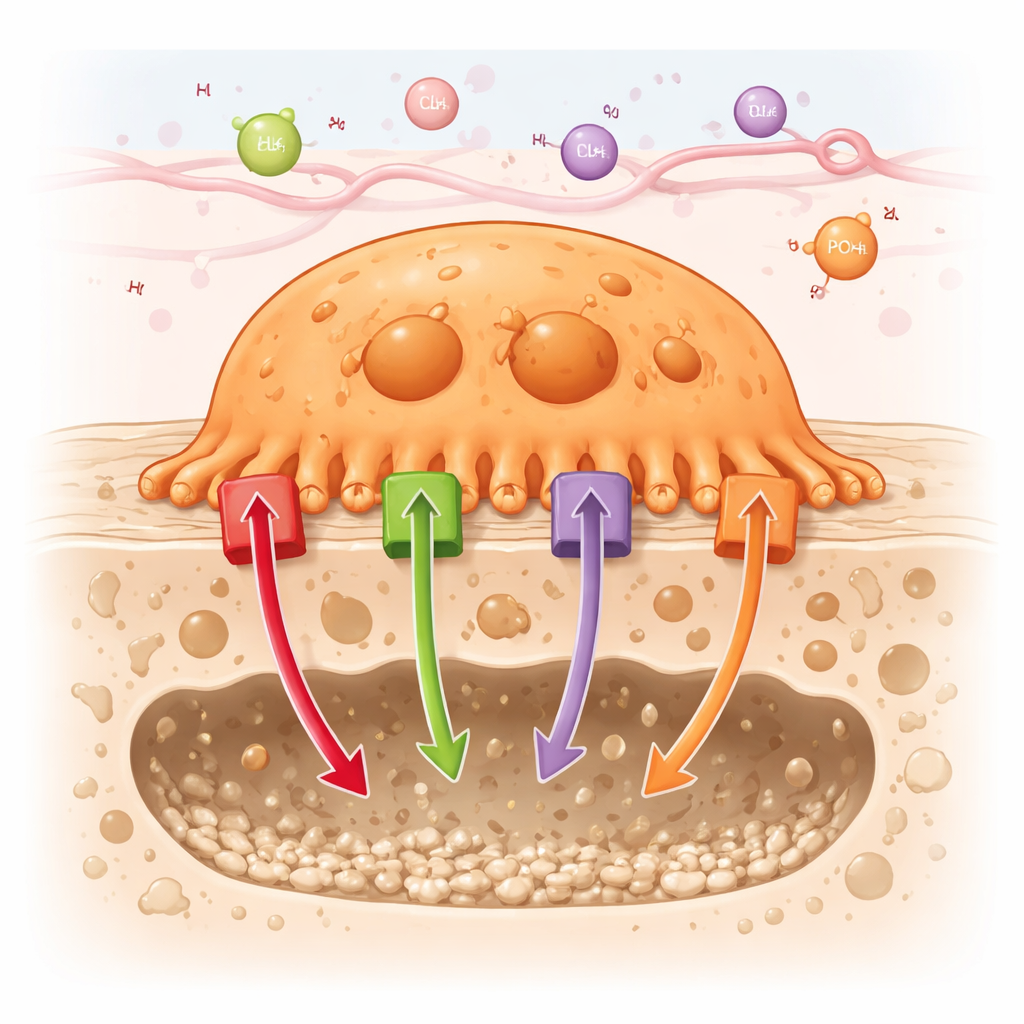
Como as células que comem osso fazem seu trabalho
Os osteoclastos atuam aderindo firmemente à superfície do osso e criando uma cavidade selada onde podem dissolver minerais e digerir proteínas com segurança. Para tornar essa “câmara de digestão” extremamente ácida, os osteoclastos bombeiam grande número de prótons (íons de hidrogênio) para dentro da cavidade. Ao mesmo tempo, eles transportam outros íons — como cloreto, cálcio e fosfato — através de suas membranas e compartimentos internos. O artigo faz um levantamento de cerca de 90 diferentes canais e transportadores encontrados em osteoclastos e os agrupa em seis famílias, incluindo bombas movidas a energia (ATPases), canais de cátions e ânions, transportadores acoplados, carreadores de nutrientes e transportadores da família de ATP‑binding cassette (ABC).
Ácido, sal e energia: a maquinaria central
Dois sistemas proteicos se destacam como centrais para a reabsorção óssea. Primeiro, bombas vacuolares de prótons conhecidas como V‑ATPases empurram ativamente prótons para a cavidade de reabsorção, tornando-a suficientemente ácida para dissolver o mineral ósseo e ativar enzimas que degradam proteínas. Subunidades específicas da V‑ATPase, como a3, d2 e vários componentes V1, estão enriquecidas na borda rugosa do osteoclasto e em lisossomos, e defeitos genéticos nessas subunidades podem enfraquecer o osso ou causar espessamento ósseo anormal. Segundo, um trocador cloreto–próton chamado ClC‑7, que atua em parceria com uma proteína chamada OSTM1, traz íons cloreto para a mesma área. Isso equilibra a carga elétrica e permite o bombeamento contínuo de prótons. Quando o ClC‑7 é mutado, humanos e camundongos desenvolvem osteopetrose, uma condição marcada por ossos excessivamente densos, porém frágeis, ilustrando o quão essencial é o fluxo iônico adequado para a saúde esquelética normal.
Cálcio, fosfato e outros coadjuvantes
Além da produção de ácido, os osteoclastos dependem de um manejo refinado de cálcio e fosfato. Uma rede de canais e bombas de cálcio na membrana celular, retículo endoplasmático, lisossomos e mitocôndrias gera “oscilações” rítmicas de cálcio que ativam genes-chave para a formação e fusão dos osteoclastos. Transportadores na borda rugosa e no lado oposto da célula movem cálcio e fosfato provenientes do osso dissolvido, reciclando-os dentro da célula ou devolvendo-os à corrente sanguínea. Outros metais e minerais — como manganês, magnésio, zinco, cobre e ferro — também são controlados por transportadores especializados e influenciam a agressividade com que os osteoclastos reabsorvem o osso. Por exemplo, o ferro e certas formas de morte celular ligadas ao ferro podem aumentar ou reduzir a atividade dos osteoclastos, enquanto transportadores de zinco tendem a conter perdas ósseas excessivas.
Controle de tráfego dentro da célula
Os canais iônicos não se limitam à membrana externa. Muitos estão em compartimentos internos, como lisossomos, endossomos, o aparato de Golgi e as mitocôndrias, criando uma rede de transporte em camadas. Esses portões internos ajudam a ajustar o pH em vesículas digestivas, a produção de energia nas mitocôndrias e o movimento de enzimas e detritos. A revisão destaca como múltiplos sistemas de canais trabalham em conjunto: trocadores sódio–hidrogênio regulam a acidez interna, cotransportadores potássio–cloreto ajudam a manter o potencial de membrana e o equilíbrio de cloreto, e canais purinérgicos e mecanossensíveis traduzem sinais químicos ou mecânicos em mudanças na reabsorção óssea. Transportadores de nutrientes para glicose, aminoácidos, nucleosídeos e vitamina C apoiam ainda mais as altas demandas energéticas e biossintéticas dos osteoclastos em atividade de reabsorção.
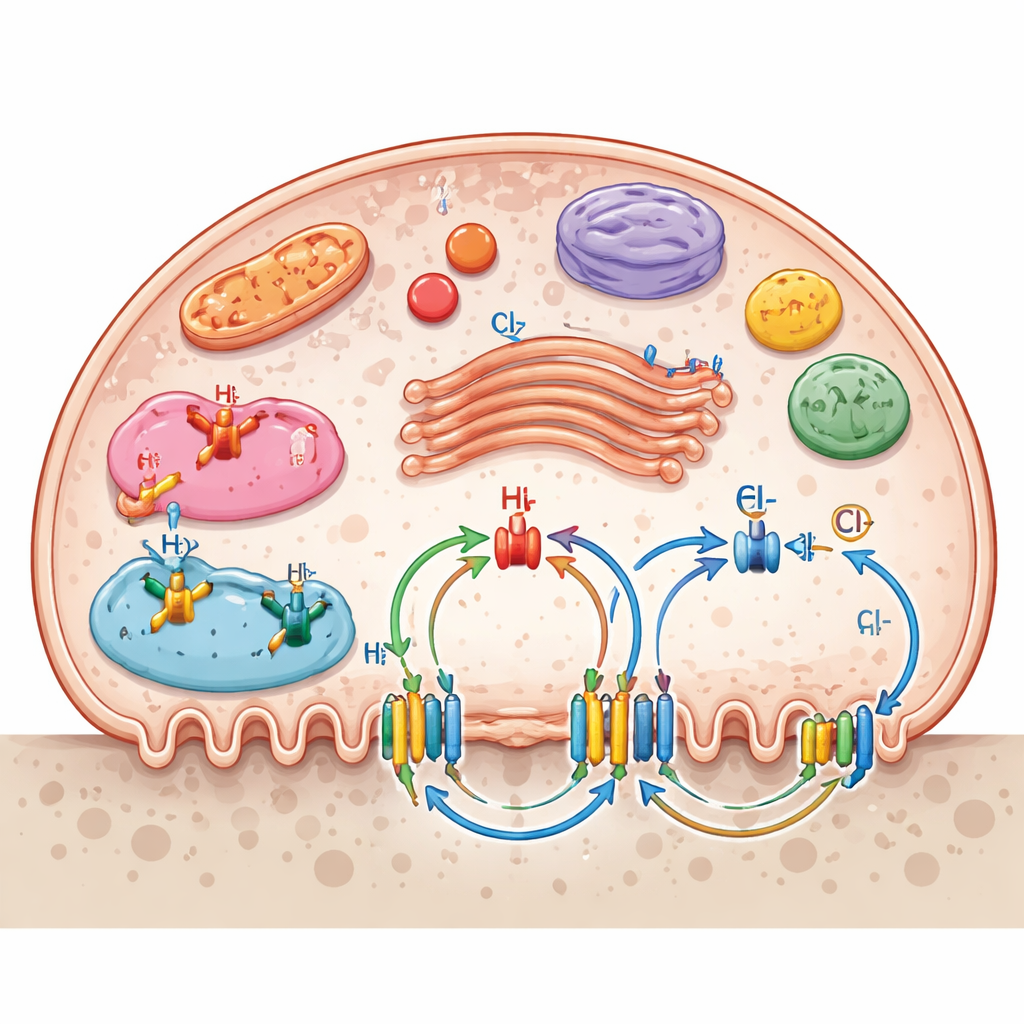
Da biologia básica a novos tratamentos
Como muitas doenças ósseas surgem quando osteoclastos estão hiperativos ou hipoativos, os canais e transportadores que orientam seu comportamento são alvos farmacológicos atraentes. Os autores revisam compostos existentes e experimentais que bloqueiam V‑ATPases, canais TRP de cálcio, trocadores de cloreto, receptores purinérgicos e outros transportadores, além de ideias mais recentes, como interromper interações entre subunidades específicas ou usar nanopartículas direcionadas para entregar fármacos diretamente ao osso. Enfatizam que muitas dessas proteínas também existem em outros tecidos, de modo que alcançar especificidade verdadeira para osteoclastos continua sendo um desafio. Ainda assim, à medida que ferramentas genômicas e de imagem revelam mais sobre onde esses canais estão e como interagem, o crescente “mapa iônico” dos osteoclastos provavelmente irá gerar terapias mais precisas para osteoporose, perda óssea inflamatória e doenças ósseas genéticas raras.
Citação: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
Palavras-chave: osteoclastos, canais iônicos, reabsorção óssea, V-ATPase, osteoporose