Clear Sky Science · pt
PRMT6 é necessário para iniciar e amplificar a inflamação induzida por macrófagos na ossificação heterotópica ao aumentar a expressão de CCL2
Quando a cicatrização vai longe demais
Às vezes, após uma lesão grave ou cirurgia, o corpo tenta tanto se curar que de fato cria novo osso onde não deveria existir. Essa condição dolorosa, chamada crescimento ósseo indesejado em tecidos moles, pode imobilizar articulações, complicar amputações e dificultar movimentos cotidianos. Os tratamentos atuais são limitados e frequentemente falham em impedir a recorrência do problema. Este estudo revela um interruptor precoce crucial do sistema imunológico que liga o trauma a essa formação óssea anormal — e aponta uma janela crítica e curta em que um tratamento direcionado poderia interromper o processo antes que ele comece. 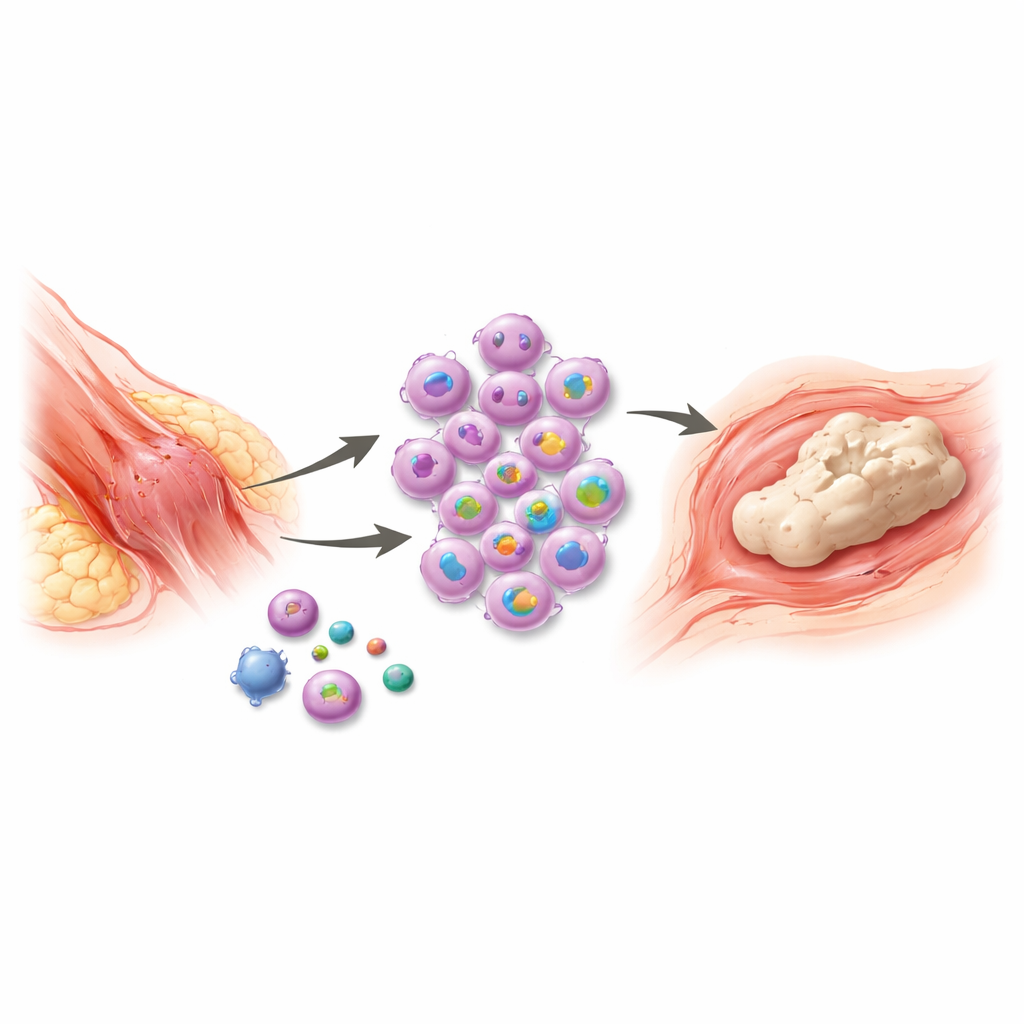
O problema do osso no lugar errado
Após traumas maiores, como queimaduras, fraturas ou cirurgias ortopédicas, alguns pacientes desenvolvem ilhas de osso dentro de músculos, tendões e outros tecidos moles. O novo osso forma-se por um processo semelhante ao desenvolvimento ósseo normal, começando com inflamação e terminando com tecido maduro e mineralizado. Embora os médicos saibam que células imunes chamadas macrófagos são centrais nessa resposta, o controle passo a passo de como elas iniciam e sustentam a inflamação não estava claro. Sem esse conhecimento, terapias como anti-inflamatórios, radiação ou remoção cirúrgica tardia tratam em grande parte as consequências, não a causa, e a recorrência é comum.
O intermediário-chave da inflamação
Usando um modelo de camundongo que combina lesão de tendão com queimadura — imitando de perto o trauma severo em humanos — os pesquisadores acompanharam o que acontece no local da lesão ao longo do tempo. Eles observaram um acúmulo rápido de macrófagos nos primeiros dias após a lesão, que depois persistiu conforme o osso anormal se formava. Quando essas células foram depletadas, o osso extra praticamente desapareceu, e o tecido circundante mostrou muito menos comprometimento dos vasos sanguíneos e das células de suporte. Uma análise genética mais profunda do tecido lesionado destacou uma molécula nesses macrófagos que se sobressaiu: PRMT6, uma enzima que modifica proteínas e ajuda a controlar quais genes são ativados.
Um botão de volume molecular para a inflamação
A equipe constatou que os níveis de PRMT6 nos macrófagos aumentavam rapidamente após a lesão e em resposta a sinais de perigo e componentes bacterianos em laboratório. Camundongos sem PRMT6, ou aqueles em que o PRMT6 foi seletivamente reduzido apenas nos macrófagos, apresentaram muito menos macrófagos no local da lesão e desenvolveram significativamente menos osso anormal. Importante, os tendões lesionados nesses animais realmente cicatrizaram melhor, com tecido mais ordenado e menor formação de cicatriz. Isso indica que PRMT6 não é necessário para a reparação saudável, mas atua como um botão de volume que amplifica a inflamação prejudicial. Quando os pesquisadores bloquearam PRMT6 com um fármaco, isso só funcionou se administrado precocemente — durante as primeiras semanas após a lesão. Iniciar o tratamento mais tarde teve pouco efeito, revelando uma janela terapêutica estreita, porém poderosa. 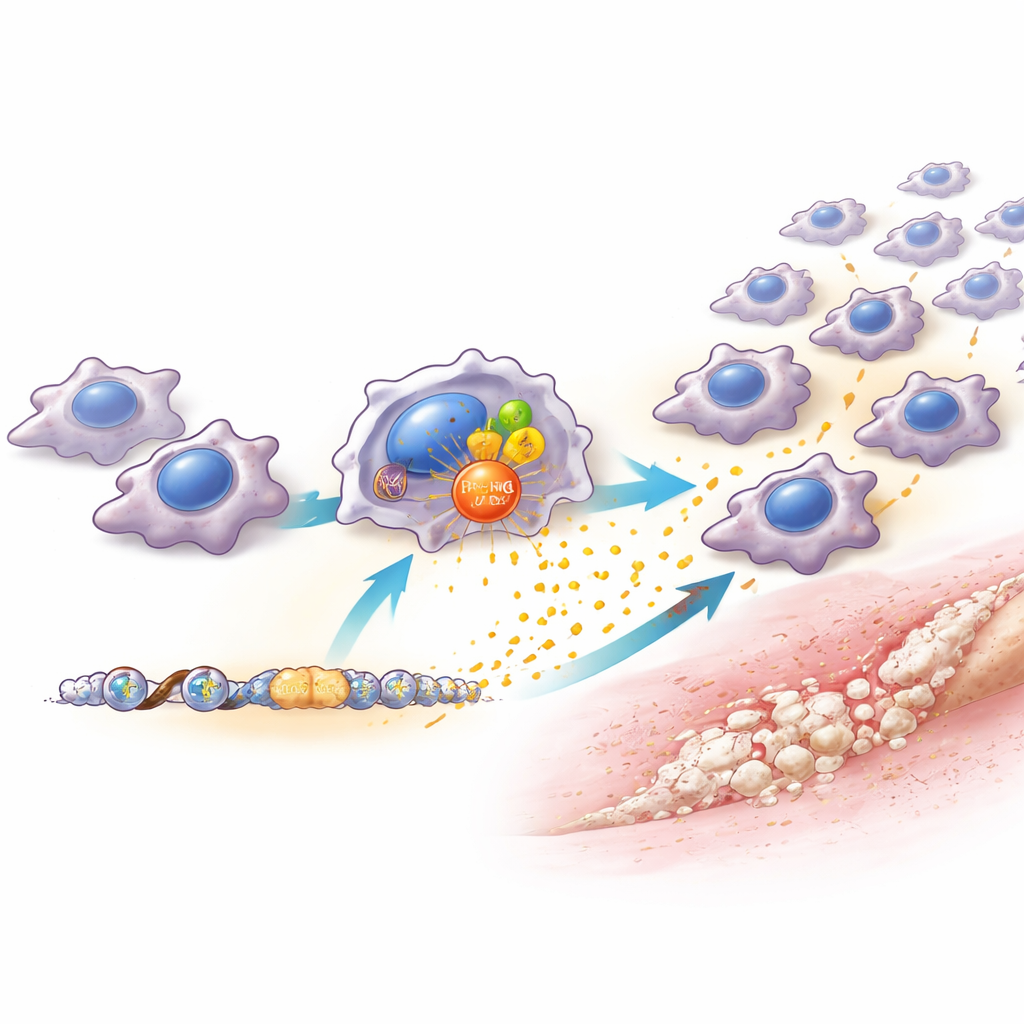
Como um sinal atrai muitas células imunes
Para entender como PRMT6 exerce esse efeito, os cientistas estudaram os macrófagos em detalhe. Sem PRMT6, essas células produziram quantidades muito menores de vários atrativos químicos, especialmente um chamado CCL2, que normalmente atrai mais monócitos e macrófagos da corrente sanguínea para o tecido lesionado. PRMT6 ajuda a ativar o gene CCL2 de duas maneiras: coopera com o conhecido controlador da inflamação NF-κB, e marca quimicamente as proteínas que empacotam o DNA nas proximidades para tornar esse gene mais fácil de ser lido. Como resultado, macrófagos com altos níveis de PRMT6 secretam mais CCL2, recrutando mais macrófagos e construindo um “centro de inflamação” que nutre vasos sanguíneos e células progenitoras formadoras de osso. Quando CCL2 foi especificamente reduzido apenas nos macrófagos, o resultado imitou de perto a perda de PRMT6 — menos macrófagos, nichos inflamatórios mais fracos e menos osso extra. Reintroduzir CCL2 restaurou parcialmente tanto o influxo de macrófagos quanto o crescimento ósseo anormal.
Uma oportunidade direcionada para prevenir o osso indesejado
Em conjunto, o estudo mostra que PRMT6 em macrófagos atua como um amplificador epigenético precoce: ele potencializa um sinal químico chave que recruta mais células imunes, as quais por sua vez impulsionam a formação de osso onde não deveria haver. Como bloquear PRMT6 apenas durante a fase inflamatória inicial reduziu drasticamente o osso indesejado enquanto deixava a cicatrização normal do tendão intacta — e até melhorou a organização tecidual — essa via oferece uma estratégia nova e promissora. Em princípio, um curto curso de terapia direcionada a PRMT6, bem cronometrado após trauma ou cirurgia grave, poderia prevenir incapacidades a longo prazo causadas por osso ectópico, sem comprometer a capacidade natural do corpo de se reparar.
Citação: Chu, W., Peng, W., Wu, Z. et al. PRMT6 is required for initiating and amplifying macrophage-induced inflammation in heterotopic ossification by increasing CCL2 expression. Bone Res 14, 29 (2026). https://doi.org/10.1038/s41413-026-00512-w
Palavras-chave: ossificação heterotópica, macrófagos, inflamação, regulação epigenética, sinalização CCL2