Clear Sky Science · pt
C/EBPβ determina a transcrição de FSHβ pós-menopausa e o bloqueio da via AEP/C/EBPβ alivia a osteoporose
Por que esta pesquisa importa para a vida após a menopausa
Muitas mulheres ouvem que a queda do estrogênio é a principal responsável pela fragilidade óssea após a menopausa. Este estudo acrescenta uma nova peça ao quebra-cabeça: outro hormônio, o hormônio folículo‑estimulante (FSH), e um par de proteínas no cérebro e no osso — C/EBPβ e AEP — atuam em conjunto para acelerar a perda óssea. Ainda mais intrigante, os pesquisadores mostram em camundongos que bloquear essa via com um comprimido experimental pode proteger os ossos tão efetivamente quanto um medicamento aprovado para osteoporose.
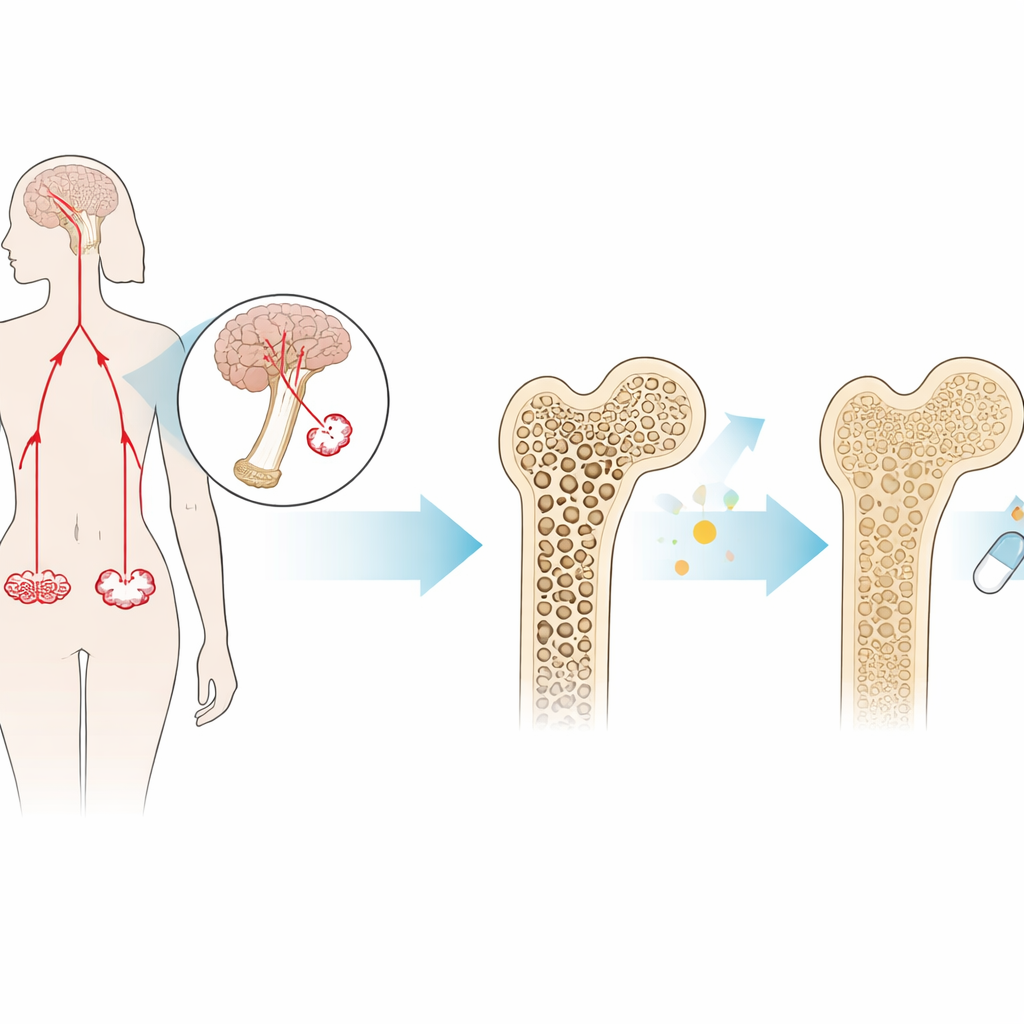
Um hormônio pouco conhecido com grande impacto no osso
O FSH é produzido na hipófise e é mais conhecido por seu papel na fertilidade. Em mulheres que se aproximam da menopausa, os níveis de FSH sobem acentuadamente vários anos antes do último período menstrual. Além de sua função reprodutiva, o FSH pode agir diretamente no osso: ele se liga a receptores em células que reabsorvem osso (osteoclastos), estimulando‑as a remover tecido ósseo mais rápido do que ele é reconstruído. Trabalhos anteriores mostraram que camundongos sem FSH ou sem seu receptor ficam protegidos da perda óssea, mesmo quando o estrogênio é baixo. Isso sugeriu que o próprio FSH, e não apenas a deficiência de estrogênio, pode impulsionar a osteoporose pós‑menopausa.
O interruptor de controle na hipófise
O novo estudo foca em C/EBPβ, uma proteína que se une ao DNA e liga ou desliga genes. Os autores descobriram que C/EBPβ se liga diretamente à região de controle do gene da subunidade beta do FSH — a parte do hormônio que determina sua identidade — e aumenta sua produção na hipófise. Em células hipofisárias em cultura, aumentar C/EBPβ elevou o FSH, enquanto silenciar C/EBPβ reduziu o FSH, especialmente quando as células eram estimuladas pelo sinal reprodutivo do cérebro, o GnRH. Em camundongos ovariectomizados, que imitam a menopausa ao remover os ovários produtores de estrogênio, animais com C/EBPβ reduzido produziram muito menos FSH na hipófise e no sangue. Esses experimentos revelam C/EBPβ como um interruptor chave que determina o quanto o FSH aumenta após a queda do estrogênio.
Um laço autorreforçador e um novo alvo farmacológico
C/EBPβ também controla outra proteína chamada AEP, uma enzima de clivagem que pode ativar ou desativar outras moléculas. No cérebro, a cadeia C/EBPβ–AEP foi associada a danos semelhantes aos do Alzheimer. Aqui, a equipe investigou se essa mesma cadeia retroalimenta o FSH e o osso. Em camundongos sem AEP, os níveis de C/EBPβ e FSH caíram na hipófise, e a perda óssea após a remoção dos ovários foi reduzida. Bloquear a AEP com uma droga de pequena molécula, apelidada de #11a, produziu efeito semelhante: após meses de tratamento, camundongos ovariectomizados apresentaram FSH mais baixo, ossos mais fortes em tomografias de alta resolução e menos células reabsorventes ósseas hiperativas. Outra classe de compostos — ativadores de TrkB que indiretamente reduzem a AEP — ajudou células ósseas em cultura, mas não conseguiu diminuir o FSH em animais, em grande parte porque seu receptor alvo é raro na hipófise. Esse contraste reforçou a conclusão de que inibir diretamente a AEP é uma maneira mais poderosa de desligar o eixo C/EBPβ–FSH em sua fonte.
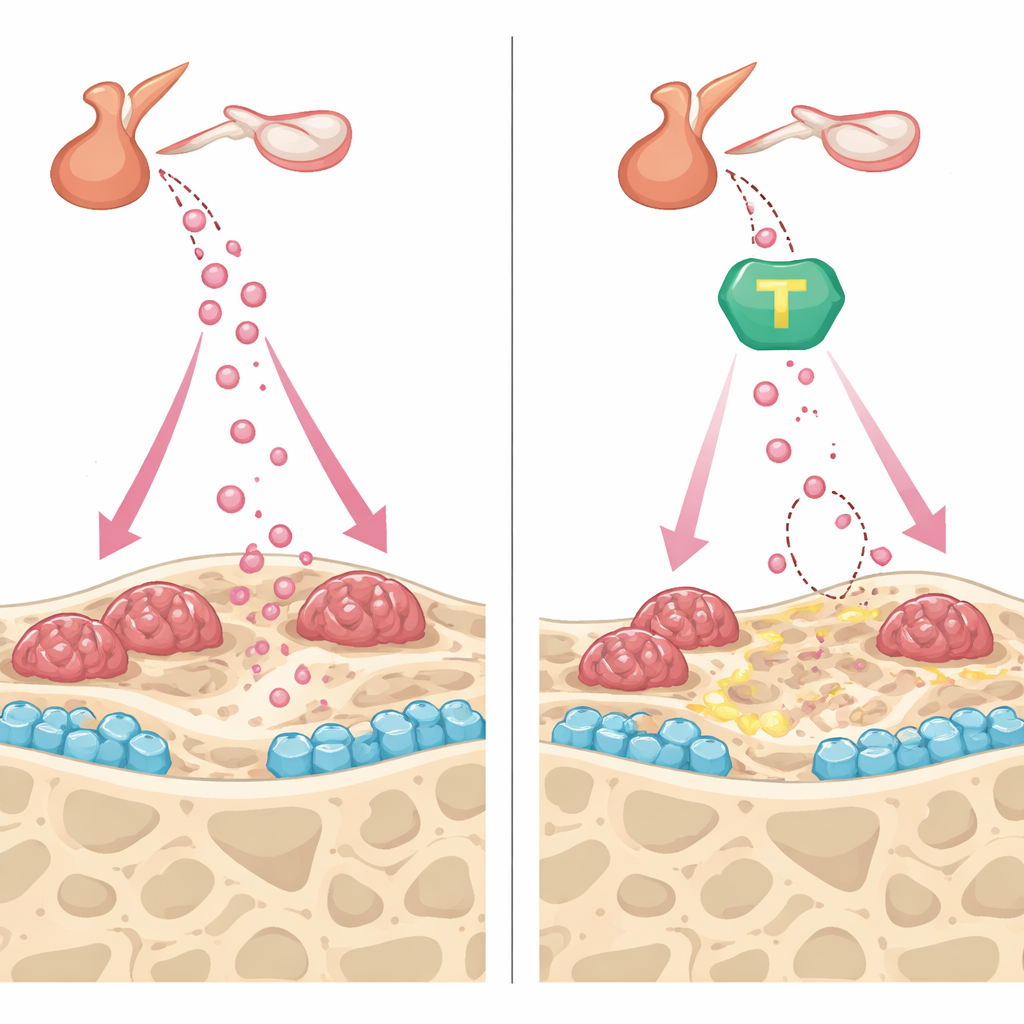
Protegendo o osso por duas frentes
Além de reduzir o FSH, #11a e o ativador de TrkB CF3CN mostraram benefícios complementares dentro do próprio osso. Em culturas de células formadoras de osso, ambos os compostos aceleraram a maturação e a deposição mineral, em parte preservando a fibronectina, uma proteína estrutural que a AEP normalmente cliva, e aumentando sinais pró‑ósseos como a osteoprotegerina. Nas células reabsorventes do osso, os medicamentos atenuaram os efeitos de um sinal chave de reabsorção, reduzindo o número de grandes células multinucleadas e sua capacidade de escavar sulcos em fatias de osso. Em camundongos vivos, tanto #11a quanto CF3CN contiveram o rápido turnover ósseo desencadeado pela remoção dos ovários, estabilizando a densidade e a microarquitetura óssea. Notavelmente, quando #11a foi comparado diretamente com teriparatida, um injetável aprovado pelo FDA que constrói osso, o comprimido experimental igualou a capacidade da teriparatida de restaurar o volume e a resistência óssea nesse modelo.
O que isso pode significar para o futuro do tratamento da osteoporose
Para um público não especializado, a conclusão é que este trabalho identifica uma via com dupla função que liga a inflamação associada à menopausa ao aumento do FSH e ao dano ósseo, e mostra que mirar na AEP pode interromper essa cadeia. Em camundongos, um inibidor oral de AEP não apenas reduz o excesso de FSH que alimenta a perda óssea, mas também desloca diretamente o equilíbrio dentro do osso em favor da formação em vez da degradação. Embora esses achados ainda precisem ser testados em pessoas, eles sugerem que tratamentos futuros para osteoporose podem ir além de simplesmente repor estrogênio ou estimular a formação óssea, e em vez disso silenciar esse circuito hormonal e enzimático recém mapeado que impulsiona a fragilidade óssea pós‑menopausa.
Citação: Xie, Z., Liao, J., Xiong, J. et al. C/EBPβ dictates postmenopausal FSHβ transcription and blockade of AEP/C/EBPβ pathway alleviates osteoporosis. Bone Res 14, 31 (2026). https://doi.org/10.1038/s41413-026-00510-y
Palavras-chave: osteoporose pós-menopausa, hormônio folículo-estimulante, via C/EBPβ AEP, remodelação óssea, terapia hormonal direcionada