Clear Sky Science · pt
A formação de cicatriz fibrótica induzida por TGF-β limita a recuperação de lesão na medula espinhal
Por que as cicatrizes na medula espinhal importam
Quando a medula espinhal sofre um ferimento grave, muitas pessoas ficam com paralisia permanente ou perda de sensibilidade porque as fibras nervosas danificadas não conseguem crescer de volta. Este estudo faz uma pergunta simples, porém crucial: o que, exatamente, está bloqueando esse recrescimento — e podemos remover essa barreira com segurança? Ao desvendar como um tipo particular de cicatriz se forma dentro da medula lesionada, os autores apontam uma nova maneira de ajudar o sistema nervoso a se reparar.
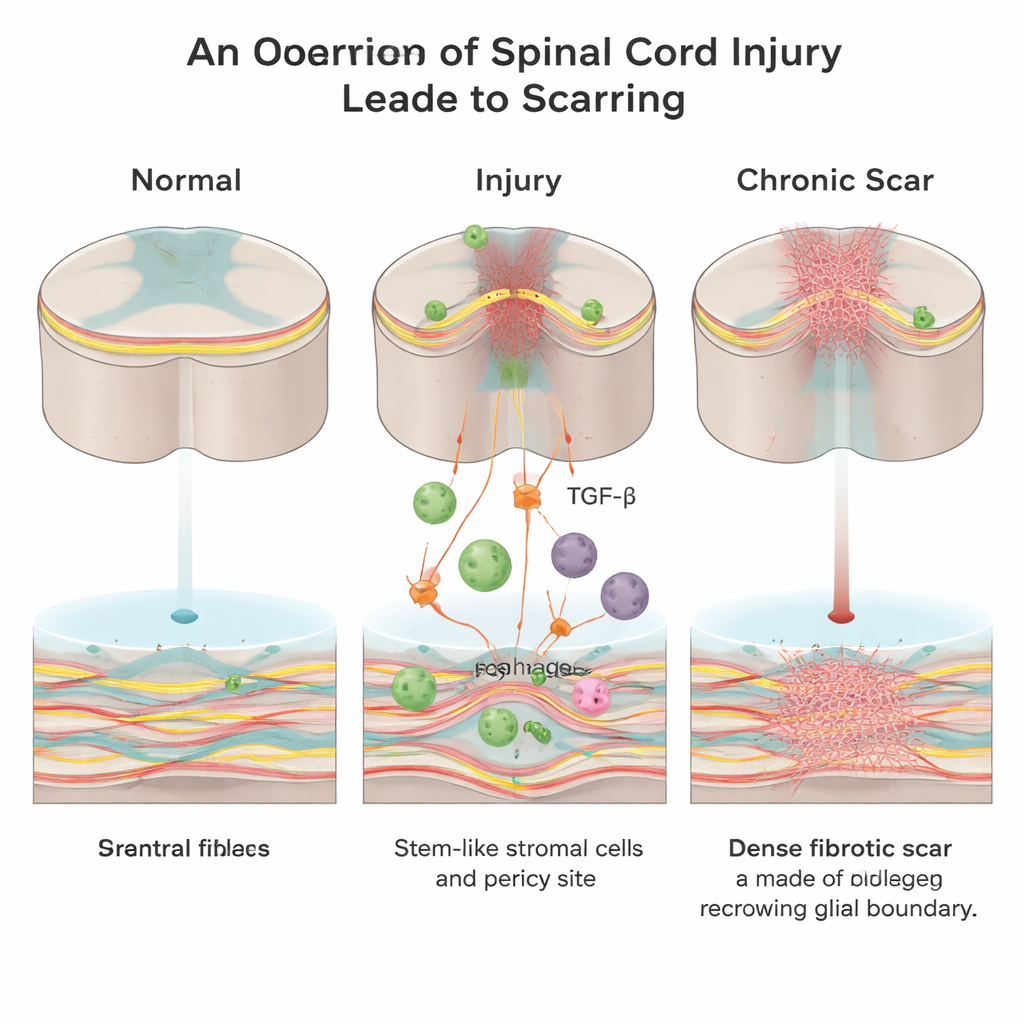
Uma parede escondida dentro da lesão
Após uma lesão na medula espinhal, o corpo corre para selar a ferida. Dois tipos principais de tecido cicatricial se formam: uma cicatriz “glial” produzida por células de suporte chamadas astrócitos, e uma cicatriz “fibrótica” rica em colágeno, fibronectina e células fibroblásticas. Enquanto a cicatriz glial pode ter papéis protetores, a cicatriz fibrótica cria uma barreira física e química densa que as fibras nervosas em crescimento não conseguem atravessar facilmente. Até agora, os cientistas sabiam muito menos sobre como esse núcleo fibrótico aparece e quais sinais impulsionam sua formação.
O papel das células imunes e de um sinal poderoso
Trabalhando com camundongos adultos, os pesquisadores se concentraram em uma molécula sinalizadora chamada fator de crescimento transformador beta (TGF-β), que ajuda a coordenar a reparação de feridas em todo o corpo e costuma estar hiperativa em doenças fibróticas. Eles descobriram que, após a lesão na medula espinhal, células imunes invasoras conhecidas como macrófagos se tornam uma fonte importante de TGF-β1 ativo no local da lesão. Esse aumento de TGF-β1 recruta células estromais/mesenquimais locais e células associadas a vasos chamadas pericitos e as empurra a se transformarem em fibroblastos — exatamente as células que depositam a cicatriz fibrótica rica em colágeno.
Reduzindo o sinal para abrir um caminho
Para testar se essa via realmente causa cicatrização prejudicial, a equipe usou várias manobras genéticas em camundongos. Quando removeram os macrófagos, ou deletaram o gene de TGF-β1 apenas em células da linhagem macrófaga, a quantidade de tecido fibrótico na medula lesionada caiu acentuadamente, e mais fibras nervosas e vias contendo serotonina conseguiram atravessar a zona da lesão. Da mesma forma, deletar o receptor de TGF-β especificamente em pericitos reduziu a resposta dessas células ao TGF-β, levou a menos acúmulo de colágeno e melhorou movimento e sensibilidade em testes comportamentais. Importante: os pericitos e células semelhantes a células-tronco ainda existiam, mas eram menos propensos a se tornar fibroblastos formadores de cicatriz.
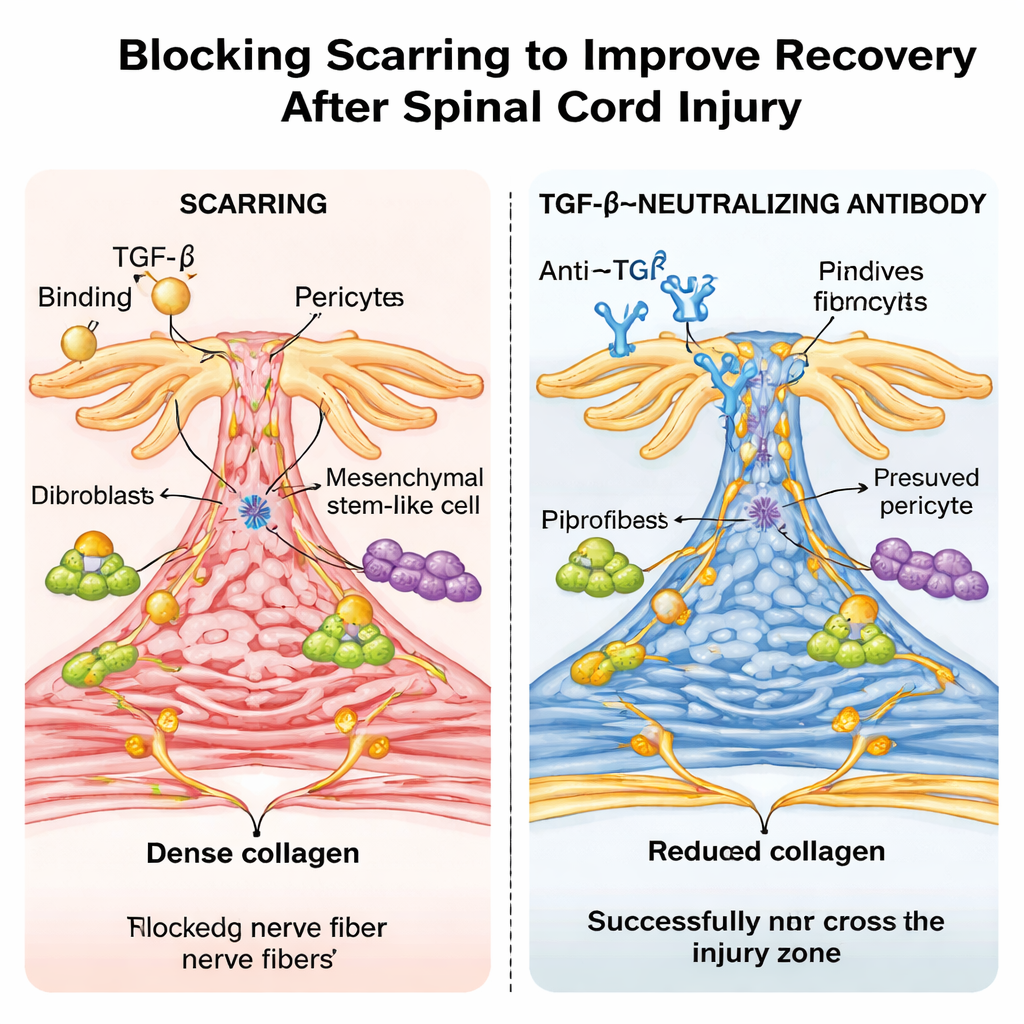
Um anticorpo tipo fármaco e um efeito surpreendente da idade
Os pesquisadores então testaram uma abordagem mais clinicamente relevante: tratar camundongos comuns com um anticorpo de laboratório que neutraliza o TGF-β. Doses repetidas após a lesão reduziram os níveis de TGF-β ativo no sangue e na medula espinhal, encolheram a cicatriz fibrótica e permitiram que fibras nervosas conectassem melhor a lesão, com ganhos marcantes na marcha e na função sensorial. Sequenciamento de RNA de célula única confirmou que genes responsivos ao TGF-β estavam altamente ativos em tipos celulares formadores de cicatriz em camundongos não tratados e foram suprimidos pelo anticorpo. Surpreendentemente, quando o mesmo tipo de esmagamento da medula espinhal foi realizado em camundongos recém-nascidos, os animais cicatrizaram praticamente sem formação de cicatriz fibrótica, não apresentaram ativação detectável de TGF-β no local da lesão e recuperaram movimento quase normal — lembrando a reparação sem cicatriz vista em alguns animais não mamíferos.
O que isso pode significar para tratamentos futuros
Em conjunto, os achados sugerem que a ativação excessiva de TGF-β após lesão na medula espinhal desvia células de reparo úteis para a construção de uma parede fibrótica rígida que bloqueia o recrescimento nervoso e a recuperação funcional. Ao impedir essa sobreativação — seja direcionando a produção de TGF-β em macrófagos, bloqueando seu receptor em pericitos e células estromais, ou usando um anticorpo neutralizante — pode ser possível reduzir a cicatriz prejudicial preservando ou até potencialmente aprimorando tipos de resposta tecidual mais benéficos. Embora a tradução dessas estratégias para humanos exija estudos cuidadosos para evitar efeitos colaterais, este trabalho destaca a cicatrização fibrótica mediada por TGF-β como uma barreira central, e potencialmente tratável com fármacos, à reparação da medula espinhal.
Citação: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
Palavras-chave: lesão da medula espinhal, cicatriz fibrótica, TGF-beta, macrófagos, regeneração nervosa