Clear Sky Science · pt
HIF-1α e BMAL1 na regeneração óssea: diálogo entre resposta à hipóxia e ritmo circadiano
Por que ossos quebrados cicatrizam melhor do que você imagina
Quando quebramos um osso ou extraímos um dente, nossos corpos iniciam silenciosamente um projeto de reparo surpreendentemente bem orquestrado. No interior da área lesionada, os níveis de oxigênio caem e nosso relógio interno dia‑noite continua a marcar o tempo. Este artigo explora como dois interruptores mestres—HIF‑1α, que detecta baixo oxigênio, e BMAL1, uma proteína central do relógio—trabalham em conjunto para guiar as células ósseas através da inflamação, do crescimento de novo tecido e da restauração final da resistência. Entender essa parceria pode melhorar tratamentos para fraturas, osteoporose, artrite e até implantes dentários.
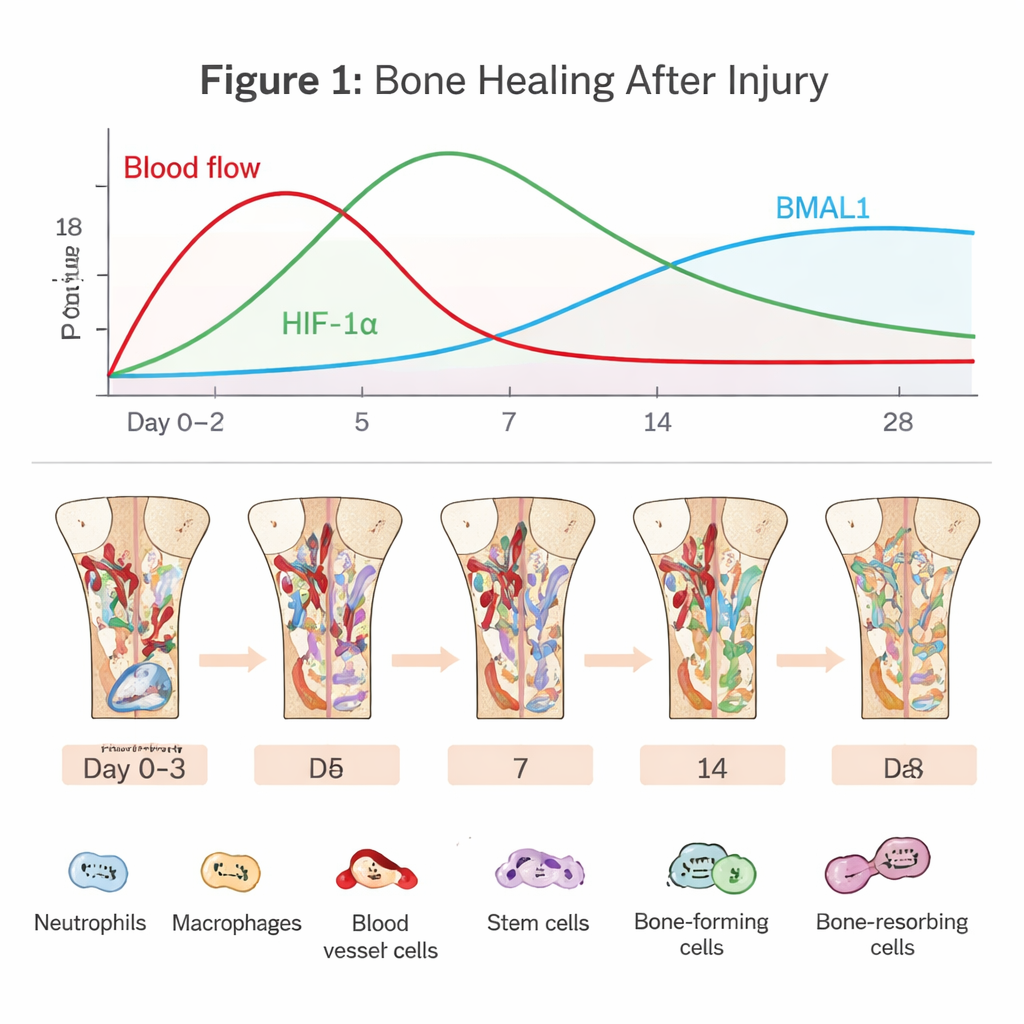
O drama oculto dentro de um osso em cicatrização
A regeneração óssea começa no momento em que vasos sanguíneos se rompem. Um coágulo se forma, interrompendo grande parte do fornecimento de oxigênio e criando um bolsão adverso de baixo oxigênio. Células imunes como neutrófilos e macrófagos correm para limpar detritos e proteger contra micróbios. Ao mesmo tempo, células‑tronco da medula óssea e células endoteliais são recrutadas para reconstruir a região. Essa fase inicial “inflamatória” é uma espada de dois gumes: um surto curto e bem cronometrado de inflamação acelera o reparo, mas se durar demais ou for muito intenso, a cicatrização pode estagnar ou falhar. O artigo enfatiza que navegar por esse caminho estreito depende fortemente de como as células percebem oxigênio e tempo.
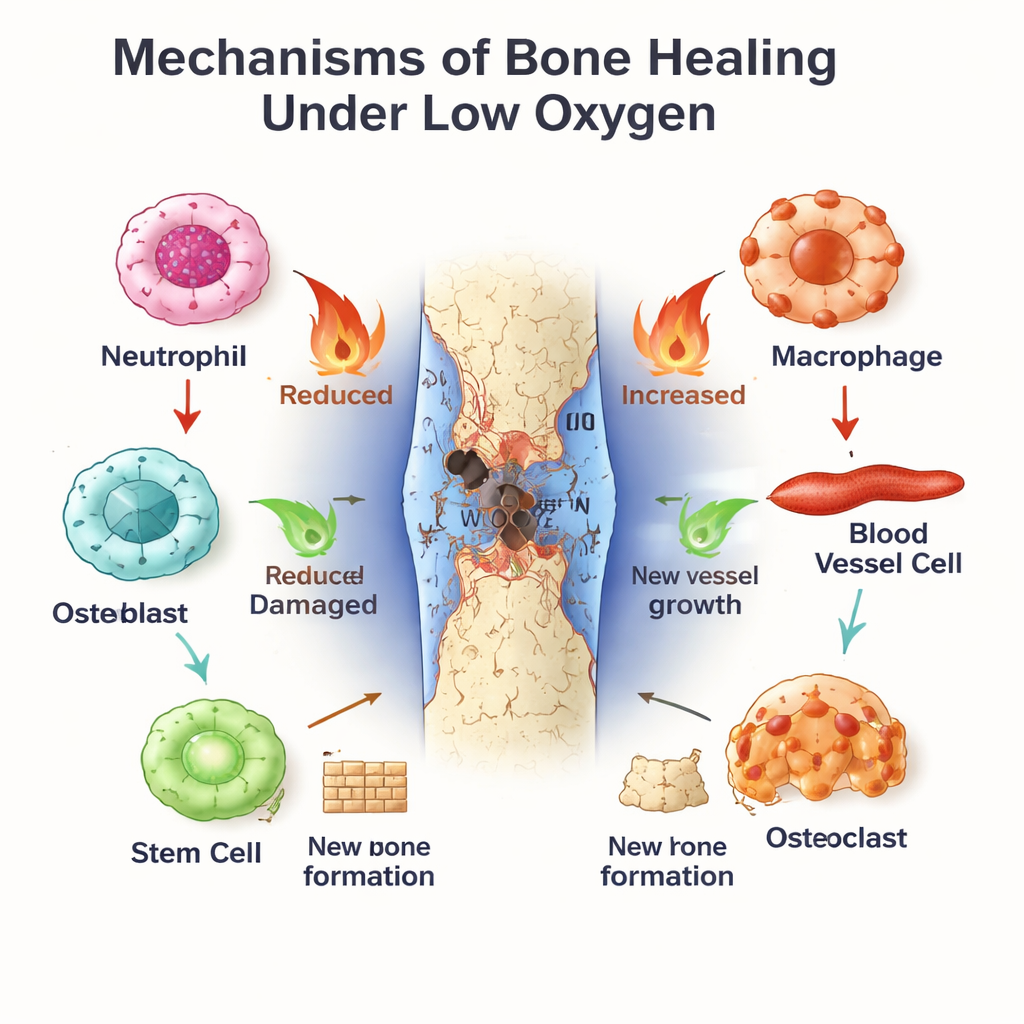
Como as células usam o baixo oxigênio a seu favor
Na zona de fratura pobre em oxigênio, a proteína HIF‑1α se estabiliza e liga genes que ajudam as células a se adaptar. Ela estimula células endoteliais a brotar novos vasos sanguíneos, garantindo que oxigênio e nutrientes frescos alcancem o defeito. Também reprograma o metabolismo celular para a glicólise, uma forma de gerar energia que funciona mesmo quando o oxigênio é escasso. Para células‑tronco e osteoblastos formadores de osso, uma ativação moderada de HIF‑1α pode aumentar proliferação, migração e formação óssea, em parte ao elevar fatores como VEGF que conectam a formação vascular ao novo osso. Mas se a hipóxia for muito severa ou prolongada, moléculas de estresse e espécies reativas de oxigênio se acumulam, levando osteoblastos à morte e estimulando osteoclastos que reabsorvem osso. O mesmo sinal hipóxico pode portanto apoiar ou sabotar a cicatrização, dependendo de sua intensidade e duração.
O relógio interno do corpo como gestor da reparação óssea
Rodando em paralelo está o relógio circadiano, um marcador molecular do tempo presente em quase todas as células. BMAL1, um de seus componentes centrais, ajuda a definir ritmos diários na atividade imune, no comportamento dos vasos sanguíneos e na diferenciação de células‑tronco. Neutrófilos e macrófagos exibem diferenças ao longo do dia na intensidade com que respondem à lesão e na rapidez com que envelhecem ou mudam de estados inflamatórios (semelhança M1) para estados de cura (semelhança M2). Em células vasculares e células‑tronco da medula óssea, BMAL1 promove proliferação saudável e formação óssea ordenada, em parte ajustando vias de crescimento como Wnt e TGF‑β/SMAD. Quando BMAL1 é perturbado—por defeitos genéticos, trabalho em turnos ou doença metabólica—os ossos tendem a perder massa, as células‑tronco se desgastam e o equilíbrio entre formação e degradação óssea se inclina para a perda.
Uma conversa entre detecção de oxigênio e o relógio corporal
O cerne da revisão é o emergente “diálogo” entre HIF‑1α e BMAL1. Essas duas proteínas compartilham estruturas semelhantes e podem interagir fisicamente, até formando pares mistos que se ligam ao DNA e controlam conjuntos sobrepostos de genes. Cada uma pode influenciar a produção e estabilidade da outra, criando circuitos de retroalimentação que ligam o timing do ciclo dia‑noite à forma como as células respondem à hipóxia. Juntas, elas também regulam o equilíbrio redox celular—quanto de espécies reativas de oxigênio danosas são produzidas versus quanta capacidade antioxidante está disponível—e co‑regulam enzimas-chave que decidem se as células dependem mais da respiração dependente de oxigênio ou da glicólise sem oxigênio. Esse controle conjunto ajuda a determinar se o ambiente da fratura favorece a reconstrução construtiva ou inflamação excessiva e reabsorção óssea.
O que isso significa para doença e tratamento
A mesma parceria HIF‑1α–BMAL1 aparece em muitas condições relacionadas ao osso. Em trabalhadores por turnos, sono perturbado e exposição à luz provavelmente alteram BMAL1, aumentam o estresse oxidativo e interferem na reparação guiada por HIF‑1α, contribuindo para a osteoporose. No diabetes, a hiperglicemia enfraquece tanto a função do relógio quanto a sinalização da hipóxia, comprometendo a formação vascular e a formação óssea dependente de células‑tronco. Na osteoartrite, a perda de BMAL1 em condrócitos desregula seu ritmo e sua relação protetora com HIF‑1α, acelerando a degradação da cartilagem. Ao redor de implantes de titânio, hipóxia controlada e um ritmo circadiano saudável parecem favorecer melhor osseointegração, sugerindo que futuros revestimentos de implantes poderiam ser projetados para ativar suavemente tanto HIF‑1α quanto BMAL1. Em geral, o artigo conclui que a regeneração óssea bem‑sucedida depende não apenas de quais células estão presentes, mas de como elas interpretam oxigênio e tempo—e que direcionar esse diálogo pode abrir novas vias para uma cicatrização mais rápida e mais resistente.
Citação: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
Palavras-chave: regeneração óssea, ritmo circadiano, hipóxia, osteoporose, cicatrização de fratura