Clear Sky Science · pt
Concentrações baixas de oligômeros de beta‑amiloide induzem sinaptogênese característica do comprometimento cognitivo leve e alteram o proteoma de novo
Alterações iniciais que podem sinalizar problemas de memória
Antes que a doença de Alzheimer roube a memória das pessoas, o cérebro passa por uma zona intermediária nebulosa conhecida como comprometimento cognitivo leve. Nesta fase, os problemas de raciocínio são notáveis, mas a vida cotidiana frequentemente continua. Curiosamente, algumas regiões cerebrais nesse estágio apresentam mais, e não menos, conexões entre neurônios. Este estudo investiga se pequenas quantidades de uma molécula tóxica relacionada ao Alzheimer podem impulsionar esse surto de novas conexões e se um fármaco já testado em pacientes com câncer poderia atenuar essas alterações muito precoces.
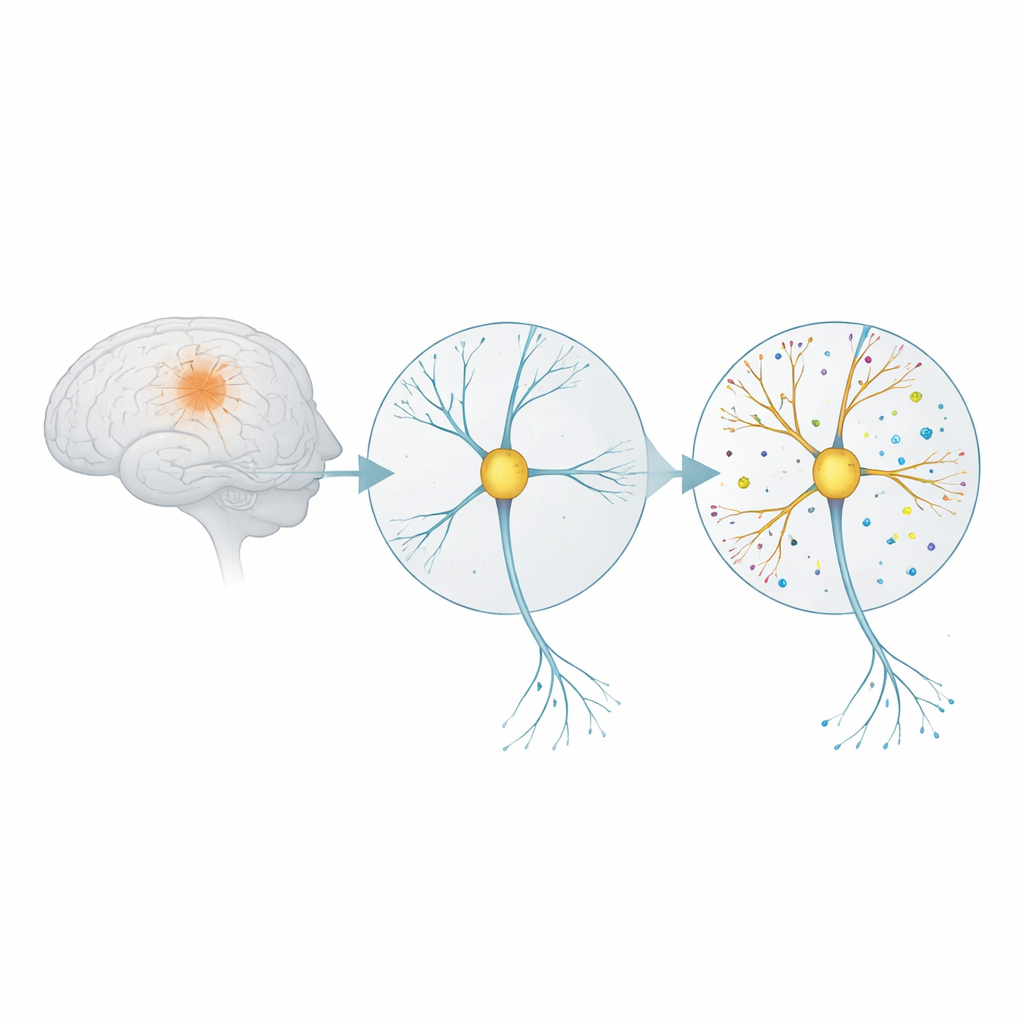
Como as conexões cerebrais reagem a um gatilho tóxico
A doença de Alzheimer está fortemente associada a pequenos aglomerados de um fragmento proteico chamado beta‑amiloide. Na forma de oligômeros, esse fragmento é particularmente prejudicial às sinapses — os pontos de contato onde os neurônios se comunicam. Os pesquisadores cultivaram células cerebrais de rato em placa até formarem redes maduras e, em seguida, as expuseram por cinco dias a uma dose baixa de oligômeros de beta‑amiloide. Também testaram o que ocorria quando adicionavam um composto chamado eFT508, que bloqueia uma enzima de sinalização (MNK) envolvida no início da produção de proteínas dentro das células. Esse arranjo foi projetado para imitar estágios muito precoces da doença, antes que ocorra morte celular generalizada.
Vendo detalhes ocultos de novas sinapses
Para examinar como as conexões mudaram, a equipe usou “microscopia de expansão”, uma técnica que expande fisicamente células preservadas dentro de um gel macio para que estruturas minúsculas possam ser vistas com muito mais detalhe. Eles marcaram fibras nervosas e ambos os lados da sinapse com etiquetas fluorescentes e as reconstruíram em 3D. A exposição ao beta‑amiloide causou um aumento claro no número de sinapses ao longo dos ramos dos neurônios. Em particular, houve mais botões simples — contatos simples um a um — e espinhas “multi‑inervadas” incomuns, onde mais de uma fibra entrante converge em um único sítio receptor. Esses padrões se assemelham aos aumentos sinápticos relatados em pessoas com comprometimento cognitivo leve. Quando o eFT508 esteve presente, o número de sinapses voltou a níveis próximos do normal, sugerindo que o fármaco poderia contrabalançar esse crescimento excessivo precoce.
Novas proteínas mudam, mesmo quando os totais não mudam
As sinapses se remodelam constantemente produzindo e degradando proteínas. A equipe, em seguida, investigou quais proteínas foram sintetizadas de novo durante e após a exposição ao beta‑amiloide. Eles forneceu aos neurônios um aminoácido artificial inofensivo que é incorporado em proteínas recém‑sintetizadas e, depois, usaram reações químicas de “click” e espectrometria de massa para isolar e identificar essas moléculas. Surpreendentemente, a quantidade total de proteína nova não mudou após vários dias de beta‑amiloide em baixa dose, com ou sem eFT508. Mas quando examinaram quais proteínas específicas foram produzidas, o quadro foi muito diferente: mais de mil proteínas recém‑sintetizadas foram detectadas, e dezenas delas mudaram para cima ou para baixo em resposta ao beta‑amiloide. Muitas estavam envolvidas na comunicação sináptica, na estrutura interna da célula, nas mitocôndrias produtoras de energia, nos sistemas de limpeza de resíduos e no controle de qualidade das proteínas.
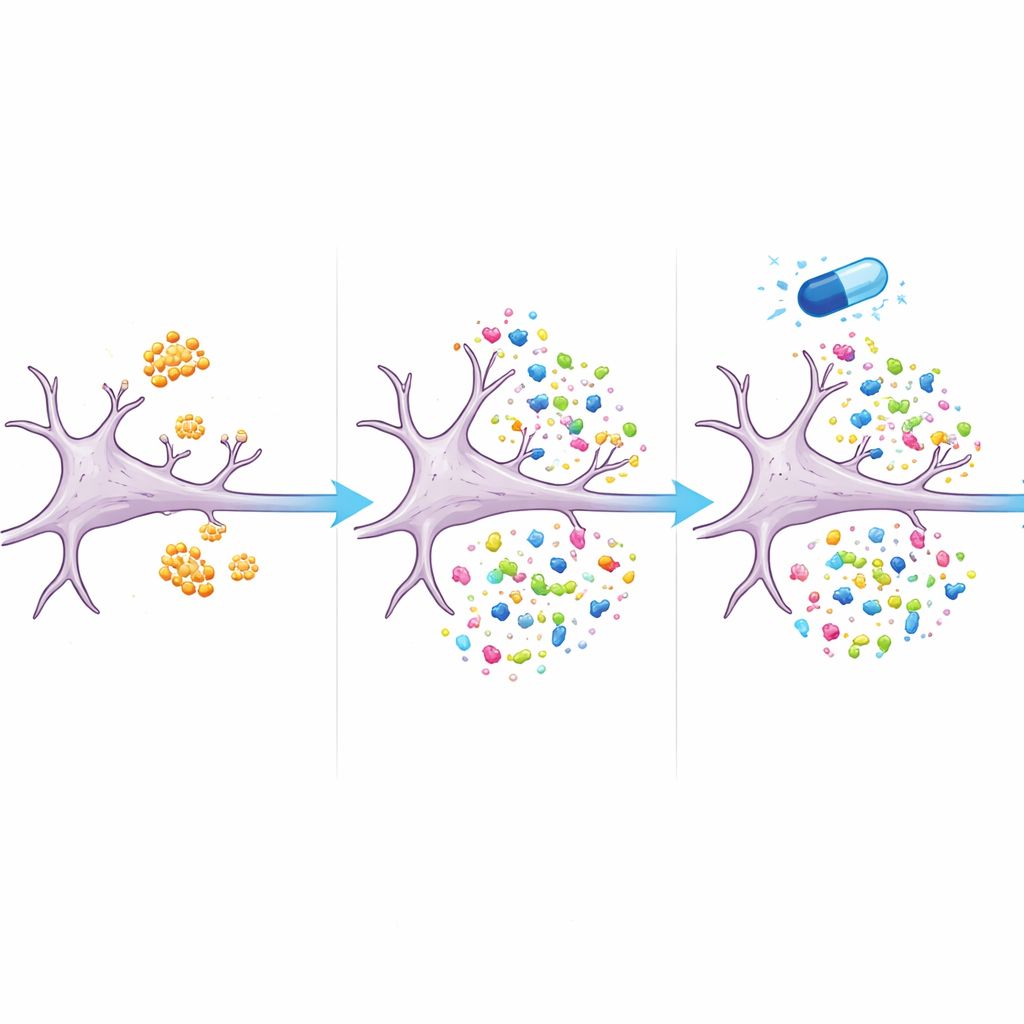
Um fármaco que orienta o equilíbrio proteico
De forma crucial, muitas das proteínas alteradas retornaram aos níveis próximos do normal quando as células foram tratadas com eFT508 juntamente com o beta‑amiloide. Mais de dois terços das proteínas alteradas apenas pelo beta‑amiloide não foram mais significativamente diferentes das células não tratadas quando o fármaco estava presente. Entre elas estavam proteínas relacionadas à estrutura e função sináptica, bem como componentes dos sistemas de reciclagem e de energia da célula. Os resultados sugerem que o eFT508 não simplesmente interrompe a produção de proteínas; em vez disso, parece remodelar quais proteínas são produzidas, inclinando o sistema para longe de um padrão semelhante ao do Alzheimer e em direção a um equilíbrio mais saudável.
O que isso pode significar para tratamentos futuros
Este trabalho desenha um quadro do dano inicial associado ao Alzheimer como uma fase de hiperconexão e sutil desorganização proteica, em vez de perda franca. Níveis baixos de beta‑amiloide impulsionam a formação de sinapses extras, às vezes incomuns, e distorcem seletivamente a mistura de proteínas que os neurônios produzem. Neste modelo em placa, o eFT508 pode tanto normalizar o número de sinapses quanto corrigir muitas das alterações proteicas, sugerindo que ajustar cuidadosamente a síntese proteica pode retardar ou impedir a progressão do comprometimento cognitivo leve para a demência plena. Embora muito ainda precise ser testado em animais vivos e em humanos, o estudo destaca uma nova forma de pensar sobre — e possivelmente intervir nos — estágios mais precoces da doença de Alzheimer.
Citação: Wu, K., Lee, S., Martinez-Serra, R. et al. Low concentrations of amyloid-beta oligomers induce synaptogenesis characteristic for mild cognitive impairment and alter the de novo proteome. Transl Psychiatry 16, 132 (2026). https://doi.org/10.1038/s41398-026-03905-x
Palavras-chave: Doença de Alzheimer, alterações sinápticas, oligômeros de beta amiloide, síntese de proteínas, neurodegeneração inicial