Clear Sky Science · pt
A modificação m6A mediada por METTL3 regula CDKN1A para atenuar o comprometimento cognitivo e a apoptose neuronal induzidos por privação crônica de sono em ratos
Por que noites em claro podem prejudicar sua memória
Muitas pessoas tratam a perda crônica de sono como parte normal da vida moderna, mas a ciência tem mostrado que a falta de sono pode danificar silenciosamente as áreas cerebrais responsáveis pela aprendizagem e memória. Este estudo em ratos investiga ao nível de moléculas individuais dentro de neurônios do hipocampo e identifica um interruptor químico específico — chamado METTL3 — que parece proteger as células cerebrais dos efeitos nocivos da privação crônica de sono. Entender esse interruptor pode, no futuro, apontar novas maneiras de proteger a memória em pessoas que não conseguem evitar a perda de sono com facilidade, como trabalhadores em turnos, cuidadores e pacientes com distúrbios do sono.
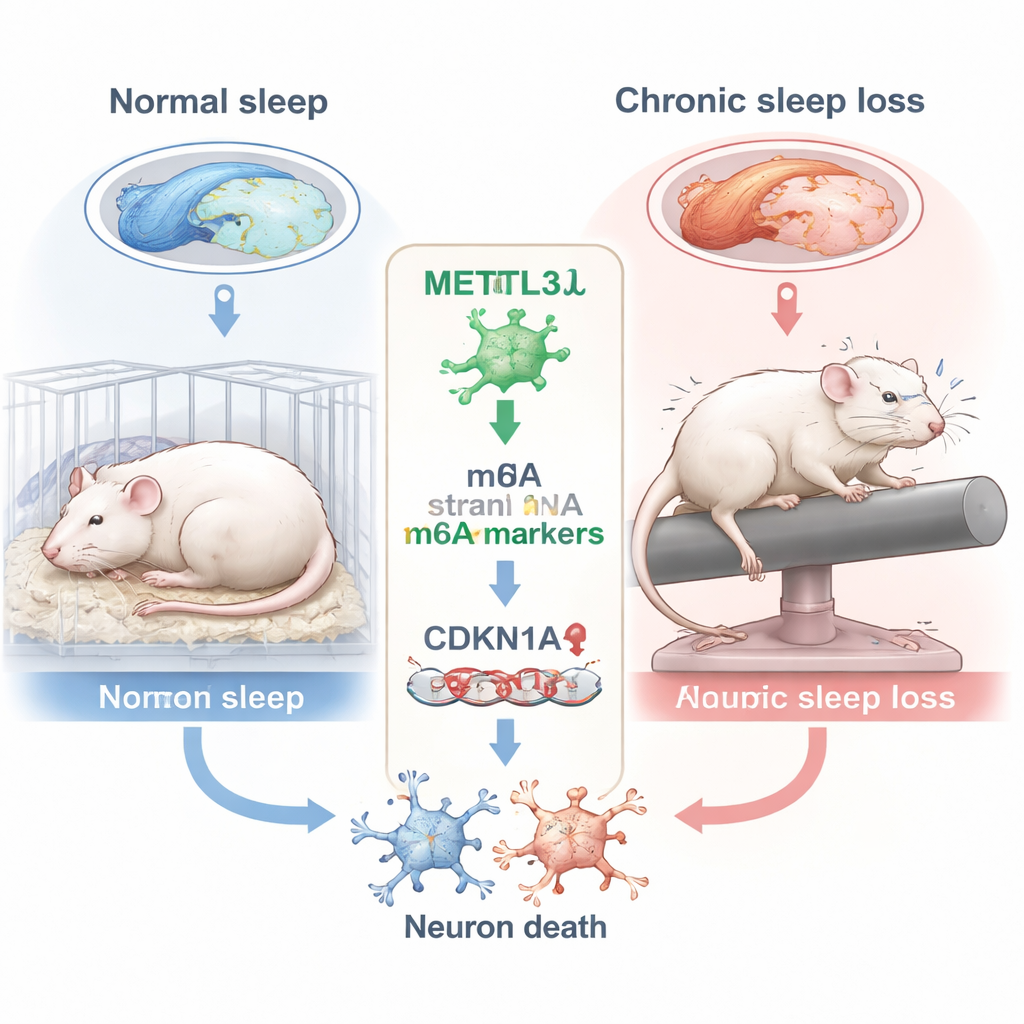
Como a perda de sono prolongada danifica o centro da memória
Os pesquisadores concentraram-se no hipocampo, uma região cerebral em forma de cavalo-marinho essencial para formar novas memórias. Dentro do hipocampo, focalizaram-se em uma sub-região chamada CA3, que ajuda a codificar e recuperar informações espaciais — habilidades testadas por tarefas como encontrar uma plataforma oculta na água. Ratos foram mantidos acordados por 10 horas por dia ao longo de seis semanas usando uma haste rotativa suave que os despertava repetidamente. Quando a memória foi testada no conhecido Labirinto Aquático de Morris, os ratos privados de sono percorreram rotas menos diretas, cruzaram menos vezes o local anterior da plataforma e passaram menos tempo no quadrante alvo — todos sinais de memória espacial prejudicada em comparação com animais bem descansados.
Uma marca química no RNA que desaparece
Para entender o que ocorria dentro dos neurônios da CA3, a equipe analisou uma etiqueta química no RNA chamada m6A, uma das marcas internas mais comuns no RNA mensageiro. Essas marcas ajudam a controlar por quanto tempo as moléculas de RNA duram e quão eficientemente são usadas para produzir proteínas. Uma enzima-chave que adiciona marcas m6A é a METTL3. Usando sequenciamento m6A de alta capacidade e análise de expressão gênica, os cientistas descobriram que a privação crônica de sono reduziu significativamente a METTL3 na região CA3. Essa queda foi confirmada tanto nos níveis de RNA quanto de proteína. O padrão dos genes afetados sugeriu perturbações no controle do ciclo celular e nas respostas ao estresse, indicando que a perda de sono pode estar empurrando os neurônios para estados indesejáveis.
Da mudança molecular à morte neuronal
Para ver como a redução de METTL3 poderia afetar os neurônios diretamente, os pesquisadores usaram células hipocampais de camundongo cultivadas em placas. Quando empregaram pequenos RNAs interferentes para silenciar METTL3, as células ficaram muito mais vulneráveis a tratamentos danosos com rapamicina, uma droga que estressa neurônios. Essas células com METTL3 reduzida mostraram níveis mais altos de proteínas clássicas de “suicídio celular”, como Bax e caspase-3 clivada, e mais células foram identificadas como apoptóticas por citometria de fluxo. Análises de RNA mais profundas apontaram para um único gene, CDKN1A (que codifica a proteína p21), como jogador-chave: quando METTL3 foi reduzida, os níveis de CDKN1A aumentaram acentuadamente.
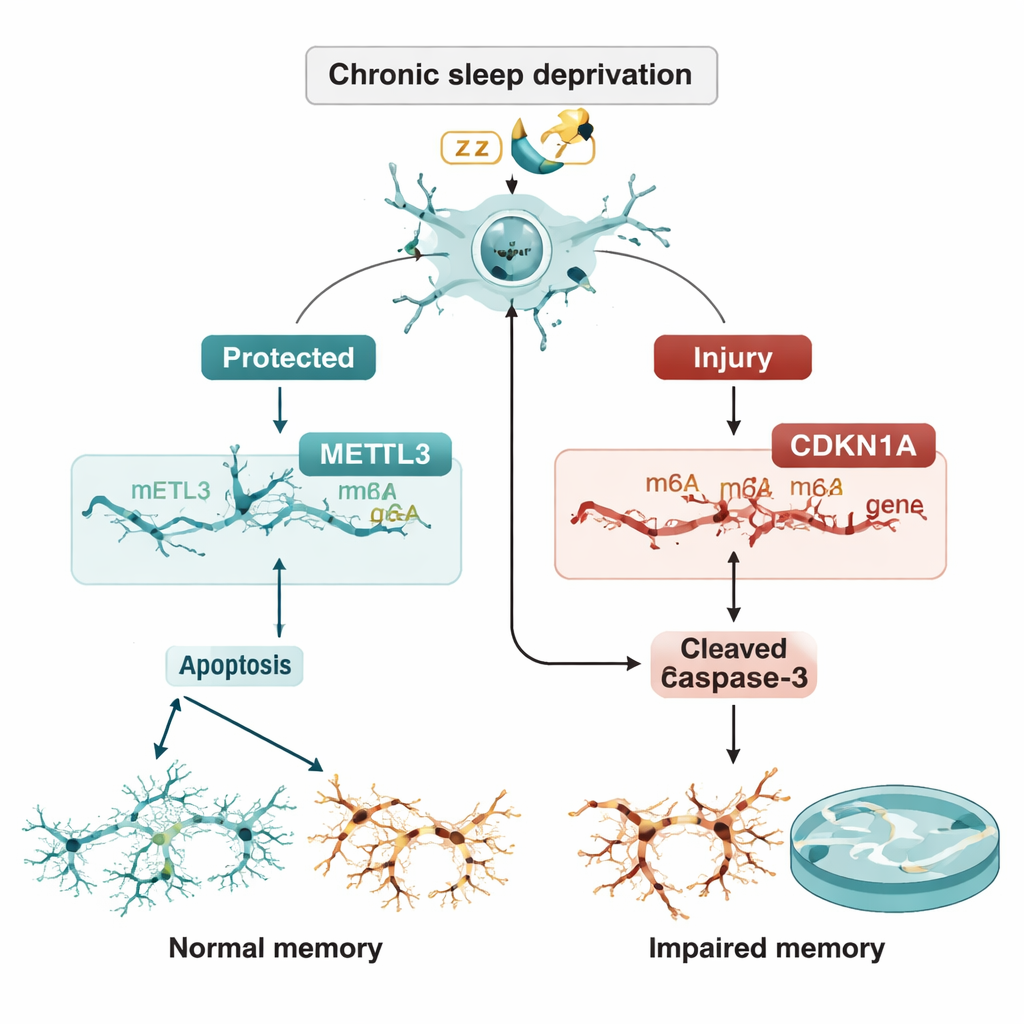
Um equilíbrio frágil entre proteção e autodestruição
A equipe então investigou se METTL3 controla CDKN1A por meio da marcação m6A. Eles demonstraram que reduzir METTL3 diminuía as marcas m6A no RNA de CDKN1A e tornava esse RNA mais estável, de modo que seus níveis se acumulavam em vez de serem degradados. O aumento de CDKN1A, por sua vez, impulsionou os neurônios para a apoptose. Crucialmente, quando o próprio CDKN1A foi silenciado, a morte celular adicional causada pela perda de METTL3 foi em grande parte revertida. Em ratos vivos, a entrega de METTL3 extra diretamente na região CA3 por um vetor viral reduziu os níveis de CDKN1A, diminuiu a abundância de proteínas de apoptose, preservou a estrutura neuronal em colorações teciduais e melhorou o desempenho no labirinto aquático apesar da perda contínua de sono.
O que isso significa para pessoas que não conseguem dormir o suficiente
Em termos simples, a privação crônica de sono parece reduzir uma enzima protetora, METTL3, em um circuito crítico de memória do cérebro. Quando a METTL3 cai, ela não consegue marcar corretamente certos RNAs, especialmente aquele que codifica CDKN1A. Esse RNA então se acumula, levando os neurônios à morte programada e contribuindo para problemas de memória. Ao restaurar a METTL3, os pesquisadores conseguiram reduzir CDKN1A, diminuir a perda neuronal e resgatar a memória em ratos privados de sono. Embora este trabalho ainda esteja na fase animal, ele identifica a via METTL3–CDKN1A como um alvo promissor para futuras drogas destinadas a proteger o cérebro das consequências cognitivas da perda crônica de sono.
Citação: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
Palavras-chave: privação crônica de sono, hipocampo, metilação de RNA, apoptose neuronal, deficiência de memória