Clear Sky Science · pt
Disfunção de interneurônios GABAérgicos subjaz a oscilações de rede neural alteradas associadas à atividade epileptiforme em camundongos deficientes em PPT1
Quando os Ritmos Cerebrais Falham
Crises epilépticas não são apenas tempestades súbitas de atividade cerebral; muitas vezes elas emergem de alterações sutis na comunicação entre neurônios. Este estudo investiga uma doença cerebral infantil rara, a doença CLN1, e coloca uma pergunta simples com implicações amplas: o que acontece aos “marcadores de ritmo” internos do cérebro quando uma única enzima, chamada PPT1, está ausente? Ao acompanhar essas mudanças em camundongos ao longo do tempo, os pesquisadores revelam como pequenas falhas iniciais na inibição podem se transformar em crises e danos cerebrais generalizados.
Os Guardiões do Equilíbrio Cerebral
Nossos cérebros dependem de dois tipos amplos de células nervosas. Células excitatórias, como os neurônios piramidais no hipocampo, impulsionam a atividade. Células inibitórias, chamadas interneurônios, atuam como freios, mantendo essa atividade sob controle e moldando os ritmos elétricos do cérebro. Entre eles, dois grupos importantes são os interneurônios positivos para parvalbumina (PV+) e os positivos para somatostatina (SST+). Eles ajudam a gerar e coordenar ondas rítmicas cerebrais, como as oscilações teta e gama, que suportam funções como aprendizagem e memória. Na doença CLN1, crianças perdem a enzima PPT1, que normalmente remove grupos lipídicos de proteínas. Os autores usaram um modelo murino com a mesma mutação encontrada em pacientes para ver como essa perda afeta os interneurônios e os ritmos cerebrais que eles ajudam a controlar.
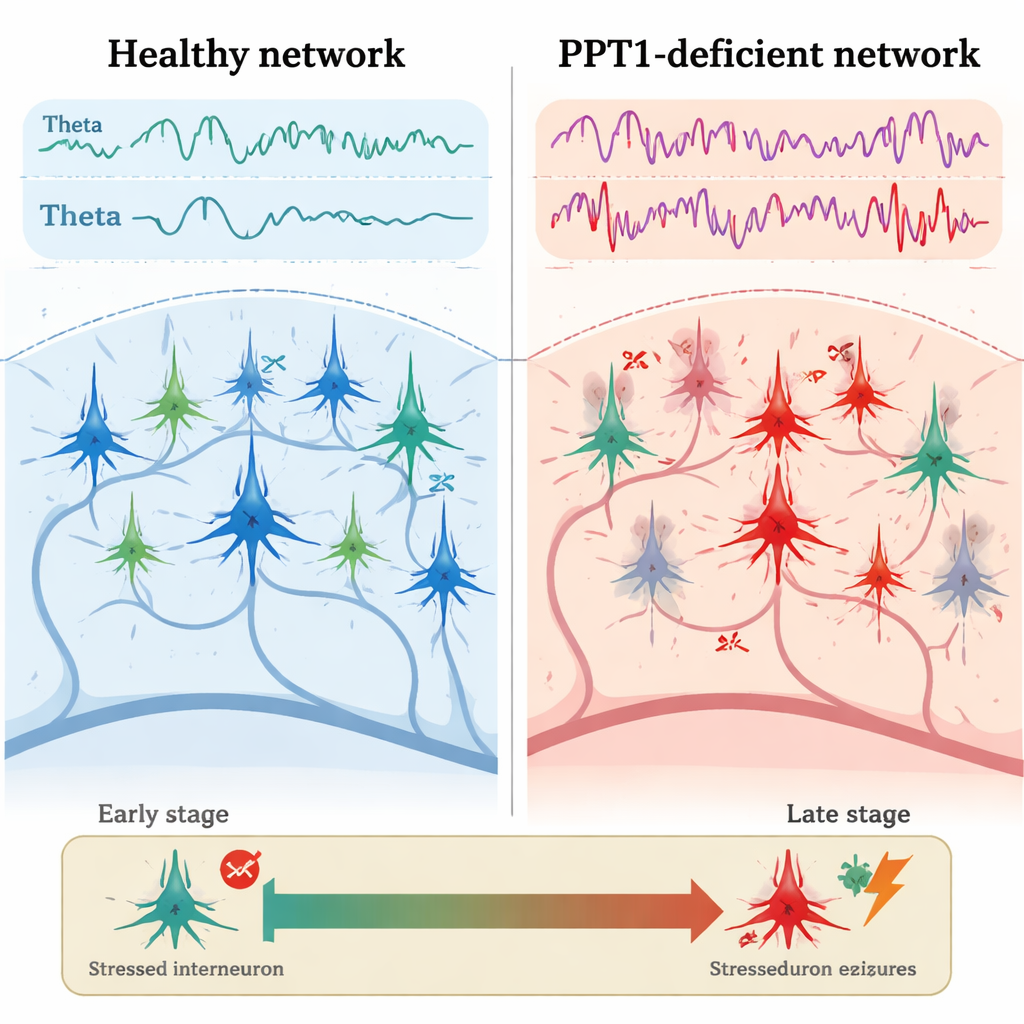
As Primeiras Fissuras no Sistema Inibitório
Em camundongos mutantes jovens-adultos, com cerca de três a quatro meses, o primeiro problema claro apareceu nos interneurônios PV+. Registros elétricos do hipocampo mostraram que essas células inibitórias disparam com menos frequência do que em camundongos saudáveis, enquanto os neurônios piramidais próximos disparam mais rapidamente e com pausas mais curtas entre picos. A microscopia revelou que muitos interneurônios PV+ apresentavam caspase-3 ativada, um executor-chave da morte celular programada, mesmo que seu número total ainda não tivesse diminuído. Ao mesmo tempo, a potência das ondas cerebrais teta e gama estava aumentada, e imagens de cálcio mostraram atividade mais intensa em neurônios do hipocampo enquanto os animais se moviam. Crucialmente, a “conversa” normal entre ritmos teta e gama — em que ondas mais lentas ajudam a organizar as mais rápidas — foi enfraquecida, sugerindo um colapso inicial no timing fino da atividade de rede.
De Ritmos Perturbados a Surtos Epilépticos
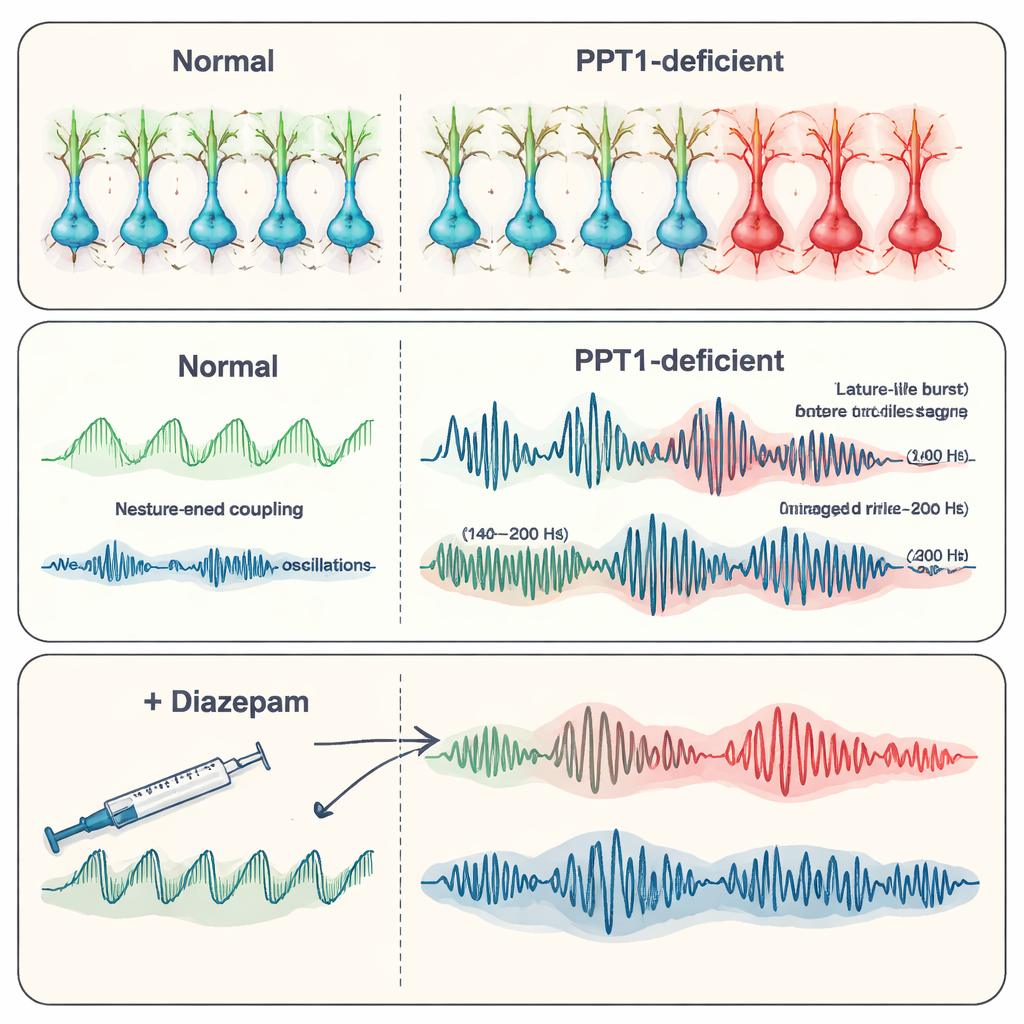
Aos seis a sete meses de idade, o quadro piorou. Muitos interneurônios PV+ foram perdidos, e agora os interneurônios SST+ também mostravam sinais de ativação de caspase-3. Registros do hipocampo revelaram descargas epileptiformes espontâneas — breves rajadas anormais de atividade associadas a convulsões. A equipe concentrou-se em “ripples” de alta frequência, oscilações rápidas que normalmente ajudam a consolidar memórias. Nos camundongos mutantes, os ripples fisiológicos (por volta de 140–200 hertz) tornaram-se menos frequentes, porém de maior amplitude, enquanto ripples ainda mais rápidos e patológicos (200–500 hertz), fortemente ligados à epilepsia, ficaram mais fortes e mais comuns. Juntas, essas mudanças sugerem uma transição de ritmos organizados relacionados à memória para padrões caóticos e propensos a crises, à medida que o controle inibitório falha.
Os Neurônios Se Esgotam e o Diazepam Entra em Cena
À medida que a doença avançou, o próprio hipocampo começou a degenerar. Sinais de cálcio em neurônios declinaram, colorações de Golgi mostraram árvores dendríticas mais finas e menos ramificadas, e houve menos espinhas sinápticas, onde as sinapses se formam. Contagens de neurônios em regiões chave do hipocampo (CA1 e CA3) confirmaram perda celular generalizada, e menos unidades ativas puderam ser detectadas nos registros elétricos. Os pesquisadores então testaram diazepam, um anticonvulsivante comum que potencializa a ação do químico inibitório GABA. Em camundongos mutantes mais velhos, o diazepam reduziu a frequência de descargas epilépticas e restaurou parcialmente padrões oscilatórios mais próximos do normal, inclusive o comportamento dos ripples, embora não reparasse a perda subjacente de receptores. Isso sugere que fortalecer os sinais inibitórios remanescentes ainda pode acalmar a rede, ao menos temporariamente.
Por Que Essas Descobertas Importam
Para o leitor leigo, a mensagem chave é que a doença CLN1 não se resume ao acúmulo de resíduos nas células cerebrais. A perda de PPT1 desencadeia uma reação em cadeia: primeiro, interneurônios inibitórios especializados ficam estressados e começam a falhar, o que libera neurônios piramidais hiperativos e distorce os ritmos cerebrais. Com o tempo, esse desequilíbrio leva a crises epilépticas e, eventualmente, à perda em grande escala de células e conexões cerebrais. O estudo aponta para uma janela de oportunidade precoce na doença, quando proteger ou resgatar interneurônios PV+ — talvez bloqueando a ativação de caspases — poderia prevenir crises e degeneração posteriores. Embora o diazepam não cure a CLN1, sua capacidade de atenuar ritmos anormais neste modelo destaca a ideia mais ampla de que restaurar a inibição pode ser uma estratégia poderosa na epilepsia e em transtornos cerebrais relacionados.
Citação: Tong, J., Liu, W., Wang, Q. et al. Dysfunction of GABAergic interneurons underlies altered neural network oscillations associated with epileptiform activity in PPT1-deficient mice. Transl Psychiatry 16, 106 (2026). https://doi.org/10.1038/s41398-026-03843-8
Palavras-chave: epilepsia, interneurônios, hipocampo, oscilações cerebrais, doença de depósito lisossomal