Clear Sky Science · pt
Alterações funcionais precoces e GFAP plasmático em famílias suecas com mutações de Alzheimer autossômico-dominante
Por que este estudo importa para famílias
A doença de Alzheimer muitas vezes parece surgir de repente, mas na realidade mudanças nocivas no cérebro se acumulam silenciosamente por muitos anos. Em famílias raras que carregam mutações herdadas ("autossômicas dominantes") da doença de Alzheimer, os cientistas podem estimar quando os sintomas provavelmente começarão e observar esses primeiros sinais se desenrolarem. Este estudo acompanhou famílias suecas com tais mutações para entender como o uso de energia do cérebro, as habilidades cognitivas e um marcador sanguíneo de células de suporte cerebral (GFAP) mudam muito antes de surgirem problemas de memória — e como essas mudanças diferem entre genes.
Acompanhando o relógio da doença em famílias de alto risco
Porque pessoas com Alzheimer autossômico dominante (ADAD) tipicamente desenvolvem sintomas em uma idade relativamente previsível, os pesquisadores podem calcular os "anos estimados para o início dos sintomas" (EYO) — quantos anos alguém está antes ou depois dos primeiros sinais esperados da doença. A equipe estudou 45 adultos de famílias suecas com mutações nos genes APP ou PSEN1, bem como parentes sem mutações. Ao longo de mais de sete anos em média, os participantes foram submetidos a exames cerebrais que medem quanto açúcar o cérebro usa (FDG PET), testes detalhados de memória e cognição e, para um subconjunto, exames de sangue para GFAP, uma proteína liberada quando células de suporte cerebral chamadas astrócitos se tornam reativas. Esse desenho permitiu aos cientistas alinhar diferentes mudanças biológicas ao longo de uma linha do tempo compartilhada da doença, em vez de apenas comparar pessoas em um único momento.
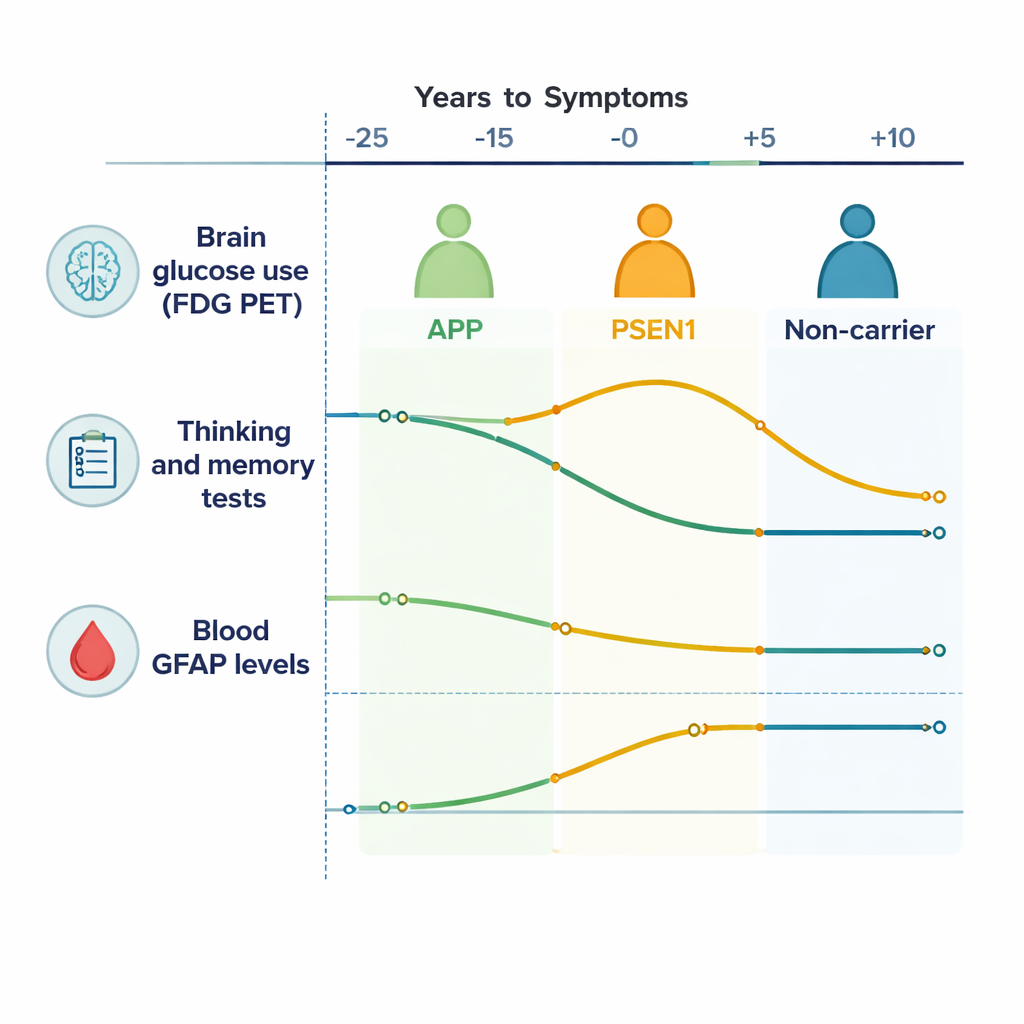
Monitorando energia cerebral e cognição ao longo do tempo
Na superfície externa do cérebro (o córtex), pessoas com mutações de Alzheimer mostraram uma queda gradual no sinal de FDG PET em comparação com familiares sem mutações, indicando que seus cérebros usavam menos glicose ao longo do tempo — um sinal de falência de células cerebrais. Regiões subcorticais mais internas, especialmente o caudado e o tálamo, também apresentaram atividade em declínio, impulsionada principalmente pelos portadores de mutação APP. Testes de pensamento e memória pioraram em vários domínios, incluindo memória episódica e flexibilidade mental, começando aproximadamente 10–15 anos antes do início esperado dos sintomas. Em outras palavras, mesmo enquanto as pessoas ainda se sentiam e funcionavam normalmente no dia a dia, testes sensíveis e exames revelaram que seus cérebros já estavam trabalhando de forma menos eficiente.
Padrões distintos para diferentes genes do Alzheimer
Um insight chave foi que os dois grupos principais de mutação — APP e PSEN1 — não seguiram trajetórias idênticas. Em portadores de PSEN1, os pesquisadores observaram um período inicial, cerca de 20 a 10 anos antes dos sintomas esperados, quando partes do cérebro mostraram uso de glicose incomumente alto ("hipermetabolismo"), junto com desempenho superior nos testes, antes de cair mais tarde. Isso provavelmente reflete uma fase temporária de compensação, na qual o cérebro e suas células de suporte aumentam a atividade para lidar com o dano crescente. Portadores de APP, por outro lado, mostraram uma queda mais direta e gradual no metabolismo cerebral sem esse pico inicial. Esses padrões específicos por gene sugerem que a "doença de Alzheimer" não é uma única história biológica, mesmo nas formas herdadas, mas uma família de processos relacionados que se desenrolam de maneiras diferentes dependendo da mutação subjacente.
O que um exame de sangue revela sobre o estresse cerebral precoce
O GFAP, medido a partir de uma simples amostra de sangue, forneceu uma janela sobre como os astrócitos respondem às mudanças precoces do Alzheimer. Os níveis de GFAP tenderam a subir de forma contínua à medida que as pessoas se aproximavam da idade esperada para o início dos sintomas, tanto em portadores quanto em não portadores de mutação, mas as relações entre GFAP, metabolismo cerebral e cognição foram específicas por gene. Em portadores de APP, níveis mais altos de GFAP estavam ligados à queda no uso de glicose em regiões profundas do cérebro e ao pior desempenho na maioria dos testes cognitivos, sugerindo que a ativação dos astrócitos está intimamente associada ao dano precoce e à perda de função. Em portadores de PSEN1, essas ligações foram mais fracas ou ausentes, apontando novamente para rotas biológicas diferentes rumo ao mesmo desfecho clínico de demência.
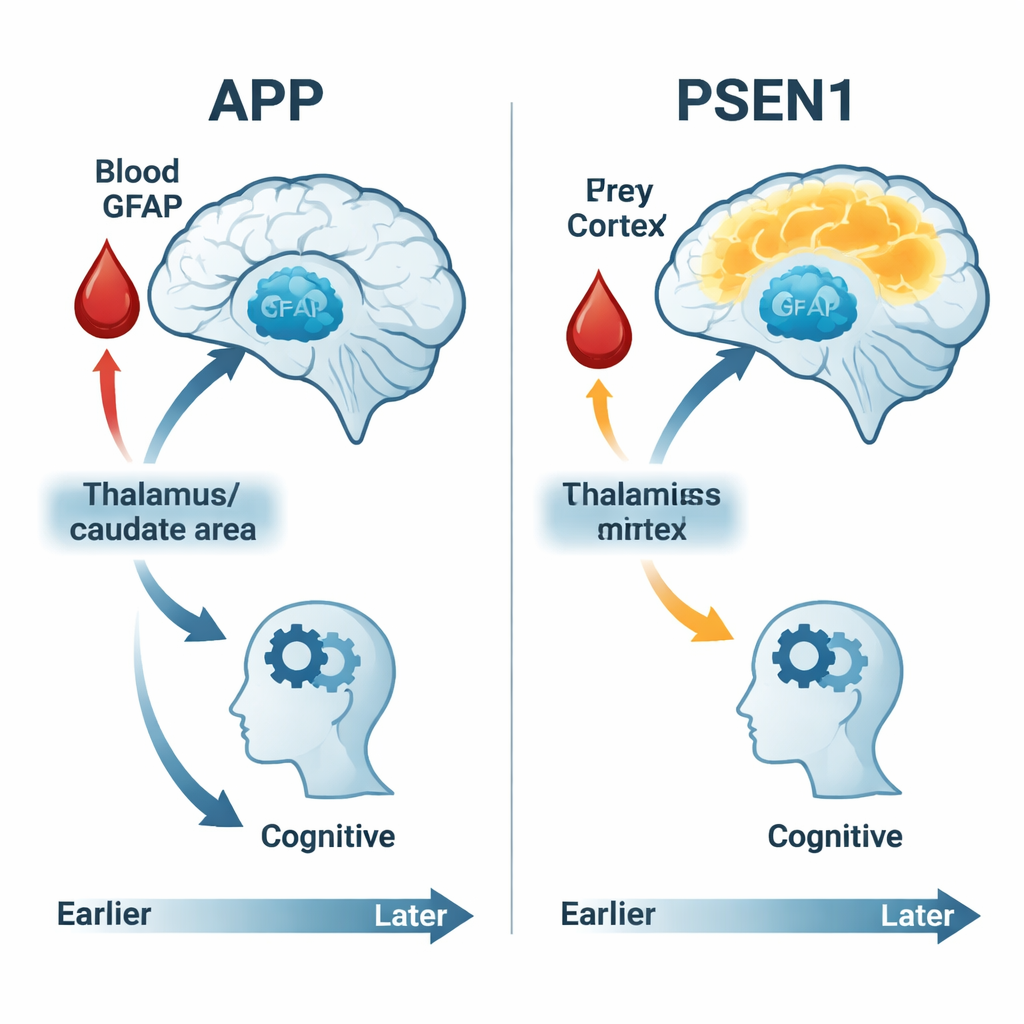
O que isso significa para detecção e tratamento precoces
Para um leitor leigo, a mensagem principal é que, nessas famílias de alto risco, mudanças relacionadas ao Alzheimer começam décadas antes da perda de memória óbvia — e elas não se parecem iguais para todos. Exames de imagem do uso de glicose cerebral, testes cognitivos detalhados e um único marcador sanguíneo como o GFAP podem, em conjunto, revelar quando o cérebro começa a ter dificuldade e com que rapidez essa dificuldade progride. Importante, pessoas com formas genéticas diferentes de Alzheimer mostram sequências distintas de mudança: algumas têm uma fase inicial de hiperatividade, outras exibem um declínio contínuo, e o marcador sanguíneo de estresse dos astrócitos se associa mais fortemente ao dano em alguns grupos do que em outros. Reconhecer essas trilhas distintas pode ajudar a adaptar futuros medicamentos e ensaios às pessoas certas no momento certo, e sustenta a promessa de exames de sangue como o GFAP para detectar a doença de Alzheimer mais cedo — antes que os sintomas roubem a independência das pessoas.
Citação: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
Palavras-chave: doença de Alzheimer autossômica dominante, biomarcador sanguíneo GFAP, metabolismo de glicose cerebral, astrócitos e neurodegeneração, detecção precoce do Alzheimer