Clear Sky Science · pt
Convergência e divergência de genes informadas por variantes comuns e raras do transtorno do espectro autista em vias e redes gênicas específicas de tecido
Por que o quebra‑cabeça genético do autismo importa
Famílias e clínicos sabem há muito tempo que o transtorno do espectro autista (TEA) é altamente variável: algumas pessoas precisam de suporte vitalício, enquanto outras vivem de forma independente, mas têm dificuldades sociais. Grande parte dessa diversidade é atribuída à genética, porém o risco está distribuído por milhares de alterações no DNA, cada uma influenciando cérebro e corpo de maneiras sutis. Este estudo faz uma pergunta simples, porém importante: como mutações raras e potentes e as muitas variantes comuns e fracas trabalham em conjunto em diferentes tecidos para moldar o autismo — e o que isso significa para entender e tratar a condição?
Dois tipos de pistas genéticas
Pesquisadores distinguem variantes raras, que podem perturbar fortemente um gene mas são encontradas em relativamente poucas pessoas, das variantes comuns, que são frequentes na população, porém costumam ter efeitos pequenos. Variantes raras têm sido mais fáceis de associar ao autismo em famílias individuais, embora expliquem apenas uma pequena fração do risco genético total. Variantes comuns, consideradas em conjunto, respondem por grande parte do componente herdável do autismo, mas o impacto de cada uma é minúsculo e fácil de passar despercebido. Os autores deste trabalho propuseram integrar sinais de variantes raras e comuns, perguntando se eles convergem para os mesmos sistemas biológicos ou apontam para diferentes partes do corpo e mecanismos de doença distintos.
Mapeando sinais do DNA em tecidos e redes
Para enfrentar essa questão, a equipe usou uma estrutura analítica chamada Mergeomics, que combina grandes estudos genéticos com informação sobre como genes são ativados e desativados em tecidos específicos. Partiram de dados de associação do genoma inteiro sobre mais de nove milhões de variantes comuns do DNA, a partir de mais de 18.000 indivíduos com autismo e cerca de 28.000 controles sem autismo. Em seguida, mapearam essas variantes para genes usando dados de referência detalhados sobre atividade gênica em quase 50 tecidos, incluindo várias regiões do cérebro, bem como órgãos periféricos digestivos, imunes, reprodutivos e outros. Agrupando genes que são ativados conjuntamente num mesmo tecido e examinando o quão fortemente esses grupos se alinham com variantes associadas ao autismo, os pesquisadores identificaram “módulos” específicos de tecido e redes regulatórias que parecem ser importantes para o TEA.
Cérebro e corpo contribuem
A análise confirmou um papel central do cérebro — especialmente regiões como córtex cingulado anterior, amígdala, córtex frontal, cerebelo e áreas corticais mais amplas, conhecidas por participarem de emoção, comportamento social, cognição e coordenação. Redes gênicas nessas regiões cerebrais foram ricas tanto em variantes comuns quanto raras relacionadas ao autismo e estiveram ligadas à sinalização sináptica, neurodesenvolvimento e ao controle imune dentro do cérebro. Ainda assim, o quadro não parou no crânio. Surpreendentemente, muitos tecidos periféricos, especialmente do sistema digestivo, imune, endócrino e reprodutor, também continham módulos gênicos fortemente informados por variantes comuns associadas ao autismo. Esses módulos foram associados a processos como respostas imunes, crescimento e divisão celular, produção de energia, splicing de mRNA e uma importante via de controle conhecida como mTOR, todos implicados no desenvolvimento cerebral e no comportamento.
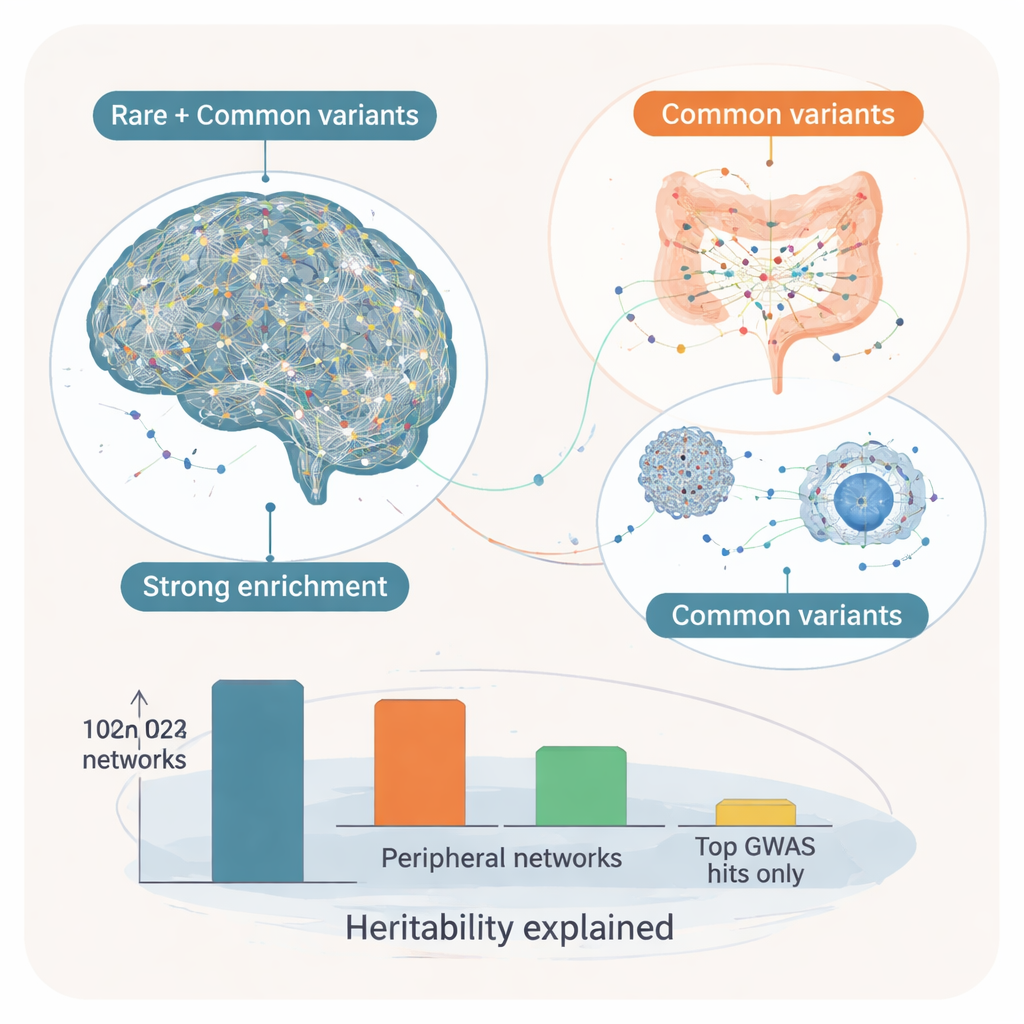
Genes de controle chave e a ideia núcleo–modificador
Ao inserir esses módulos em redes regulatórias gênicas direcionais, os pesquisadores perguntaram então quais genes ocupam os hubs — os chamados “motoristas chave” que influenciam muitos outros genes. Nas redes cerebrais, esses drivers chave mostraram forte enriquecimento por variantes raras de alto impacto no autismo, bem como por variantes comuns, sugerindo que formam um conjunto “núcleo” de genes onde ambos os tipos de risco convergem. Exemplos incluem SYT1, que ajuda a controlar a liberação de neurotransmissores nas sinapses, e ADD2, envolvido na modelagem da estrutura e conectividade neuronal. As redes ao redor desses genes incluem uma mistura de genes raros já associados ao autismo e alvos de variantes comuns envolvidos na comunicação sináptica e excitabilidade neuronal. Em contraste, os drivers chave em tecidos periféricos, especialmente órgãos digestivos e endócrinos, foram mais fortemente influenciados apenas por variantes comuns. Eles parecem atuar como “modificadores”, ajustando vias imunes, metabólicas e de sinalização que podem moldar como vulnerabilidades centrais do cérebro se manifestam em sintomas.
O que isso significa para pessoas e tratamentos futuros
Quando os autores estimaram quanto do risco herdável do autismo poderia ser atribuído a essas redes, os módulos cerebrais explicaram cerca de 7% do componente hereditário e os módulos periféricos mais 3%, juntos capturando quase toda a herdabilidade atribuível a variantes comuns observada no estudo original — e muito mais do que a pequena fração explicada apenas pelos poucos eventos individuais de maior efeito. Para não especialistas, a conclusão é que a genética do autismo segue um padrão em camadas: variantes raras e comuns convergem para um conjunto central de redes centradas no cérebro que são cruciais para o neurodesenvolvimento, enquanto variantes comuns amplas em tecidos intestinais, imunes e hormonais provavelmente modificam o curso e as características da condição. Esse quadro núcleo–modificador ajuda a explicar por que o autismo se apresenta de forma tão distinta entre as pessoas e sugere que terapias futuras podem precisar abordar não apenas o cérebro, mas também os sistemas corporais mais amplos que interagem com ele.
Citação: Gill, C., Zuo, Y., Ha, D.Sm. et al. Convergence and divergence of genes informed by common and rare variants of autism spectrum disorders in tissue-specific pathways and gene networks. Transl Psychiatry 16, 98 (2026). https://doi.org/10.1038/s41398-026-03824-x
Palavras-chave: genética do autismo, variantes raras, variantes comuns, redes cerebrais, eixo intestino–cérebro