Clear Sky Science · pt
Preditores computacionais de variantes para farmacogenômica: da avaliação de alelos isolados à análise de reações adversas a antidepressivos
Por que seus genes importam para a segurança dos antidepressivos
Quando duas pessoas tomam o mesmo antidepressivo, uma pode melhorar com poucos efeitos colaterais enquanto outra enfrenta problemas sérios, incluindo toxicidade medicamentosa. Este estudo investiga se programas de computador conseguem ler pequenas diferenças no nosso DNA para prever quem provavelmente processará antidepressivos com segurança e quem pode ter maior risco de reações nocivas, potencialmente tornando a prescrição do dia a dia mais segura e precisa.

De rótulos rígidos a escores genéticos flexíveis
Hoje, muitas clínicas dependem de um sistema chamado “alelos estrela”, que agrupa variantes de DNA conhecidas em genes que processam medicamentos em algumas categorias amplas de função, como atividade normal ou reduzida. Essa abordagem tem orientado tratamentos, mas falha quando uma pessoa carrega variantes raras ou nunca antes vistas, ou combinações complexas de alterações que não estão nas listas oficiais. Os autores argumentam que isso é um ponto cego importante: a maioria das variantes farmacogenéticas é rara, e uma parcela considerável da variação em como as pessoas metabolizam medicamentos permanece sem explicação pelos rótulos atuais.
Testando ferramentas mais inteligentes em variantes conhecidas e novas
A equipe avaliou dez ferramentas computacionais que pontuam quão danosa uma mudança no DNA provavelmente é, incluindo dois novos modelos que desenvolveram (PharmGScore e PharmMLScore). Primeiro, verificaram se essas ferramentas conseguiam reproduzir as categorias funcionais já atribuídas a 541 alelos estrela curados em oito genes-chave de processamento de medicamentos. Ao somar as pontuações de todas as variantes dentro de cada haplótipo, várias ferramentas igualaram ou até superaram o desempenho do sistema estrela, com o PharmGScore liderando. Em seguida, desafiaram as ferramentas com dados de experimentos de laboratório de alta vazão em duas enzimas importantes, CYP2C9 e CYP2C19, que metabolizam muitos fármacos. Esses experimentos mediram como milhares de variantes individuais afetavam a atividade enzimática e os níveis de proteína, a maioria nunca observada em pacientes. Novamente, as melhores ferramentas, especialmente os conjuntos focados em farmacogenes e o CADD, identificaram com precisão variantes que prejudicavam severamente a função enzimática.
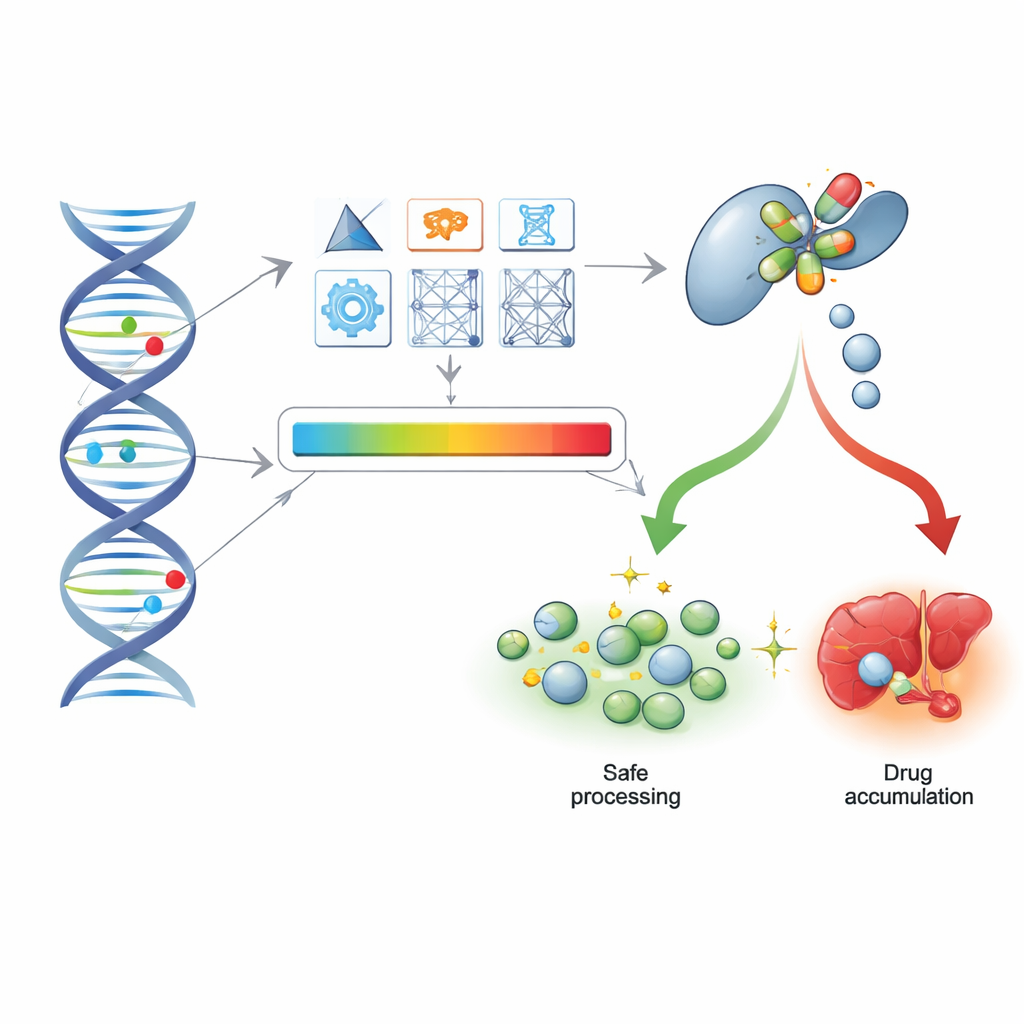
Das sequências de DNA aos registros clínicos do mundo real
Para ver se essas pontuações computacionais se mantêm na medicina cotidiana, os pesquisadores recorreram a dados de sequenciamento do exoma de mais de 200.000 participantes do UK Biobank, junto com seus históricos de prescrições e registros hospitalares. Compararam as previsões das ferramentas com as chamadas de alelos estrela para cinco genes principais de processamento de medicamentos e descobriram que os métodos com melhores pontuações basicamente recapturaram os mesmos agrupamentos funcionais, apesar de os dados de exoma não capturarem algumas alterações não codificantes e estruturais. Importante, a abordagem aditiva — somar o impacto de todas as variantes em um gene — funcionou bem o suficiente para separar pessoas com genótipos sem função daquelas com atividade normal.
Identificando pessoas em risco de reações graves a antidepressivos
Os autores então focaram no uso e na segurança de antidepressivos, concentrando-se na enzima CYP2C19, que ajuda a metabolizar vários medicamentos comuns para depressão. Entre mais de 75.000 usuários de antidepressivos, examinaram dois desfechos: trocas frequentes de medicação, como um indicador aproximado de resposta ruim, e registros hospitalares ou de óbito indicando intoxicação por antidepressivos. Enquanto nem os alelos estrela nem a maioria das pontuações mostraram um sinal forte ou claro para troca de tratamento, revelaram um padrão significativo para reações adversas graves. Portadores de variantes danosas em CYP2C19 apresentaram cerca de 20–35% mais chance de códigos de intoxicação por antidepressivos em seus registros, seja classificados por alelos estrela ou por ferramentas computacionais de melhor desempenho, como PharmGScore, PharmMLScore e CADD. Essa relação permaneceu semelhante mesmo quando as análises foram restritas a casos sem histórico documentado de autoagressão.
O que isso pode significar para prescrições futuras
No geral, o estudo mostra que preditores computacionais bem desenhados podem alcançar o mesmo nível de precisão do sistema tradicional de alelos estrela, ao mesmo tempo em que superam sua maior fraqueza: a incapacidade de lidar com variantes genéticas novas, raras ou complexas. Ao traduzir sequências brutas de DNA em escores de risco contínuos que funcionam em todo o genoma, essas ferramentas poderiam eventualmente permitir que clínicos enxergassem além de uma lista curta de genótipos conhecidos e antecipassem melhor quem tem maior risco de efeitos colaterais graves por antidepressivos. Antes de serem usados na prática rotineira, serão necessárias mais validações e integração com outros fatores clínicos, mas este trabalho estabelece uma base sólida para prescrições mais seguras e personalizadas com base em informações genéticas abrangentes.
Citação: Hajto, J., Piechota, M., Krätschmer, I. et al. Computational variant predictors for pharmacogenomics: from evaluation of single alleles to assessment of adverse drug reactions to antidepressants. Pharmacogenomics J 26, 8 (2026). https://doi.org/10.1038/s41397-026-00399-0
Palavras-chave: farmacogenômica, antidepressivos, variantes genéticas, reações adversas a medicamentos, predição computacional