Clear Sky Science · pt
A desdiferenciação de células de Schwann dirigida por prostaglandina E2 leva à invasão perineural no adenocarcinoma ductal pancreático
Quando o câncer se arrasta ao longo dos nervos
O câncer de pâncreas é notoriamente letal, em parte porque ele não cresce apenas como um nódulo — muitas vezes se espalha rastejando ao longo de nervos próximos, um processo chamado invasão perineural. Essa via oculta está associada à dor, à disseminação precoce e a pior sobrevida, mas os médicos ainda carecem de boas ferramentas para prevê‑la ou bloqueá‑la. O estudo resumido aqui revela como tumores pancreáticos “reprogramam” quimicamente as células de suporte ao redor dos nervos, transformando‑as em cúmplices ativas que ajudam as células cancerosas a invadir. Compreender essa parceria nervo–tumor pode abrir novas maneiras de aliviar a dor e frear a progressão da doença.
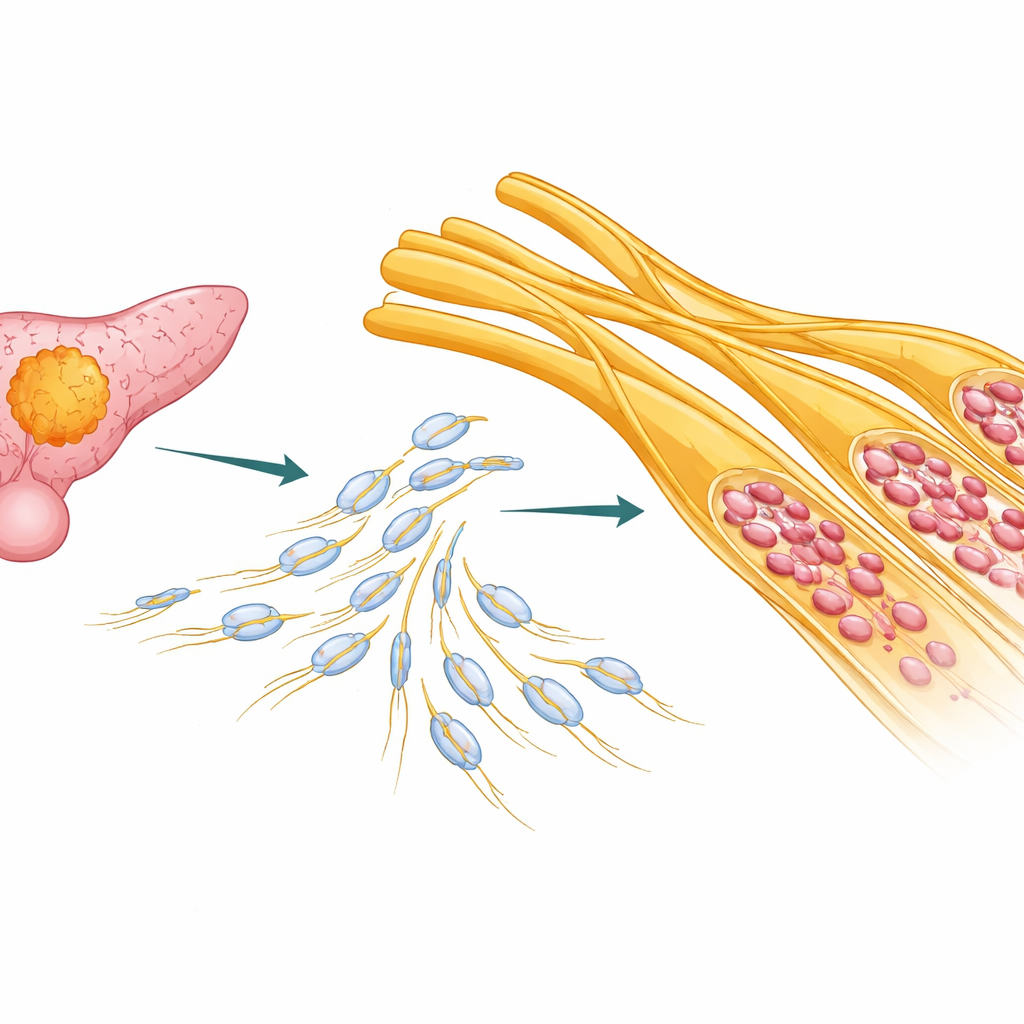
Rodovias escondidas dentro do pâncreas
Em muitos pacientes com adenocarcinoma ductal pancreático, as células tumorais não se limitam a invadir o tecido vizinho; elas envolvendo e viajam ao longo dos nervos. Os autores analisaram amostras de tumor e bases de dados públicas de câncer de mais de cem pacientes. Eles descobriram que pacientes com invasão nervosa mais severa tendiam a ter desfechos piores, especialmente em subtipos moleculares menos agressivos do câncer pancreático. Isso sugere que a invasão perineural não é apenas um efeito colateral, mas um motor relevante da progressão da doença que deveria orientar a estratificação de risco e o tratamento dos pacientes.
Células de suporte que mudam de lado
Os nervos do corpo são envolvidos e protegidos por células de Schwann, um tipo de célula de suporte que também ajuda os nervos a se reparar após lesão. No tecido do câncer pancreático, os pesquisadores usaram sequenciamento avançado de RNA, transcriptômica espacial e análise de célula única para mapear onde os diferentes tipos celulares se localizam e quais genes ativam. Eles descobriram que uma forma particular de célula de Schwann — semelhante ao estado de “reparo” observado após lesão nervosa — estava concentrada exatamente nas regiões onde os nervos eram invadidos pelo tumor. Essas células exibiam sinais de desdiferenciação: perderam sua função isolante normal e tornaram‑se alongadas, móveis e altamente ativas, expressando marcadores como p75NTR, SOX2 e c‑Jun.
Um sinal químico do tumor para o nervo
Para descobrir o que empurra as células de Schwann para esse estado pró‑invasão e semelhante ao de reparo, a equipe cultivou células de câncer pancreático junto com células de Schwann em sistemas de cocultura laboratoriais. Eles observaram que as células tumorais aumentavam a mobilidade das células de Schwann, remodelavam sua morfologia e ativavam genes de desdiferenciação. Análises genéticas em múltiplas camadas apontaram para uma enzima tumoral como o principal culpado: PTGES, que produz o mensageiro lipídico prostaglandina E2 (PGE2). PTGES era especialmente abundante em regiões tumorais próximas a nervos invadidos, e os níveis de PGE2 aumentavam quando células cancerosas e de Schwann eram cocultivadas. Quando os pesquisadores bloquearam a PTGES com um inibidor de pequena molécula ou a eliminaram geneticamente, os níveis de PGE2 caíram e as células de Schwann ficaram muito menos propensas a se ativar e migrar.

Como células reprogramadas abrem a porta
Adicionar PGE2 purificada diretamente às células de Schwann as fez adotar as formas alongadas e bipolares típicas do estado de reparo e aumentar marcadores de desdiferenciação. Em culturas tridimensionais, essas células alteradas esticavam‑se em direção a agregados de câncer pancreático e estruturas semelhantes a nervos, efetivamente construindo “trilhos” celulares que guiavam as células tumorais. Observando mais de perto, os cientistas descobriram que as células de Schwann estimuladas por PGE2 secretavam altos níveis de duas proteínas-chave: fator inibitório de leucemia (LIF), que promove crescimento e remodelamento nervoso, e ADAMTS‑1, uma enzima que ajuda a degradar a matriz extracelular circundante. Juntos, esses fatores secretados afinaram as barreiras físicas ao redor dos nervos e incentivaram a brotação de novos nervos, criando caminhos macios e remodelados que as células cancerosas podiam seguir facilmente.
Transformando o mecanismo em ideias de tratamento
Experimentos em animais sustentaram esse quadro: quando células de câncer pancreático haviam sido primeiro “preparadas” por células de Schwann, os tumores cresciam mais e causavam maior dano nervoso e fraqueza nos membros dos camundongos. Tratamentos que bloquearam a PTGES ou neutralizaram o LIF reduziram a carga tumoral, diminuíram a invasão nervosa e melhoraram a função nervosa, ao mesmo tempo em que preservaram a isolação nervosa ao microscópio. O modelo geral que emerge é um circuito parácrino: tumores pancreáticos liberam PGE2, que reprograma células de Schwann para um estado semelhante ao de reparo e propenso à invasão; essas células então secretam LIF e ADAMTS‑1, remodelam nervos e tecido circundante e abrem caminho para a disseminação tumoral ao longo dos nervos. Para os pacientes, esse trabalho sugere que fármacos que atinjam o eixo PTGES–PGE2–célula de Schwann, ou que bloqueiem o LIF, poderão algum dia ajudar a conter a invasão nervosa, aliviar a dor e retardar a progressão do câncer de pâncreas.
Citação: Wang, L., Liu, Q., Zhang, Z. et al. Prostaglandin E2-driven dedifferentiation of Schwann cells leads to perineural invasion in pancreatic ductal adenocarcinoma. Sig Transduct Target Ther 11, 122 (2026). https://doi.org/10.1038/s41392-026-02648-x
Palavras-chave: câncer de pâncreas, invasão perineural, células de Schwann, prostaglandina E2, microambiente tumoral