Clear Sky Science · pt
Sinalização de monofosfato de guanosina cíclico–proteína quinase G atenua a calcificação da valva aórtica por meio da autofagia mediada por ULK1
Por que a “ferrugem” das válvulas cardíacas importa
À medida que as pessoas envelhecem, a valva aórtica — a principal saída do coração — pode gradualmente enrijecer e ficar recoberta por cálcio, uma condição chamada doença da valva aórtica calcificada. Esse “endurecimento” obriga o coração a bombear com mais força e pode levar a dor no peito, desmaios, insuficiência cardíaca ou à necessidade de troca da válvula por cirurgia. Hoje, não existe medicamento que desacelere esse processo de forma confiável; os médicos só podem aguardar até a válvula estar gravemente danificada e então operar. Este estudo explora uma via celular inata que parece proteger a válvula contra a calcificação e testa um fármaco moderno para insuficiência cardíaca como uma possível forma de religar essa proteção.
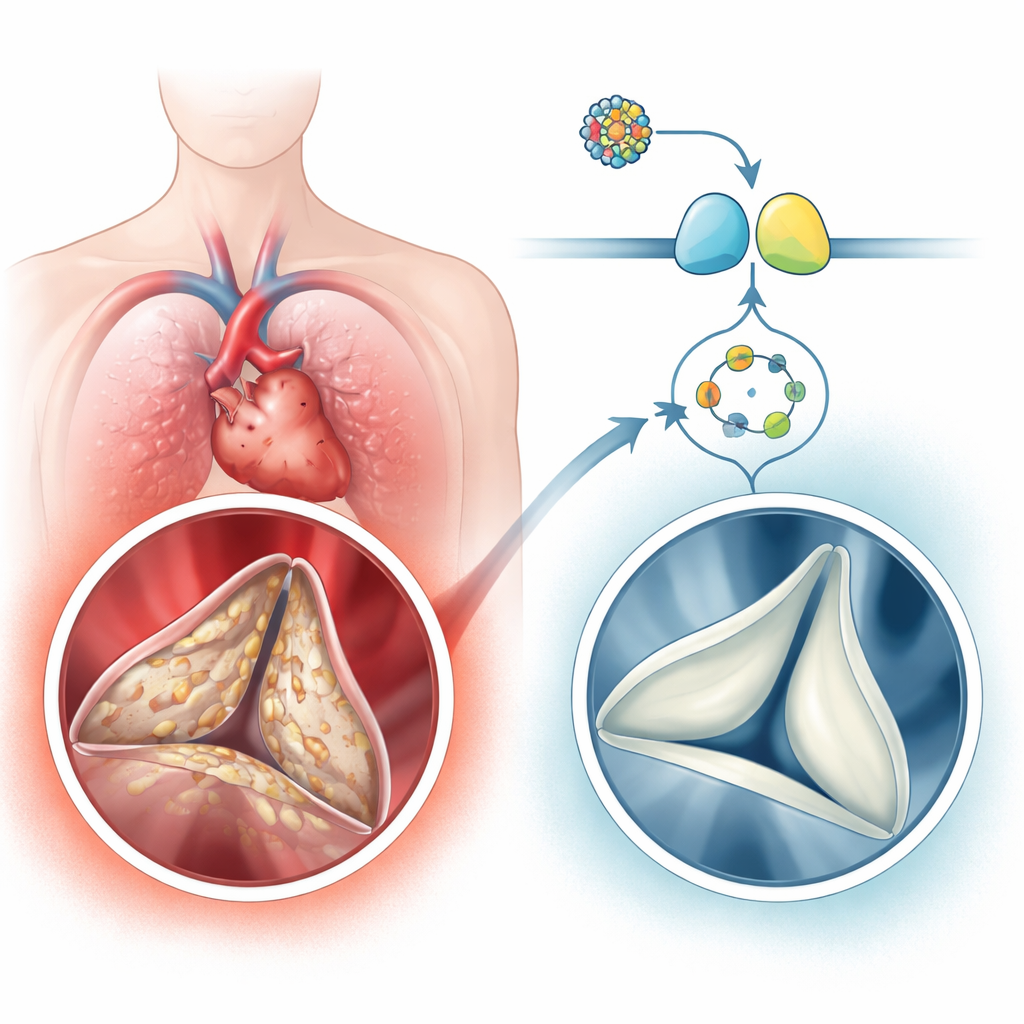
Um problema cardíaco comum, mas negligenciado
A doença da valva aórtica calcificada é surpreendentemente comum em adultos mais velhos, afetando alguns por cento das pessoas com mais de 65 anos e até uma em cada dez pessoas com mais de 75 anos. A doença não é apenas um “desgaste” passivo. Em vez disso, as células do tecido conectivo macio da válvula, conhecidas como células intersticiais valvares, mudam para estados semelhantes à cicatrização e à formação óssea. Elas depositam colágeno extra e, em seguida, cálcio, transformando os folhetos antes flexíveis em lâminas rígidas como pedra. Os autores analisaram tecido valvar humano e grandes conjuntos de dados de expressão gênica e descobriram que uma via de sinalização centrada em uma pequena molécula chamada cGMP e sua enzima parceira proteína quinase G (PKG) estava consistentemente reduzida em válvulas calcificadas, enquanto genes e proteínas ligados à formação óssea estavam aumentados. Pessoas com calcificação valvar severa também apresentavam níveis menores de cGMP no sangue, que se correlacionavam com o grau de estreitamento e obstrução das válvulas.
Um sinal protetor que desaparece
Para investigar causa e efeito, a equipe usou camundongos e células valvares humanas cultivadas. Camundongos geneticamente modificados para produzir menos PKG desenvolveram folhetos valvares mais espessos e mais calcificados após uma lesão controlada da valva aórtica, e suas válvulas mostraram níveis mais altos de uma proteína mestre da formação óssea. Em células valvares humanas cultivadas em placa sob condições que favorecem o acúmulo de cálcio, reduzir a atividade de PKG com ferramentas genéticas acelerou essa mudança para um fenótipo ósseo. Esses resultados sugerem que a sinalização cGMP‑PKG normalmente atua como um freio contra a reprogramação celular prejudicial na válvula — e quando esse freio enfraquece, a calcificação acelera.
Reaproveitando um medicamento para insuficiência cardíaca
Os pesquisadores então perguntaram se reforçar essa via poderia retardar ou reverter a calcificação. Testaram três medicamentos que aumentam o cGMP de maneiras diferentes, incluindo o vericiguat, um fármaco aprovado para certos pacientes com insuficiência cardíaca. Em células valvares humanas, os três medicamentos reduziram depósitos de cálcio e marcadores de mudança para um fenótipo ósseo, com o vericiguat apresentando o efeito mais forte. O vericiguat também diminuiu a calcificação em pequenos fragmentos de tecido valvar humano mantidos vivos fora do corpo. Em dois modelos murinos — um induzido por dieta rica em colesterol e outro por lesão mecânica da valva — o tratamento diário com vericiguat levou a folhetos mais finos, menos calcificados e melhor fluxo sanguíneo através da válvula, sem enfraquecer a força de ejeção do coração. Quando a PKG foi reduzida geneticamente, contudo, o vericiguat perdeu em grande parte seus benefícios, indicando que a PKG é a peça chave a jusante.
Limpeza celular e válvulas mais saudáveis
Ao aprofundar, a equipe descobriu que o vericiguat e a PKG protegiam as mitocôndrias — as pequenas usinas das células valvares. Sob condições calcificantes, as células acumulavam espécies reativas de oxigênio danosas, perdiam potencial de membrana mitocondrial e produziam menos energia. O vericiguat restaurou o desempenho mitocondrial e reduziu o estresse oxidativo. Mapas em larga escala de proteínas e de fosforilação os direcionaram à autofagia — o sistema interno de limpeza e reciclagem celular. Em válvulas humanas calcificadas, imagens microscópicas e marcadores proteicos mostraram redução na formação e atividade de autofagossomos, as “sacolas de lixo” da autofagia. Em análises de célula única, vários subtipos de células valvares de válvulas doentes exibiram ampla supressão de programas relacionados à autofagia. Em células cultivadas, bloquear a autofagia eliminou o efeito protetor da ativação da PKG, sugerindo que a PKG age em grande parte reativando esse sistema de limpeza.
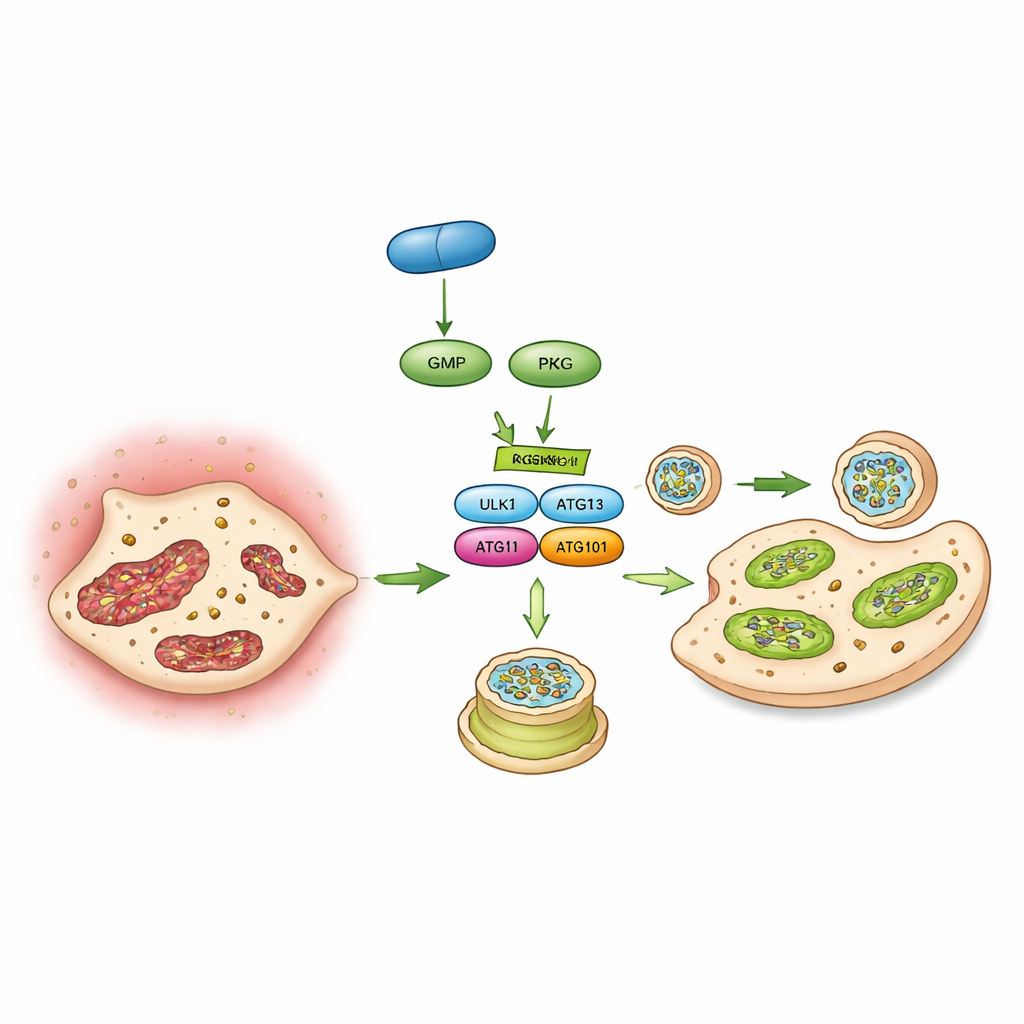
Virando um interruptor molecular
Por fim, os autores identificaram um interruptor molecular específico que liga a PKG à autofagia: uma proteína chamada ULK1, que inicia a formação dos autofagossomos. Usando fosfoproteômica, estudos de interação e ensaios de quinase in vitro, eles demonstraram que a PKG adiciona diretamente um grupo fosfato à ULK1 em um sítio particular (um aminoácido chamado serina 556). Quando esse sítio foi mutado para não poder mais ser modificado, a PKG não conseguiu aumentar a autofagia nem bloquear a calcificação em células valvares. Em camundongos, forçar a expressão desse mutante de ULK1 não responsivo nas células valvares também anulou a capacidade do vericiguat de proteger a válvula. Em conjunto, essas descobertas delineiam uma cadeia de eventos: o vericiguat estimula o cGMP, que ativa a PKG, que aciona o interruptor ULK1, que revive a autofagia, preserva as mitocôndrias e impede que as células valvares se transformem em células formadoras de osso.
O que isso pode significar para os pacientes
Este trabalho posiciona o eixo cGMP–PKG–ULK1–autofagia como um sistema de defesa inato contra a “ferrugem” da valva aórtica. Na doença valvar calcificada, essa defesa é atenuada, permitindo que as células acumulem danos e se desloquem para uma identidade semelhante à óssea. Ao restaurar farmacologicamente o sinal com um fármaco já usado em clínicas de insuficiência cardíaca, os pesquisadores desaceleraram a calcificação em vários modelos experimentais. Embora ensaios clínicos em humanos com doença valvar sejam necessários, o estudo oferece uma ideia clara e testável: reforçar com cautela essa via de limpeza celular pode um dia retardar ou reduzir a necessidade de cirurgia de substituição valvar em adultos mais velhos em risco de estenose aórtica.
Citação: Wang, Y., Xu, F., Song, C. et al. Cyclic guanosine monophosphate-protein kinase G signaling attenuates aortic valve calcification through ULK1-mediated autophagy. Sig Transduct Target Ther 11, 90 (2026). https://doi.org/10.1038/s41392-026-02624-5
Palavras-chave: doença da valva aórtica calcificada, sinalização cGMP PKG, vericiguat, autofagia, calcificação das válvulas cardíacas