Clear Sky Science · pt
Sinalização Fibrinogênio–Bmal1 como alvo terapêutico para limitar a dissecção aórtica preservando a contratilidade das CMLV
Por que o Guardião Oculto da Aorta Importa
A dissecção aórtica é uma das emergências mais assustadoras da medicina: a principal artéria que sai do coração pode rasgar de repente, muitas vezes sem aviso, e muitos pacientes morrem em poucas horas. A cirurgia pode salvar vidas, mas é arriscada e nem sempre é possível de imediato. Este estudo investiga um aliado inesperado já circulando em nosso sangue — o fibrinogênio, uma proteína da coagulação — e mostra que, além de ajudar a estancar sangramentos, ela pode também contribuir para manter a aorta intacta e retardar a progressão da doença, potencialmente dando aos médicos um tempo precioso para agir.
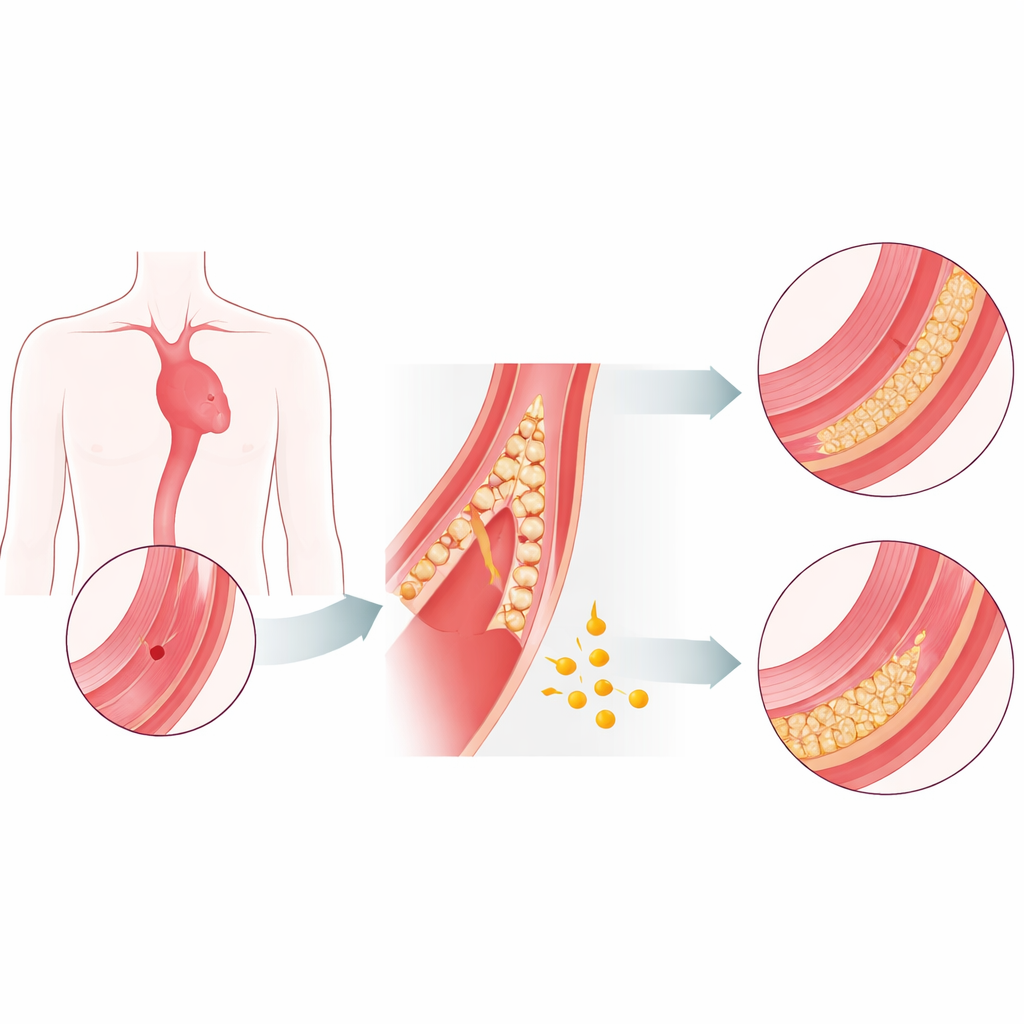
Um Assassino Silencioso que Precisa de Novas Opções
A aorta é construída como uma mangueira resistente e em várias camadas. Quando suas camadas internas enfraquecem e se separam, o sangue pode invadir a parede e descolá‑la — isso é uma dissecção aórtica. Na fase inicial e perigosa, o risco de morte aumenta hora após hora, e a cirurgia de emergência costuma ser a única opção. Pacientes que sobrevivem tempo suficiente para chegar a uma fase mais estável e crônica tendem a ter um prognóstico muito melhor. Hoje não existem medicamentos comprovados que retardem de forma confiável o processo de rasgamento ou que reforcem a parede aórtica. Os autores buscaram descobrir se o fibrinogênio, uma proteína sanguínea comum conhecida principalmente por seu papel na coagulação, também poderia agir como um estabilizador natural da aorta.
Pistas de Pacientes: Mais Fibrinogênio, Melhor Sobrevida
A equipe primeiro examinou 310 pacientes com dissecção aórtica aguda que não puderam ser submetidos à cirurgia e foram tratados apenas com medicamentos. Compararam os que sobreviveram à internação com os que não sobreviveram. Pacientes que morreram tipicamente apresentavam níveis muito mais baixos de fibrinogênio no sangue. Quando os pesquisadores agruparam os pacientes por nível de fibrinogênio, verificaram que níveis muito baixos (abaixo de 2 gramas por litro) estavam associados a taxas de mortalidade muito maiores, enquanto níveis altos (acima de 4 gramas por litro) estavam associados a melhor sobrevida. Esse padrão sugeriu que o fibrinogênio não era apenas um espectador, mas podia realmente ajudar a aorta a resistir a novos rasgamentos.
Observando a Aorta Romper e Cicatrizar em Camundongos
Para ir além da associação e testar causa e efeito, os cientistas usaram modelos de camundongo nos quais a aorta pode ser levada a enfraquecer e se dissecar. Nesses animais, o fibrinogênio normalmente estava ausente da parede aórtica saudável, mas à medida que a doença se desenvolvia, ele começou a infiltrar a camada média onde residem as células musculares lisas. Surpreendentemente, o acúmulo maior de fibrinogênio apareceu em segmentos gravemente danificados, porém ainda não rompidos, sugerindo que sua presença poderia ajudar a evitar que a parede cedesse de vez. Quando os pesquisadores usaram terapia gênica para reduzir a produção de fibrinogênio no fígado, as dissecações pioraram: as aortas dilataram mais, o dano estrutural aumentou e mais camundongos morreram. A reposição com fibrinogênio purificado reverteu esses efeitos. Experimentos independentes usando um modelo diferente de aneurisma aórtico mostraram tendência protetora semelhante, fortalecendo a hipótese de que o fibrinogênio protege ativamente a parede do vaso.
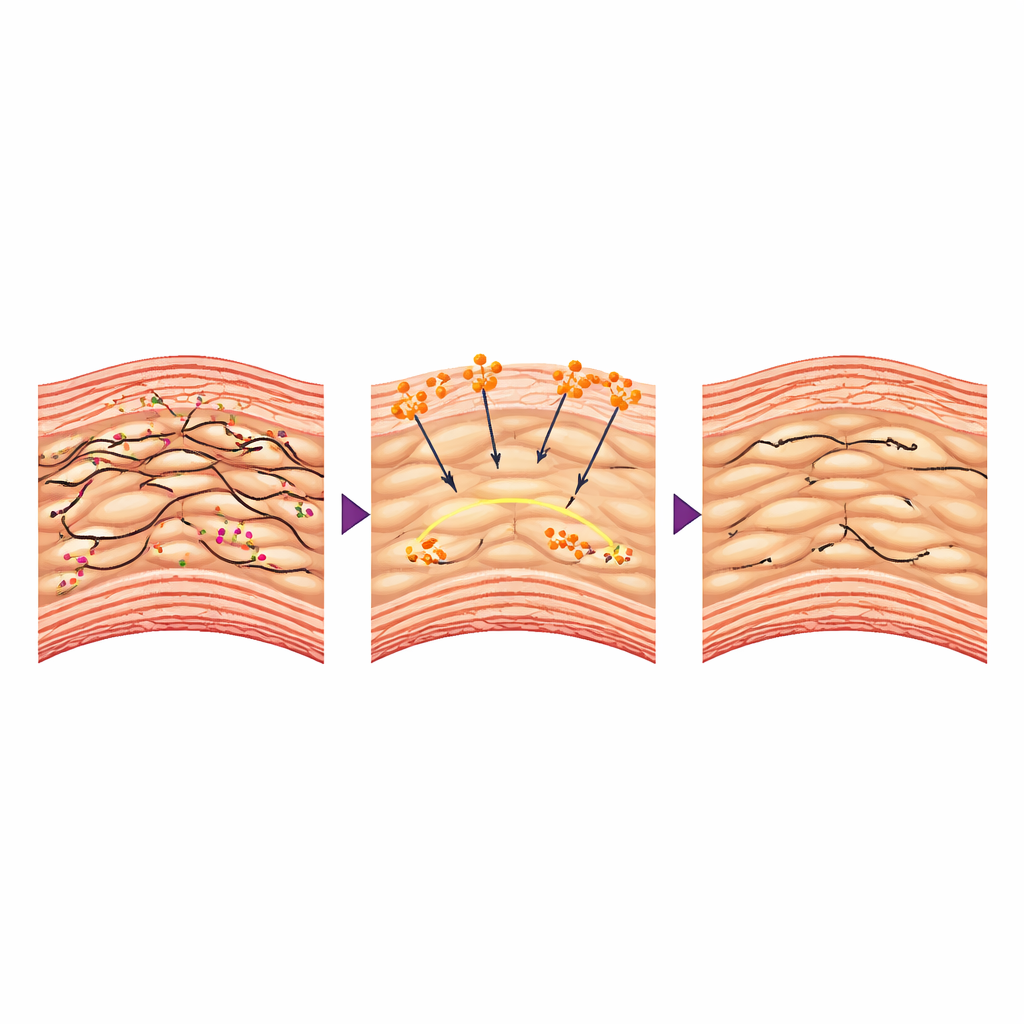
O Diálogo Oculto entre Proteína Sanguínea e Células Musculares
Como uma proteína de coagulação poderia proteger a aorta de dentro? Os autores focalizaram as células musculares lisas vasculares, as células contráteis que formam a camada média da aorta e atuam como seus “anéis de reforço” vivos. Na doença, essas células frequentemente perdem seu estado contrátil e compacto e mudam para uma forma mais frouxa e sintética que degrada o tecido ao redor. O estudo constatou que, quando o fibrinogênio entrava na parede aórtica, ele interagia com receptores específicos nessas células e ajudava a preservar seu arcabouço interno de filamentos de actina. Células musculares lisas de animais tratados estavam mais rígidas, contraíam‑se com mais força em testes e expressavam mais marcadores “contráteis” e menos proteínas que degradam a matriz de suporte. No nível gênico, o fibrinogênio atenuou a atividade de Bmal1, um regulador mestre ligado ao relógio biológico que, neste contexto, promovia mudanças prejudiciais no comportamento das células musculares. Forçar a elevação de Bmal1 apagou os benefícios do fibrinogênio, demonstrando que essa via de sinalização era central para o efeito protetor.
Do Mecanismo ao Potencial Tratamento
Como o fibrinogênio também promove a coagulação, a equipe perguntou se seu benefício se devia simplesmente à formação de coágulos mais fortes. Usando um anticoagulante potente para bloquear a trombina — a enzima que converte fibrinogênio em coágulo sólido — eles mostraram que o fibrinogênio ainda protegia a aorta mesmo quando a formação de coágulos estava largamente desabilitada. Por fim, testaram diferentes doses e descobriram que apenas quantias suficientemente altas de fibrinogênio administrado retardavam a progressão da doença, reduziam rupturas e preservavam a estrutura tecidual. Em conjunto, esses achados retratam o fibrinogênio como uma molécula com dupla função: em níveis mais altos, o fibrinogênio intacto pode penetrar uma parede aórtica enfraquecida, acalmar uma via de sinalização prejudicial nas células musculares lisas e ajudá‑las a permanecer fortes e contráteis. Para os pacientes, isso levanta a possibilidade de que infusões de fibrinogênio cuidadosamente dosadas possam um dia se tornar um tratamento semelhante a medicamento para retardar a dissecção aórtica e estender com segurança a janela para cirurgia planejada e salvadora.
Citação: Zhong, X., Li, D., Zhao, Y. et al. Fibrinogen–Bmal1 signaling as a therapeutic target to limit aortic dissection by preserving VSMC contractility. Sig Transduct Target Ther 11, 103 (2026). https://doi.org/10.1038/s41392-026-02610-x
Palavras-chave: dissecção aórtica, fibrinogênio, células musculares lisas vasculares, sinalização Bmal1, aneurisma aórtico