Clear Sky Science · pt
CircArhgap26 modificado por m6A atenua a lesão por isquemia‒reperfusão cardíaca ao suprimir a palmitoilação da plakofilina‑1
Por que proteger o coração após um infarto é importante
Quando alguém tem um infarto, os médicos agem rapidamente para reabrir a artéria obstruída e restaurar o fluxo sanguíneo. Essa intervenção salva vidas, mas também tem um lado negativo: o retorno súbito do sangue pode causar mais danos ao coração, um problema conhecido como lesão por isquemia–reperfusão. O estudo resumido aqui investiga um defensor natural inesperado dentro das células cardíacas — um pedaço circular de RNA chamado circArhgap26 — que ajuda a proteger o músculo cardíaco dessa onda secundária de dano. Entender como essa pequena molécula atua pode apontar caminhos para novos tratamentos e exames sanguíneos para pessoas com doença cardíaca.
Um círculo oculto no roteiro genético do coração
A maioria de nós pensa em genes como fios retos de DNA e RNA, mas as células também produzem moléculas de RNA em forma de anel, chamadas RNAs circulares, que são incomumente estáveis e podem ajustar finamente muitos processos celulares. Os pesquisadores procuraram em corações de camundongos por RNAs circulares que mudam durante a lesão cardíaca e focaram em um, o circArhgap26, cujos níveis caíram acentuadamente quando o fluxo sanguíneo foi interrompido e depois restabelecido. Eles confirmaram que esse RNA circular forma um loop fechado, é encontrado principalmente no compartimento fluido da célula e não serve como molde para produzir proteína. Em vez disso, parece agir como um regulador, interagindo com outras moléculas para influenciar se uma célula cardíaca sobrevive ou morre após o estresse. 
Prova de que o RNA circular protege o coração
Para ver o que o circArhgap26 realmente faz, a equipe aumentou ou reduziu seus níveis em corações de camundongos. Quando usaram um vírus para elevar o circArhgap26 especificamente nas células do músculo cardíaco, animais submetidos a um bloqueio temporário de uma artéria coronária seguido de restauração do fluxo sanguíneo apresentaram melhor capacidade de bombeamento do coração, áreas danificadas menores e menos células morrendo. Marcadores clássicos de lesão no sangue e no tecido cardíaco também foram mais baixos. O oposto ocorreu quando o RNA circular foi silenciado: mesmo sem um infarto induzido, a função cardíaca piorou e a morte celular aumentou, e esses problemas ficaram mais graves quando a isquemia–reperfusão foi adicionada. Efeitos protetores semelhantes apareceram em células cardíacas humanas em laboratório, sugerindo que o mecanismo é conservado entre camundongos e humanos.
Uma proteína parceira nociva mantida sob controle
Investigando mais a fundo, os pesquisadores perguntaram como o circArhgap26 exerce essa proteção. Usando técnicas bioquímicas de “pesca”, eles descobriram que ele se liga diretamente a uma proteína estrutural chamada plakofilina‑1 (PKP1), que pode influenciar o quão fortemente as células se aderem e quão prontamente elas entram em morte programada. Em corações lesionados e em células cardíacas estressadas, os níveis de PKP1 aumentaram e foram associados a danos mais graves. Silenciar PKP1 aliviou a lesão cardíaca e a morte celular, enquanto forçar sua produção piorou os desfechos. Quando o circArhgap26 foi aumentado, a quantidade de proteína PKP1 caiu mesmo sem mudança na atividade gênica, indicando um ponto de controle após a produção da mensagem de RNA. Experimentos mostraram que o circArhgap26 acelera a degradação da proteína PKP1 ao interferir em um processo de modificação por gorduras chamado palmitoilação, que normalmente estabiliza a PKP1.
Uma disputa molecular pela sinalização da morte celular
A palmitoilação é realizada por uma família de enzimas; uma em particular, ZDHHC1, foi identificada como responsável por anexar grupos gordurosos à PKP1 e torná‑la mais duradoura. O circArhgap26 se liga à PKP1 na mesma região usada pela ZDHHC1, criando uma disputa molecular. Quando o RNA circular vence, a PKP1 recebe menos marcas gordurosas, torna‑se menos estável e é eliminada mais rapidamente. Isso tem um efeito cascata: a PKP1 normalmente estimula a produção de outra proteína, a APAF1, ao interagir com um segmento regulatório do RNA dessa proteína. APAF1 é parte central da maquinaria que ativa as enzimas caspase‑9 e caspase‑3, executoras centrais da morte celular. Com menos PKP1 estável, a produção de proteína APAF1 diminui, a cascata de sinalização da morte é atenuada e as células do coração têm maior probabilidade de sobreviver ao estresse do restabelecimento do fluxo sanguíneo. 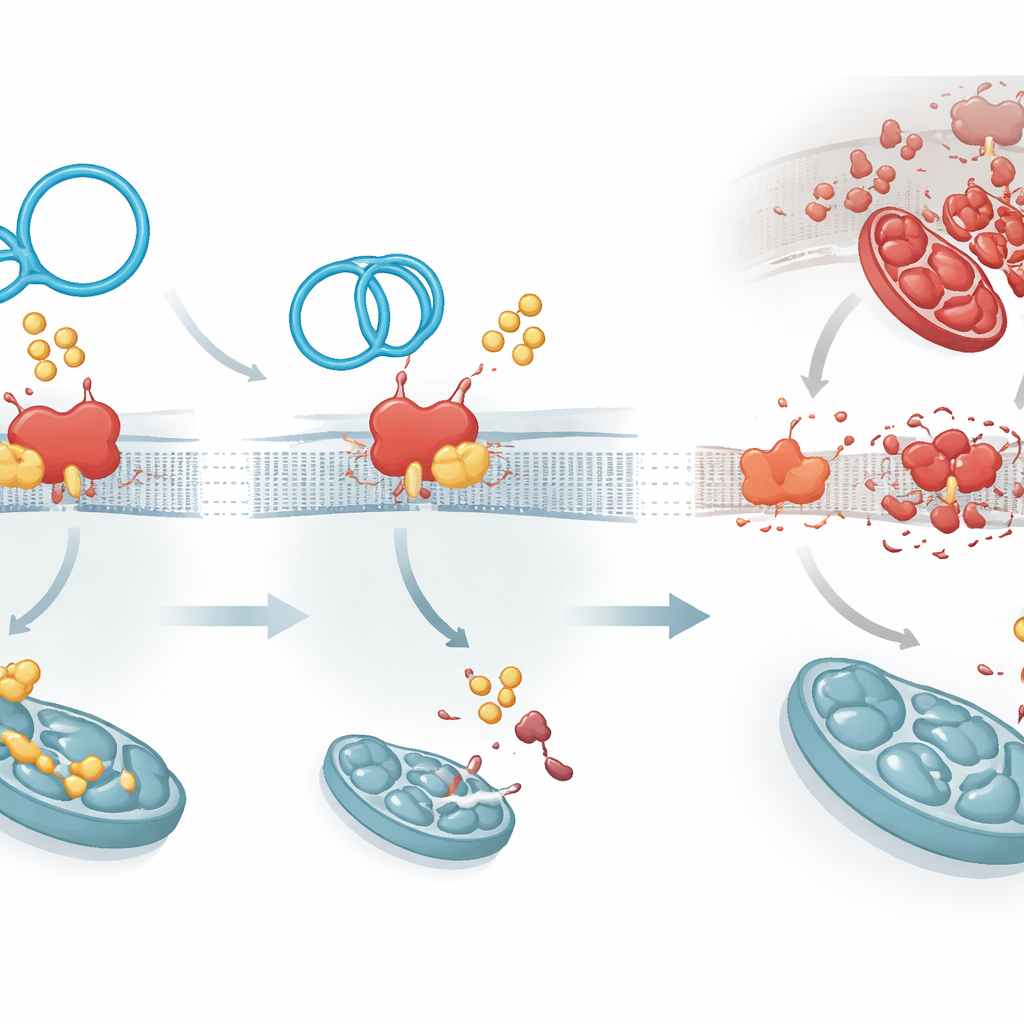
Ajustando o círculo e sua promessa para pacientes
O estudo também revela como o próprio circArhgap26 é reduzido durante a lesão. Uma marca química comum em RNA, chamada m6A, se acumula nesse RNA circular em corações estressados. Uma proteína “leitura” chamada YTHDF2 reconhece essa marca e promove a degradação do circArhgap26, enfraquecendo a defesa natural do coração justamente quando ela é mais necessária. Importante, a versão humana desse RNA circular é altamente semelhante à versão de camundongo e está nitidamente mais baixa no sangue de pacientes submetidos a procedimentos de reabertura de artéria em comparação com voluntários saudáveis. Em conjunto, esses achados sugerem que restaurar ou imitar o circArhgap26 poderia servir tanto como marcador de risco detectável no sangue quanto como uma terapia nova. Em termos simples, o trabalho revela uma pequena molécula circular que atua como guardiã contra o dano por reperfusão ao desarmar uma reação em cadeia letal dentro das células cardíacas.
Citação: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
Palavras-chave: lesão por isquemia e reperfusão, RNA circular, infarto, apoptose de cardiomiócitos, terapia baseada em RNA