Clear Sky Science · pt
Sinergia quimio‑fototérmica estimula a imunidade antitumoral via ferroptose
Transformando o calor e a luz do corpo em um combatente do câncer
Os medicamentos de quimioterapia podem reduzir tumores, mas frequentemente trazem efeitos colaterais severos e nem sempre impedem a recidiva do câncer. Este estudo investiga uma nova forma de fazer um fármaco já existente, o docetaxel, atuar com mais eficácia e precisão ao embalá‑lo em partículas minúsculas sensíveis ao calor e ativá‑las com luz no infravermelho próximo. O objetivo não é apenas matar células tumorais com maior precisão, mas também despertar o sistema imunológico para que ele reconheça e persiga o câncer por todo o organismo e previna recidivas futuras. 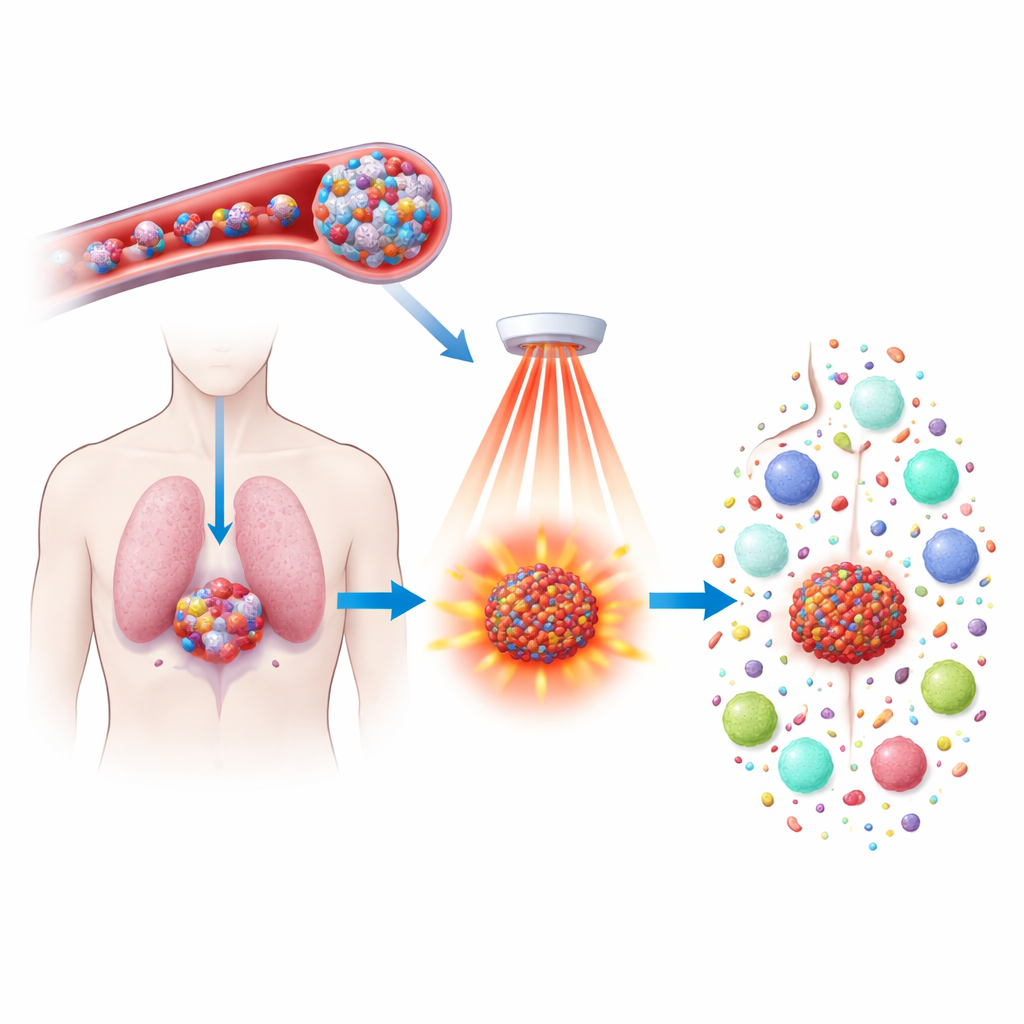
Pequenos mensageiros que sabem onde ir
Os pesquisadores construíram um novo tipo de nanopartícula a partir de um polímero contendo ferroceno, uma molécula com ferro que reage fortemente com peróxido de hidrogênio—um oxidante presente em níveis mais altos dentro de tumores do que em tecidos normais. Esses polímeros se auto‑assentam em esferas hidrofílicas que podem transportar tanto docetaxel quanto um corante absorvedor de luz chamado IR808. Uma vez injetadas na corrente sanguínea, as partículas são pequenas e estáveis o suficiente para circular e extravasar nos tumores, onde os vasos sanguíneos permeáveis e os altos níveis de peróxido de hidrogênio começam a enfraquecer as partículas e liberar lentamente sua carga. Esse projeto concentra o tratamento nos tumores enquanto limita danos aos órgãos saudáveis.
Usando a luz para potencializar o dano local
Luz no infravermelho próximo, que penetra tecidos de forma segura, é então direcionada à área do tumor. O IR808 dentro das nanopartículas absorve essa luz e a converte em calor, ao mesmo tempo em que gera espécies reativas de oxigênio. A combinação do peróxido de hidrogênio produzido pelo tumor e dos oxidantes gerados pela luz faz com que as partículas se desestabilizem mais rapidamente e liberem seu carregamento exatamente onde é necessário. Ao mesmo tempo, o ferro presente no segmento de ferroceno ajuda a transformar esses oxidantes em formas especialmente agressivas que atacam os componentes lipídicos das membranas celulares. Esse ataque químico e térmico direcionado aumenta drasticamente o poder de eliminação em comparação com docetaxel ou tratamento por luz isoladamente. 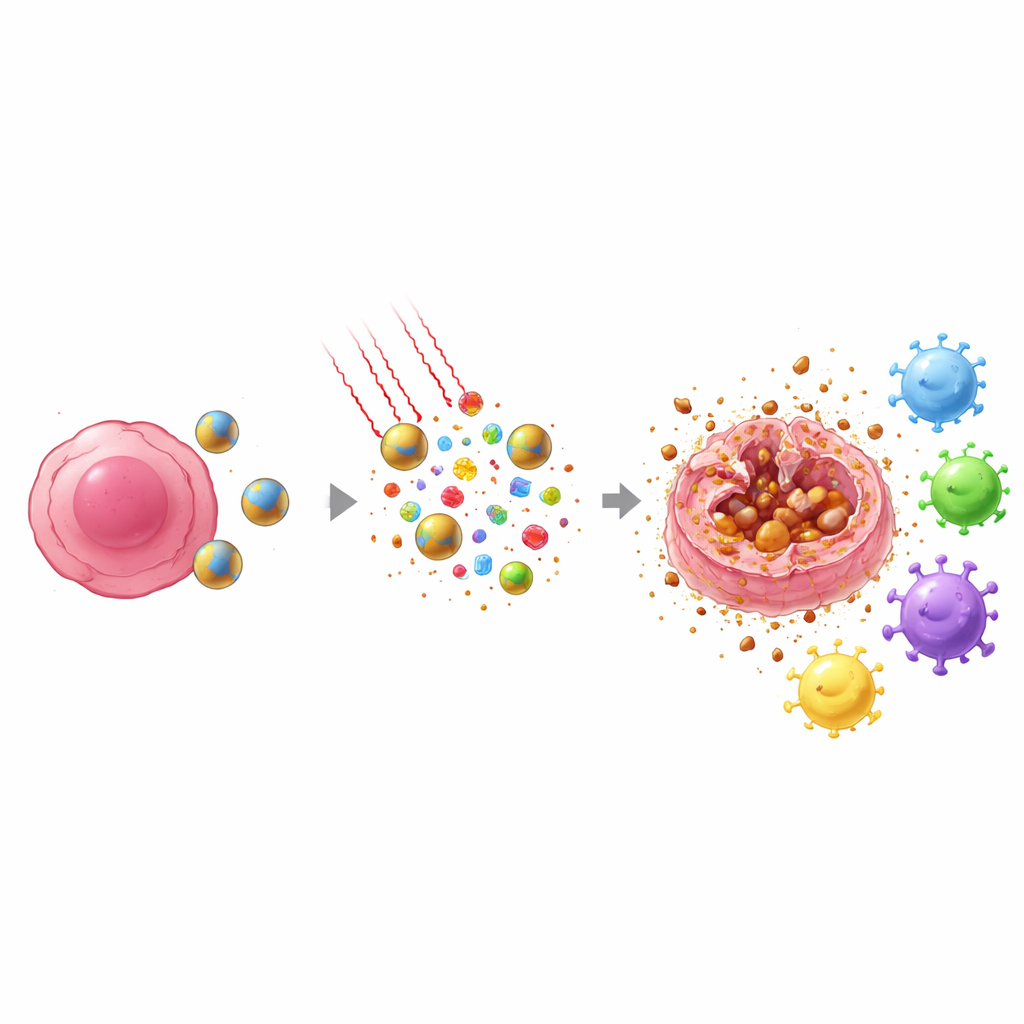
Uma queima controlada que sinaliza ao sistema imunológico
Importante, a forma como as células tumorais morrem sob esse tratamento é diferente da quimioterapia convencional. Em vez de se fragmentarem silenciosamente em restos ordenados, muitas células passam por um processo chamado ferroptose, uma forma de morte dependente de ferro que danifica lipídios e provoca ruptura da membrana externa. Quando isso ocorre, as células liberam sinais de alarme internos e fragmentos específicos do tumor no ambiente ao redor. Ao mesmo tempo, o docetaxel promove o deslocamento de uma proteína nuclear chave, HMGB1, em direção à borda celular, preparando‑a para ser liberada. Juntos, calor, oxidantes e a ação do fármaco geram uma explosão de sinais de perigo e antígeno que sentinelas imunes próximas—as células dendríticas—podem detectar e transportar para os linfonodos.
Do ataque local à defesa em todo o corpo
Em modelos tumorais de camundongos, esse tratamento combinado quimio‑fototérmico não só reduziu os tumores diretamente aquecidos mais eficazmente do que qualquer componente isolado, como também alterou o panorama imune. Os tumores apresentaram mais células dendríticas maduras e um maior número de células T citotóxicas, tanto no próprio tumor quanto nos linfonodos de drenagem. Em alguns camundongos com sistema imune competente, os tumores primários desapareceram após apenas dois ciclos de tratamento. Quando os cientistas implantaram posteriormente novos tumores em locais distantes ou no flanco oposto, esses crescimentos secundários foram retardados ou suprimidos, indicando que os animais haviam desenvolvido uma forma de memória imune específica contra o câncer. A adição de um anticorpo bloqueador de checkpoint que evita a exaustão das células T reduziu ainda mais as metástases pulmonares e estendeu a sobrevida, sugerindo que esse tratamento local pode ser combinado com imunoterapias modernas.
Por que isso importa para o cuidado futuro do câncer
Para quem não é especialista, a principal conclusão é que essa abordagem transforma o docetaxel de um veneno sistêmico de efeito bruto em parte de uma estratégia anticâncer inteligente e em vários passos. Ao embalar o fármaco em nanopartículas ativadas por luz e contendo ferro que respondem à própria química do tumor, a terapia causa mais dano dentro dos tumores enquanto poupa o tecido saudável. O padrão particular de morte celular que ela desencadeia age como uma vacina dentro do próprio tumor, ensinando o sistema imunológico a reconhecer e memorizar o câncer. Se esses achados se traduzirem em humanos, sistemas quimio‑fototérmicos assim poderiam ajudar a converter tumores “frios” resistentes em tumores “quentes” que respondem muito melhor a tratamentos baseados no sistema imunológico, potencialmente reduzindo recidivas e melhorando o controle a longo prazo.
Citação: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
Palavras-chave: nanomedicina contra o câncer, terapia fototérmica, ferroptose, imunoterapia do câncer, liberação de docetaxel