Clear Sky Science · pt
Ablation de DUSP6 restaura a aptidão de células CAR T prejudicada pela perda de CD58 tumoral por meio da reativação da sinalização AP-1
Por que reforçar células que combatem o câncer importa
Células imunes geneticamente modificadas chamadas CAR T transformaram o tratamento de alguns cânceres do sangue, mas muitos pacientes ainda recaem porque seus tumores aprendem a escapar do ataque. Este estudo revela uma vulnerabilidade oculta em certos tumores que silenciosamente desativa as CAR T por dentro — e mostra como um ajuste genético preciso pode restaurar a resistência, o suprimento de energia e a capacidade de matar dessas células. Para o leitor, é uma visão de como terapias celulares de próxima geração podem se tornar mais duradouras e eficazes para mais pessoas.
Uma alça que desapareceu nas células tumorais
As CAR T precisam de um contato firme com seu alvo para funcionar bem. Muitas células tumorais exibem uma molécula de superfície chamada CD58 que serve como uma “alça” para as células imunes, ajudando-as a se fixar e formar uma zona de contato apertada. Trabalhos anteriores mostraram que, quando os cânceres perdem CD58, as CAR T têm dificuldade em formar esse contato e se tornam menos eficazes. Neste estudo, os pesquisadores fizeram uma pergunta mais profunda: além desse problema mecânico de aperto de mãos, como a perda de CD58 reconfigura a biologia interna das CAR T para reduzir seu desempenho ao longo do tempo?
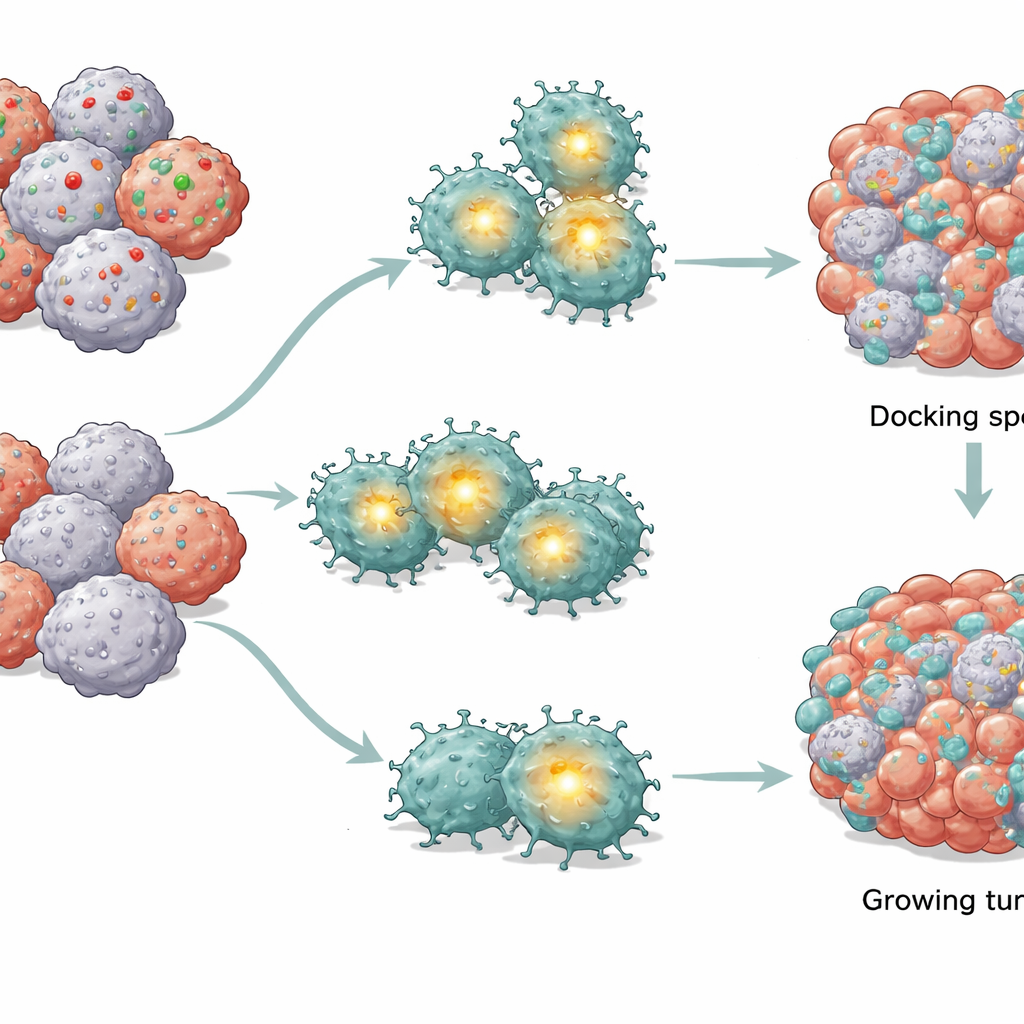
Fiação curta dentro das células CAR T
Ao comparar CAR T expostas a tumores normais com aquelas diante de tumores deficientes em CD58, a equipe descobriu que um centro regulador-chave dentro das células T — chamado AP-1 — estava seletivamente enfraquecido, enquanto outras vias principais de sinalização permaneciam amplamente intactas. AP-1 é um conjunto de proteínas que ativam genes envolvidos na ativação e sobrevivência. Quando a atividade de AP-1 caía, as CAR T exibiam sinais característicos de uma crise energética interna: menos e menores mitocôndrias (suas usinas de energia), capacidade reduzida de consumir oxigênio e usar açúcar, e perda da carga elétrica através das membranas mitocondriais. Ao mesmo tempo, moléculas reativas de oxigênio prejudiciais se acumulavam. Juntas, essas mudanças empurravam as CAR T para um programa de autodestruição baseado em danos dentro de suas próprias mitocôndrias, mesmo na ausência de sinais externos de morte.
Desligando um freio interno
Para entender por que o AP-1 estava tão suprimido, os pesquisadores buscaram a montante por “freios” moleculares que pudessem estar hiperativos. Eles descobriram que CAR T confrontadas com tumores CD58-negativos aumentavam várias fosfatases — enzimas que desligam vias de sinalização — particularmente uma chamada DUSP6. Usando drogas e depois edição genética precisa para bloquear essas enzimas, descobriram que remover DUSP6 foi o que mais fortemente reviveu a atividade de AP-1. As CAR T editadas para DUSP6 expandiram melhor, formaram mais mitocôndrias, queimaram combustível com mais eficiência, produziram mais moléculas que matam o câncer e foram menos propensas à apoptose, especialmente quando desafiadas repetidamente por células tumorais deficientes em CD58.
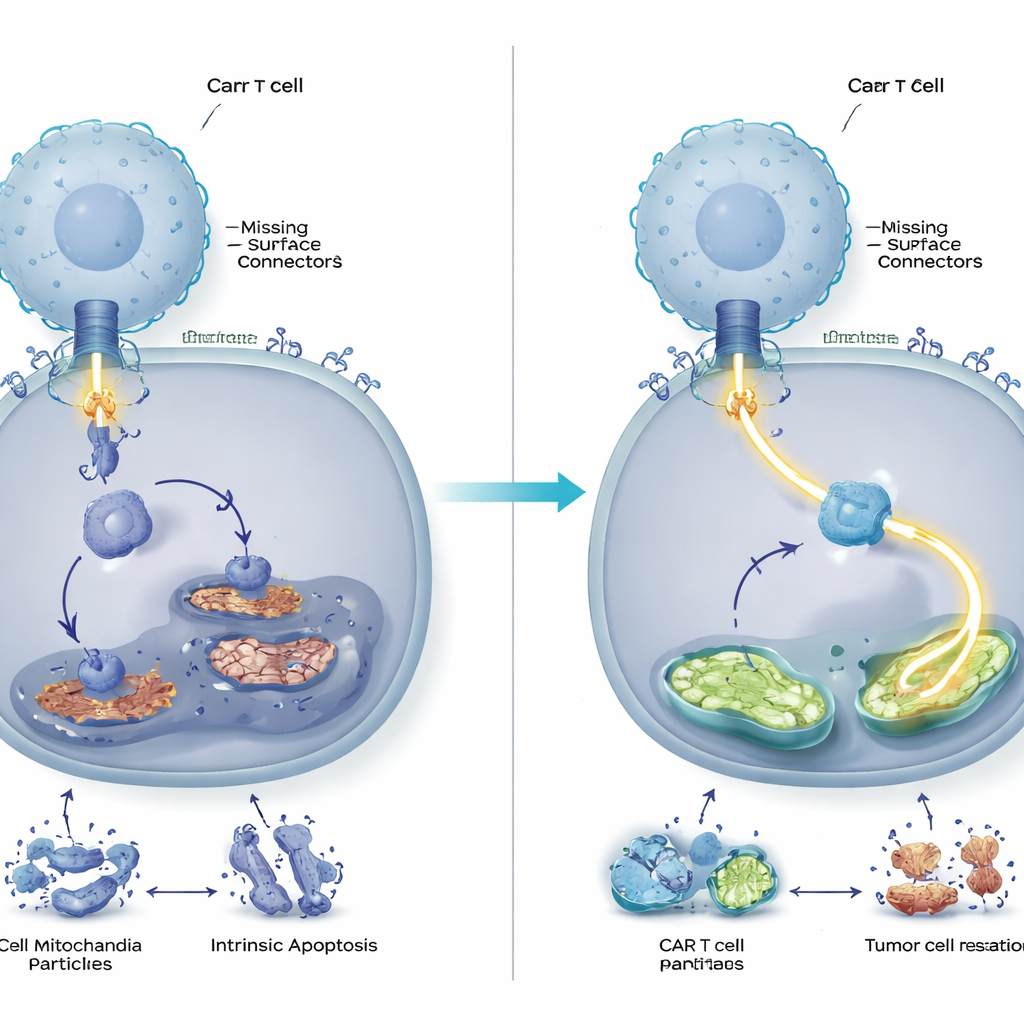
Controle tumoral mais forte e duradouro em animais
A equipe então testou se esse ajuste molecular fazia diferença em sistemas vivos. Em camundongos carregando células de câncer de sangue humano que tinham ou não CD58, as CAR T deficientes em DUSP6 eliminaram tumores de forma mais eficaz e os mantiveram sob controle por mais tempo do que CAR T convencionais. As células modificadas se multiplicaram com mais robustez, exibiram menos marcadores de exaustão e secretaram níveis maiores de mensageiros imunológicos chave. Notavelmente, os benefícios da remoção de DUSP6 foram observados não apenas quando os tumores careciam de CD58, mas também quando o conservavam, sugerindo que essa modificação poderia aumentar amplamente as terapias com CAR T em vez de ser uma correção restrita para um subtipo tumoral raro.
Pistas a partir de dados de pacientes
Para explorar a relevância em humanos, os pesquisadores examinaram dados de expressão gênica de pessoas tratadas com CAR T ou com drogas que bloqueiam checkpoints imunes. Em pacientes com linfoma difuso de grandes células B que receberam uma terapia CAR T de alvo duplo, níveis mais baixos de DUSP6 em células T CD8 antes ou logo após a infusão foram associados a taxas mais altas de resposta completa. Em uma coorte separada de câncer de pele tratada com anticorpos anti–PD-1, células T CD8 exauridas de não respondedores tenderam a expressar mais DUSP6 do que as de respondedores. Em conjunto, essas observações sugerem que DUSP6 age como um marcador negativo de aptidão das células T em diferentes imunoterapias e que reduzi-lo poderia melhorar os desfechos.
O que isso significa para terapias futuras contra o câncer
Para um leitor leigo, a mensagem é que alguns tumores escapam do ataque de CAR T não apenas escondendo-se do reconhecimento, mas sabotarando os motores internos das células. Perder a “alça” CD58 nas células tumorais diminui silenciosamente a sinalização AP-1 nas CAR T, esvaziando suas mitocôndrias, elevando subprodutos tóxicos e impulsionando-as para uma morte precoce. Ao remover o freio DUSP6, os cientistas podem restaurar essa sinalização perdida, reparar a saúde mitocondrial e dar às CAR T maior resistência e poder de eliminação, mesmo contra tumores resistentes. Embora sejam necessários mais testes de segurança e clínicos, a ablação de DUSP6 surge como uma estratégia promissora de engenharia para tornar medicamentos vivos contra o câncer mais potentes, duradouros e potencialmente eficazes para uma gama mais ampla de pacientes.
Citação: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
Palavras-chave: Células CAR T, CD58, DUSP6, imunoterapia contra o câncer, metabolismo de células T