Clear Sky Science · pt
Liberando o potencial da via STING mediada por nanobomba bimetálica para aprimorar engajadores bispecíficos de células T contra a fotoimuno‑terapia do câncer colorretal
Transformando o sistema imune contra o câncer de cólon
Os cânceres de cólon e reto são comuns e frequentemente letais, em parte porque os tumores aprendem a se esconder do sistema imunológico. Este estudo explora uma nova estratégia que reúne várias táticas anticâncer em uma pequena "nanobomba" para despertar as defesas do corpo, ajudar as células imunes a localizar o tumor e evitar que o câncer retorne ou se espalhe.
Por que os medicamentos imunológicos atuais precisam evoluir
Uma classe promissora de medicamentos contra o câncer, chamada engajadores bispecíficos de células T, funciona como corretores biológicos: uma extremidade captura uma célula T (um importante combatente imune) e a outra se liga a um marcador na célula tumoral, forçando o contato para que a célula T mate o tumor. Embora eficazes em cânceres hematológicos, esses fármacos têm dificuldades em tumores sólidos como o colorretal. Eles são eliminados rapidamente do corpo, podem atacar tecidos saudáveis que compartilham o mesmo marcador e frequentemente enfrentam tumores "frios" que não têm células imunes suficientes para que o tratamento funcione. Médicos e cientistas, portanto, procuram formas de administrar esses medicamentos com mais segurança e converter tumores frios em "quentes", repletos de células imunes ativadas.
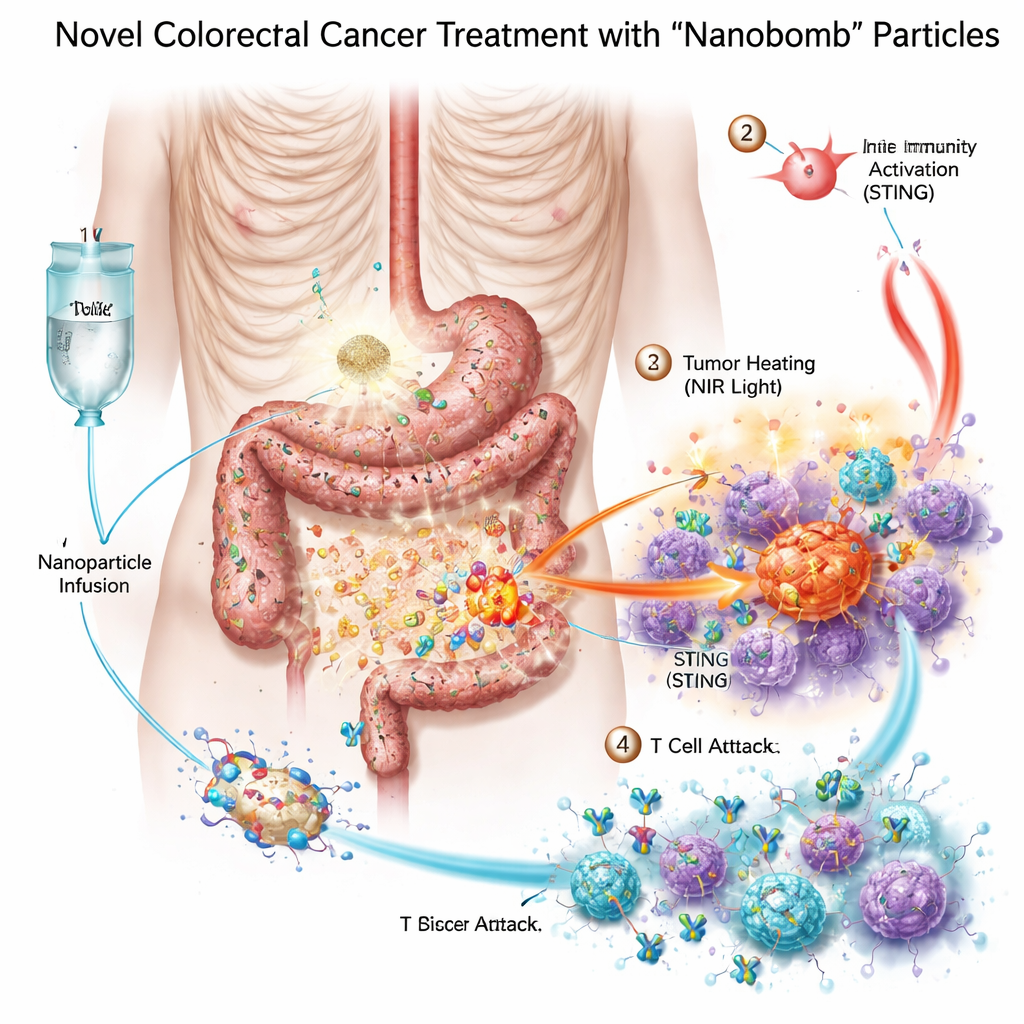
Empacotando três armas em uma pequena “nanobomba”
Os pesquisadores projetaram uma nanobomba bimetálica—cientificamente denominada MnO2/Co‑DA@BiTE/HPT—que combina três modos de tratamento em uma única partícula. Primeiro, o núcleo contém manganês e cobalto, metais que podem ativar um sistema de alarme celular chamado via STING, que ajuda o organismo a detectar perigo e convocar células imunes. Segundo, a superfície da partícula é revestida com um engajador bispecífico de células T que conecta células T às células tumorais. Terceiro, o material absorve luz no infravermelho próximo, permitindo aquecer o tumor externamente em uma forma de terapia fototérmica. Para garantir que as nanobombas se dirijam às células do câncer colorretal, a equipe acrescentou um pequeno trecho de DNA, um aptâmero, que reconhece PD‑L1, uma molécula frequentemente abundante nesses tumores. Uma vez que essas partículas alcançam o tumor, enzimas naturais no tecido tumoral ajudam a fragmentá‑las e liberar sua carga exatamente onde é necessário.
Aquecendo, soando o alarme e recrutando o exército imune
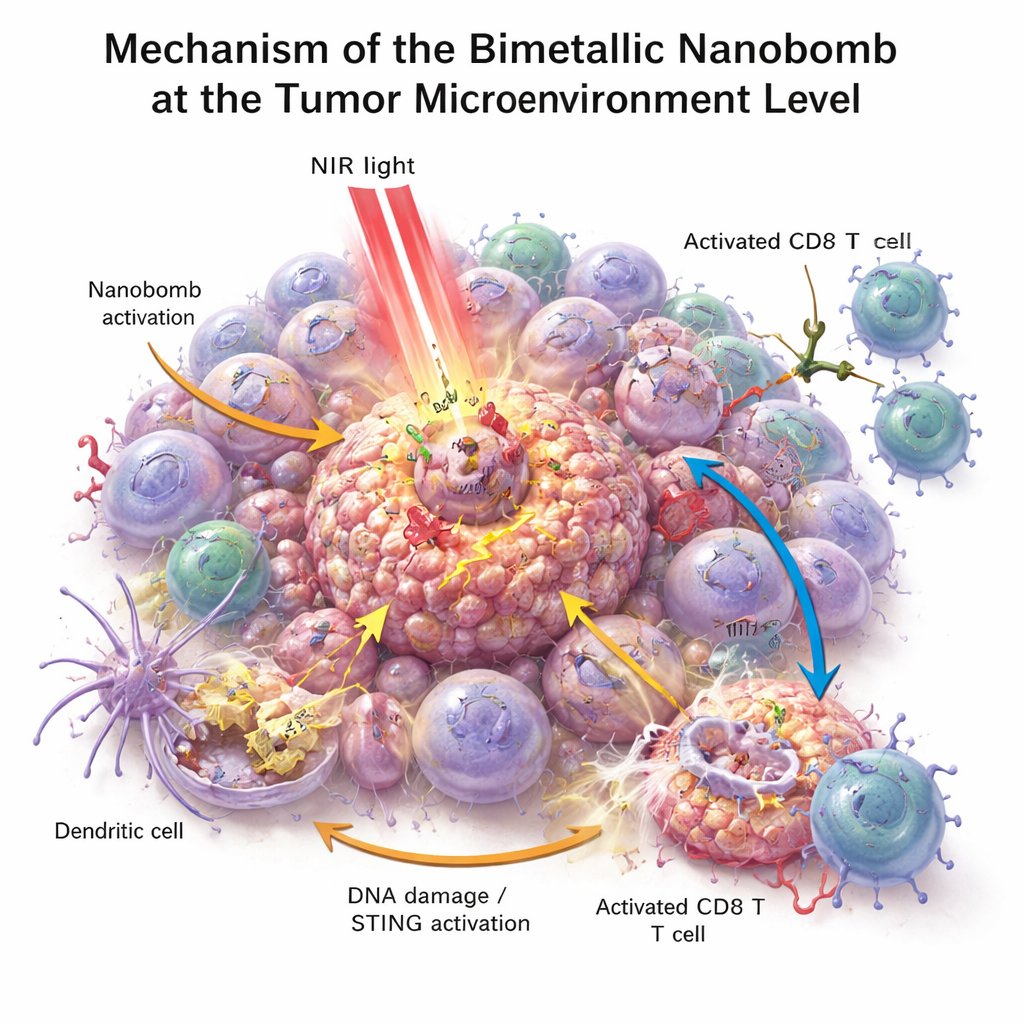
Em placas de laboratório, as nanobombas mataram células de câncer colorretal de maneira mais eficaz do que qualquer componente isolado. Quando iluminadas com luz no infravermelho próximo, as partículas aqueceram, estressaram e danificaram as células tumorais, e ajudaram a gerar espécies reativas de oxigênio—moléculas altamente reativas que agravam o dano às células tumorais. Esse estresse quebrou o DNA das células e as levou a uma forma de morte particularmente visível que emite sinais de "perigo". Células imunes próximas, especialmente células dendríticas, engoliram o material tumoral em morte e ativaram a via STING com a ajuda do manganês e do cobalto liberados. Em seguida produziram interferons e outras moléculas inflamatórias que amadurecem e atraem células T. Ao mesmo tempo, o engajador bispecífico na nanobomba ligou fisicamente as células T às células tumorais PD‑L1‑positivas, melhorando a ativação e a citotoxicidade das células T mesmo em tumores previamente frios.
Da redução do tumor à memória imune duradoura
Em vários modelos de camundongos—including tumores colorretais subcutâneos, tumores em ambos os lados do corpo, metástases pulmonares e um modelo de recidiva pós‑cirúrgica—as nanobombas mais luz retardaram fortemente ou quase estancaram o crescimento tumoral. Tumores tratados continham muito mais células T CD8 citotóxicas e menos células T reguladoras que normalmente suprimem respostas imunes. Células dendríticas dentro dos tumores e nos linfonodos mostraram sinais de maturação, e exames de sangue revelaram níveis elevados de citocinas estimuladoras do sistema imune. Importante, camundongos que eliminaram seus tumores após o tratamento com nanobombas estavam melhor protegidos quando o câncer foi reintroduzido, e desenvolveram menos metástases pulmonares, demonstrando que a terapia ajudou a construir memória imune de longo prazo em vez de apenas causar uma redução tumoral pontual.
O que isso pode significar para o futuro do tratamento do câncer
Este trabalho apresenta uma nanomedicina de "triplo impacto" que aquece tumores, ativa um alarme interno de perigo e guia células T diretamente até as células tumorais, tudo em uma única partícula direcionada. Em camundongos, essa abordagem não só transformou tumores colorretais frios em tumores quentes e inflamados, como também ajudou a prevenir recidivas e disseminação. Embora a tecnologia ainda esteja distante do uso clínico—escalonamento, segurança a longo prazo e testes em humanos permanecem desafios importantes—ela oferece um roteiro para futuros tratamentos que combinam materiais inteligentes com fármacos imunológicos para proporcionar aos pacientes uma resposta anticâncer mais forte e duradoura.
Citação: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
Palavras-chave: câncer colorretal, imunoterapia, nanopartículas, via STING, engajador bispecífico de células T