Clear Sky Science · pt
Terapia guiada personalizada por farmacocinética–farmacodinâmica via plataforma multi-organoide derivada de células-tronco pluripotentes induzidas em câncer de mama mutante para NF1
Por que esta pesquisa importa para os pacientes
Muitas pessoas com câncer recebem medicamentos que funcionam bem em alguns pacientes, mas não em outros, e frequentemente causam efeitos colaterais severos. Este estudo descreve uma nova maneira de testar tratamentos contra o câncer fora do corpo usando mini-órgãos cultivados em laboratório a partir das próprias células do paciente. O trabalho foca em uma forma de câncer de mama de difícil tratamento impulsionada por alterações no gene chamado NF1 e mostra como combinar uma estratégia de correção gênica com um medicamento direcionado pode levar a uma terapia mais segura, mais eficaz e verdadeiramente personalizada.
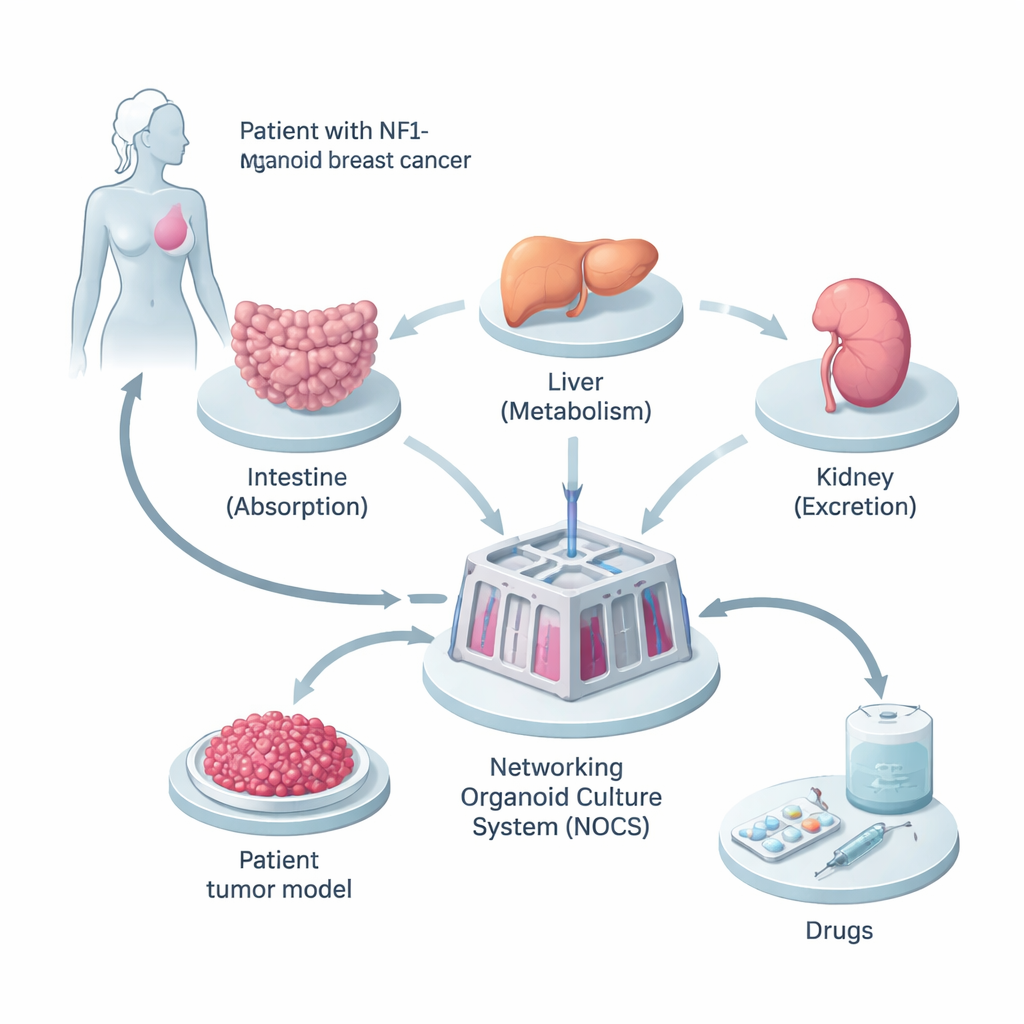
Construindo uma versão em miniatura do corpo do paciente
Os pesquisadores começaram com tecido de uma mulher cujo câncer de mama apresentava uma mutação herdada no gene NF1. Eles reprogramaram suas células normais semelhantes à pele em células-tronco pluripotentes induzidas, que podem se diferenciar em quase qualquer tipo celular do corpo. A partir dessas, cultivaram três tipos de mini-órgãos—intestino delgado, fígado e rim—porque são os locais-chave onde os fármacos são absorvidos, processados e eliminados. Em paralelo, criaram “esferoides” tumorais 3D a partir das células cancerígenas dela, preservando a mistura de tipos celulares e as alterações genéticas encontradas no tumor original.
Um circuito vivo para testar medicamentos
Para fazer esses mini-órgãos se comportarem mais como um corpo real, a equipe os conectou em um dispositivo preenchido por fluido chamado Sistema de Cultura de Organoides em Rede, ou NOCS. Neste arranjo, o meio líquido flui entre os compartimentos de intestino, fígado, rim e tumor, imitando a circulação sanguínea. Os medicamentos podem ser adicionados de forma que se assemelhe a engolir um comprimido ou receber uma injeção, e sensores e bombas controlam a velocidade do “sangue” e com que frequência ele é renovado. Isso permitiu aos cientistas rastrear quanto do fármaco é absorvido, quão rápido ele é degradado e quão fortemente age sobre o tumor—tudo em um modelo humano específico do paciente.
Corrigindo um gene defeituoso com exclusão de éxon
O tumor da paciente carregava uma mutação prejudicial no NF1 que mantém vias de crescimento ativadas e torna muitos medicamentos padrão ineficazes. A equipe desenhou pequenos fragmentos de material genético, chamados oligonucleotídeos antissenso, para fazer com que a maquinaria de processamento de RNA da célula ignore a peça defeituosa (éxon 2) do gene NF1. Usando um sistema de entrega viral que permanece ativo por dias, eles induziram uma “exclusão de éxon” estável nas células cancerígenas da paciente. Isso produziu uma proteína NF1 mais curta, mas funcional, reduziu os sinais de crescimento hiperativos e tornou as células tumorais mais sensíveis ao tratamento.
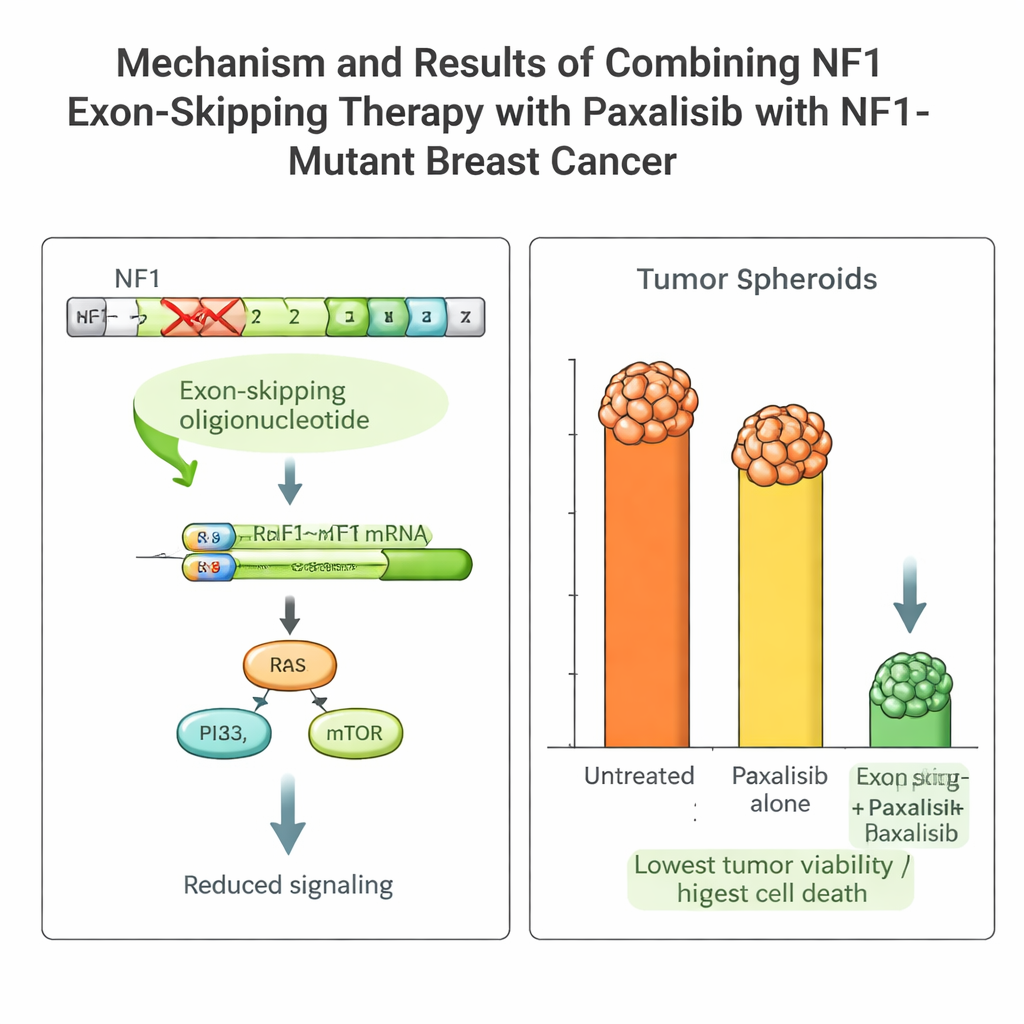
Escolhendo o medicamento direcionado certo com orientação PK/PD
Com esta plataforma, a equipe comparou vários medicamentos avançados que bloqueiam a via PI3K–mTOR, que atua a jusante do NF1. Eles mediram farmacocinética (como o organismo lida com o fármaco) e farmacodinâmica (como o fármaco age sobre o tumor) tanto em camundongos quanto no NOCS. Um medicamento, Paxalisibe, destacou-se: foi bem absorvido no intestino, persistiu no sistema em níveis úteis e mostrou comportamento semelhante em animais e no dispositivo de organoides. Quando combinado com a exclusão do éxon de NF1, o poder de morte celular do Paxalisibe contra as células tumorais da paciente aumentou dramaticamente, com fortes reduções no crescimento e sinais claros de morte celular programada, tanto no NOCS quanto em camundongos carregando o tumor da paciente.
Equilibrando benefício e risco entre órgãos
Porque os modelos de intestino, fígado e rim faziam parte do mesmo circuito, os pesquisadores também puderam observar sinais precoces de dano orgânico. O Paxalisibe causou respostas de estresse e enfraquecimento sutil das barreiras nos modelos de intestino e rim e sinais de sobrecarga no fígado, mas sem perda significativa da viabilidade celular na dose testada. Esse tipo de visão de todo o corpo, usando tecido humano, oferece uma maneira de comparar opções de tratamento não apenas por quanto reduzem tumores, mas também por como podem afetar órgãos saudáveis antes que um medicamento chegue a um paciente.
O que isso pode significar para o cuidado futuro do câncer
Em termos simples, este estudo mostra que agora é possível cultivar um “mini corpo em um chip” simplificado e específico do paciente que pode testar como diferentes medicamentos—e até abordagens de correção gênica—vão se comportar e interagir. Para esta paciente com câncer de mama mutante para NF1, a estratégia ótima foi uma combinação da terapia de exclusão de éxon de NF1 e do fármaco oral Paxalisibe, que juntos retardaram o crescimento tumoral muito mais do que cada um isoladamente. Se desenvolvidas e testadas em mais pacientes, tais plataformas poderiam orientar médicos para planos de tratamento adaptados aos genes e à biologia de cada pessoa, aumentando as chances de sucesso enquanto reduzem toxicidade desnecessária.
Citação: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
Palavras-chave: oncologia personalizada, câncer de mama, organoides, mutação NF1, terapia direcionada