Clear Sky Science · pt
GPR54 regula o desenvolvimento do câncer de pulmão não pequenas células via dopa descarboxilase
Por que essa história sobre câncer de pulmão importa
O câncer de pulmão continua sendo um dos mais letais, e a maioria dos casos corresponde a uma forma chamada câncer de pulmão não pequenas células (CPNPC). Muitos pacientes acabam ficando sem opções de tratamento eficazes porque os tumores se adaptam ou resistem aos medicamentos atuais. Este estudo revela um sistema de controle antes pouco apreciado dentro das células de câncer de pulmão, centrado em um receptor chamado GPR54 e em uma enzima chamada dopa descarboxilase (DDC). Ao entender como essas moléculas ajudam os tumores a crescer e a se alimentar, os pesquisadores apontam para novas maneiras de retardar ou até reduzir o CPNPC.
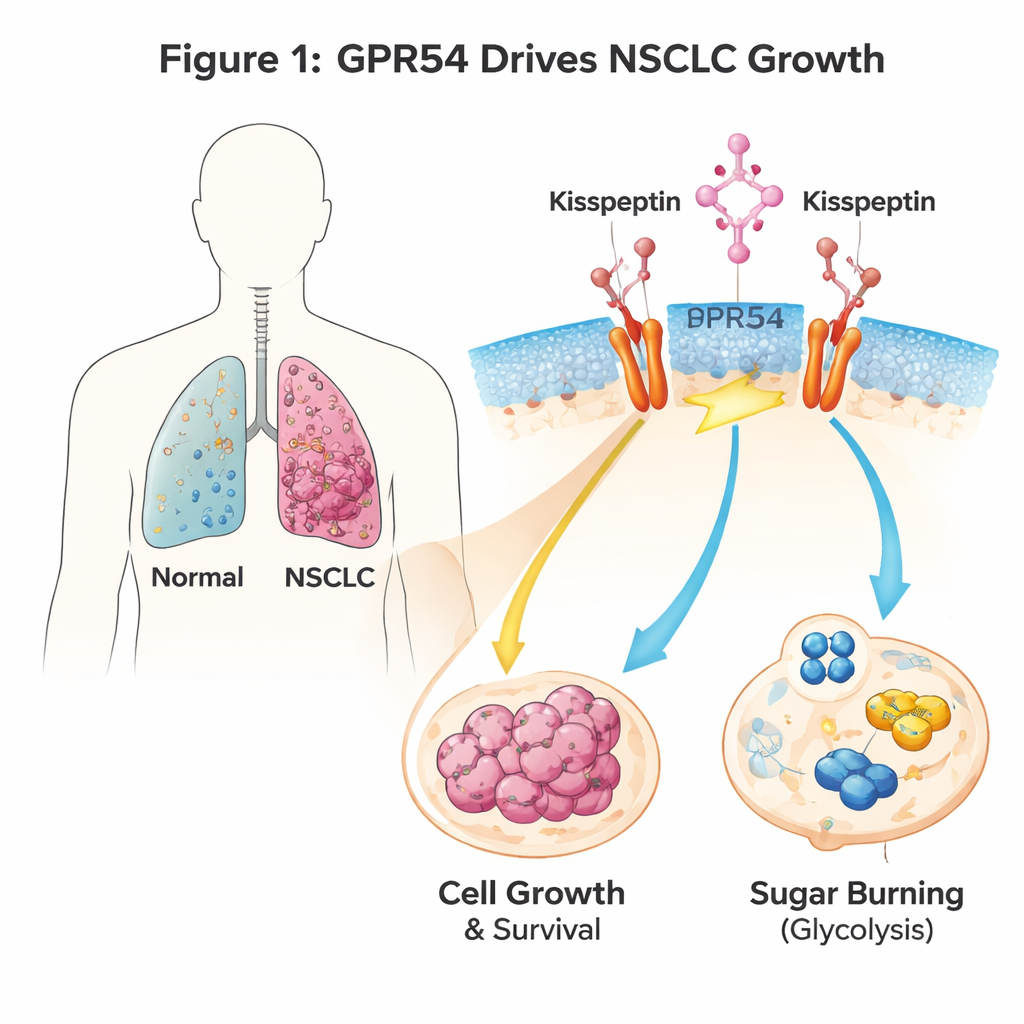
Um interruptor de sinal nas células do câncer de pulmão
GPR54 é um sensor que fica na superfície das células e responde a um sinal natural chamado kisspeptina. É mais conhecido por papéis na puberdade e na reprodução, mas também aparece em muitos cânceres. Os autores usaram camundongos geneticamente modificados que desenvolvem CPNPC quando um gene promotor de câncer chamado Kras é ativado nas células pulmonares. Quando eles deletaram o gene Gpr54 nesses animais, os animais viveram mais, desenvolveram tumores pulmonares em menor número e menores, e suas células cancerosas mostraram sinais claros de autodestruição (apoptose). Linhagens humanas de CPNPC contaram a mesma história: quando os níveis de GPR54 foram reduzidos, as células tumorais cresceram mais devagar, formaram menos colônias e morreram mais facilmente, independentemente de suas mutações genéticas específicas.
Como GPR54 mantém as células tumorais vivas
Aprofundando, os pesquisadores perguntaram quais circuitos internos o GPR54 usa. Eles descobriram que o GPR54 alimenta duas grandes vias de crescimento dentro da célula, conhecidas como AKT e ERK. Ambas são “hubs” de sinalização comuns que dizem às células cancerosas para se dividir e resistir à morte. Quando GPR54 foi bloqueado ou removido, a atividade de AKT e ERK caiu, e as células tornaram-se mais propensas à apoptose. Restaurar sinais fortes de AKT ou ERK pôde resgatar parcialmente as células, confirmando que GPR54 ajuda as células de CPNPC a sobreviver ao apoiar esses circuitos de crescimento.
Reconfigurando como o câncer usa açúcar
Células cancerosas frequentemente reprogramam o uso de nutrientes, favorecendo a quebra rápida de açúcar (glicólise) para abastecer o crescimento. Perfis de atividade gênica de tumores de camundongos sem Gpr54 mostraram que muitos genes envolvidos no manejo de glicídios e na produção de energia foram reduzidos. Em células de câncer de pulmão tratadas com kisspeptina para ativar GPR54, medidas do uso de oxigênio e da produção de ácido — proxies para o metabolismo energético — revelaram que GPR54 aumenta a glicólise. Bloquear a via GPR54 em vários pontos (o interruptor Gαq/11, PI3K, AKT ou mTOR) reduziu o consumo de glicose e a produção de lactato e empurrou as células em direção à apoptose. Em termos simples, GPR54 ajuda as células de CPNPC a queimar açúcar mais rápido e com mais eficiência, sustentando seu crescimento acelerado.
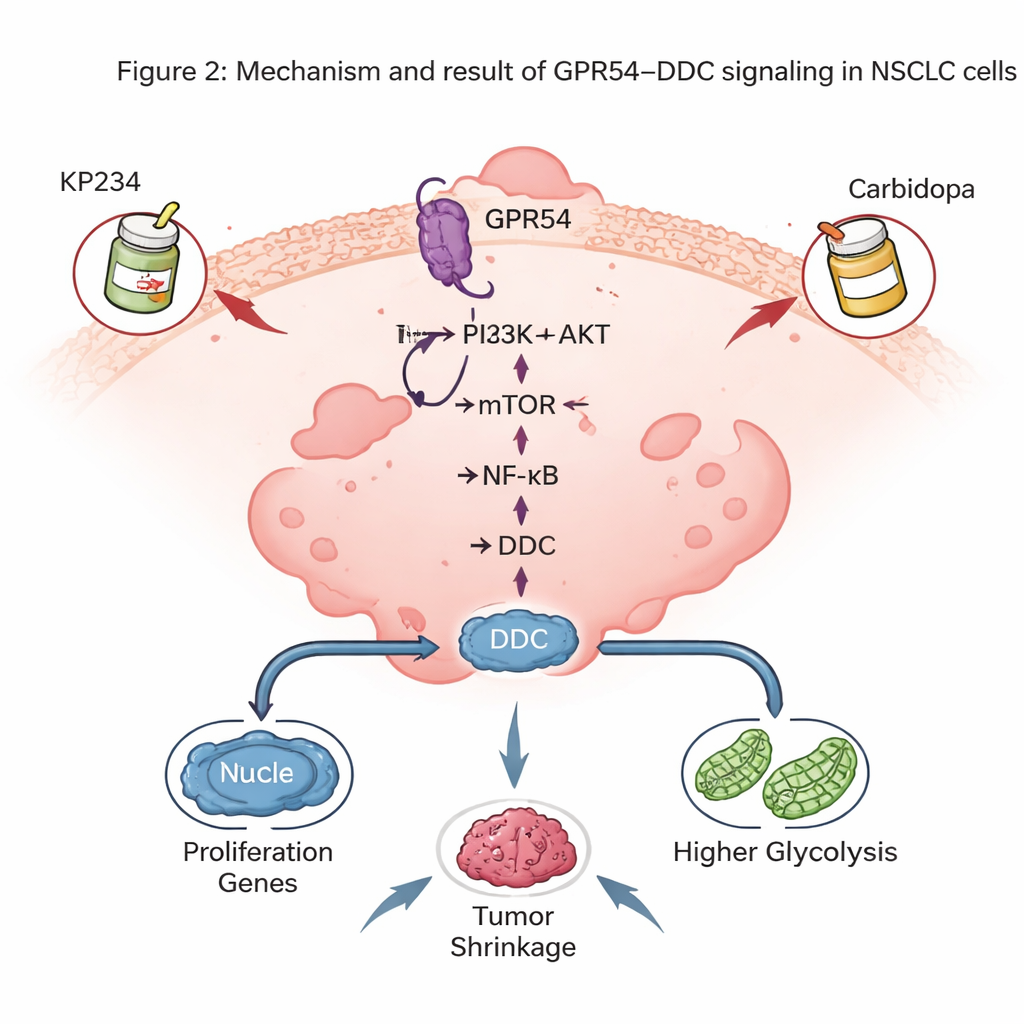
O papel surpreendente de uma enzima relacionada ao cérebro
Uma das descobertas mais marcantes foi que GPR54 controla os níveis de DDC, uma enzima mais conhecida por produzir os neurotransmissores dopamina e serotonina. Em tumores de camundongo, os níveis de DDC acompanharam de perto a quantidade de GPR54: menos GPR54 significou menos DDC. Tumores humanos de CPNPC e linhas celulares também mostraram DDC mais alto do que células pulmonares normais, e pacientes com mais DDC tiveram sobrevida pior. Reduzir DDC em células de câncer de pulmão retardou o crescimento tumoral em camundongos, diminuiu a divisão celular em cultura e desencadeou mais apoptose. Em nível molecular, DDC ajudou a manter a atividade na via NF-κB, um regulador mestre que promove a sobrevivência das células cancerosas e a inflamação, e também sustentou o estado de alta glicólise das células tumorais.
Testando uma estratégia de combinação de drogas
Como DDC já é alvo no tratamento da doença de Parkinson por meio de um fármaco chamado carbidopa, os autores exploraram se combinar um bloqueador de GPR54 (KP234) com carbidopa poderia atacar o CPNPC por duas frentes. Em cultura celular e em modelos de camundongo onde células humanas de CPNPC foram crescidas no pulmão, o tratamento duplo reduziu o crescimento tumoral mais do que qualquer droga isolada e aumentou a morte das células cancerosas, sem perda de peso óbvia nos animais. Essas combinações também mostraram potencial junto com alguns medicamentos-alvo modernos direcionados a genes RAS mutantes, sugerindo que o sinal GPR54–DDC pode ser combinado com terapias de precisão já existentes.
O que isso significa para o cuidado futuro do câncer de pulmão
Para um público leigo, a mensagem principal é que células de CPNPC dependem de uma parceria até então pouco valorizada entre um interruptor de superfície (GPR54) e uma enzima metabólica (DDC) para permanecerem vivas e queimarem combustível rapidamente. Disromper essa parceria enfraquece os tumores, fazendo-os crescer mais devagar e morrer mais facilmente em modelos experimentais. Embora muito trabalho ainda seja necessário antes que tais estratégias cheguem à clínica, este estudo posiciona GPR54 e DDC como potenciais biomarcadores para identificar CPNPC agressivo e como alvos promissores para novas combinações de tratamento que possam melhorar os resultados para pacientes cujos tumores hoje escapam às terapias padrão.
Citação: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
Palavras-chave: câncer de pulmão não pequenas células, GPR54, dopa descarboxilase, metabolismo do câncer, terapia alvo