Clear Sky Science · pt
Espécies reativas de oxigênio (ERO) no câncer: do mecanismo às implicações terapêuticas
Quando moléculas úteis se tornam perigosas
Dentro de cada célula, pequenas fagulhas químicas chamadas espécies reativas de oxigênio, ou ERO, são constantemente produzidas como parte da vida normal. Em níveis adequados, elas ajudam as células a crescer, comunicar-se e defender-se contra germes. Mas esta revisão explica como as mesmas moléculas também podem danificar o DNA, torcer o circuito celular e impulsionar o câncer a crescer, espalhar-se e resistir ao tratamento. Compreender essa “dupla vida” das ERO tem ajudado cientistas a projetar novas terapias contra o câncer que ou acalmam o estresse oxidativo prejudicial ou o empurram deliberadamente além do limite para matar células tumorais.
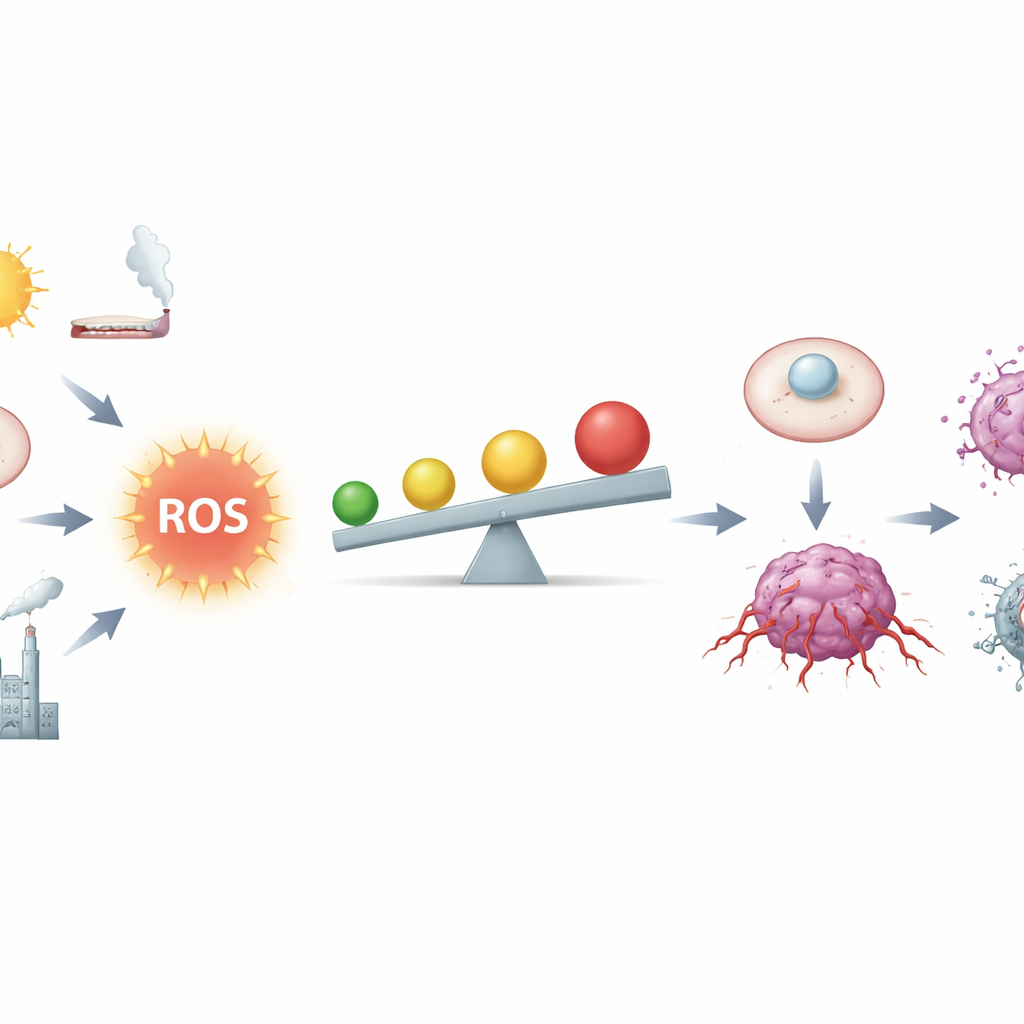
A tênue linha entre combustível e fogo
Os autores descrevem as ERO como subprodutos químicos da respiração e do metabolismo, mas também como mensageiros potentes. Em tecidos saudáveis, pequenas quantidades de ERO ajudam a controlar o ciclo celular, reparar danos e ajustar a imunidade. As células mantêm esses sinais sob controle usando uma intrincada rede antioxidante, incluindo moléculas como a glutationa e enzimas reguladas por um interruptor mestre chamado Nrf2. As células cancerosas, porém, vivem mais próximas da zona de perigo: genes defeituosos, mitocôndrias sobrecarregadas, inflamação crônica, fumaça do tabaco, radiação e certos metais elevam as ERO. Em níveis moderadamente altos, as ERO podem fender o DNA, desestabilizar cromossomos e manter circuitos de crescimento e sobrevivência cronicamente “ligados”, facilitando que uma célula normal se torne cancerosa.
Como o estresse oxidativo molda o comportamento tumoral
Uma vez estabelecido o tumor, as ERO continuam a moldar sua biologia. Estresse oxidativo moderado ativa muitas vias de crescimento que incentivam as células a dividir-se, vascularizar, invadir tecidos próximos e resistir à quimioterapia. As ERO podem reprogramar como as células cancerosas usam açúcares, gorduras e aminoácidos, direcionando combustíveis para rotas que geram poder antioxidante extra e blocos de construção para novas células. Elas também influenciam decisões de destino celular: dependendo da intensidade e do contexto, as ERO podem inclinar o equilíbrio para sinais de sobrevivência ou para uma de várias formas de morte celular programada, incluindo a apoptose clássica e formas mais recentes como ferroptose, necroptose e cuproptose. Isso torna as ERO tanto cúmplices na progressão tumoral quanto potenciais gatilhos da autodestruição do tumor.
Reconfigurando a imunidade e a resposta aos medicamentos
A revisão destaca que as ERO não atuam apenas dentro das células cancerosas — elas remodelam o entorno tumoral. Estresse oxidativo elevado pode exaurir ou matar linfócitos T e células natural killer que combatem o câncer, ao mesmo tempo em que favorece células supressoras que protegem o tumor do ataque. As ERO também ajudam os tumores a aumentar sinais de “não me mate”, como proteínas de checkpoint, atenuando os efeitos da imunoterapia. Ao mesmo tempo, níveis moderados de ERO podem impulsionar resistência a medicamentos ao reforçar bombas de efluxo de fármacos e respostas ao estresse, permitindo que as células tumorais expulsem a quimioterapia ou reparem os danos que ela causa. Ainda assim, em outras condições, elevar as ERO além de um limiar crítico pode desmontar essas defesas, ressensibilizando tumores ao tratamento.
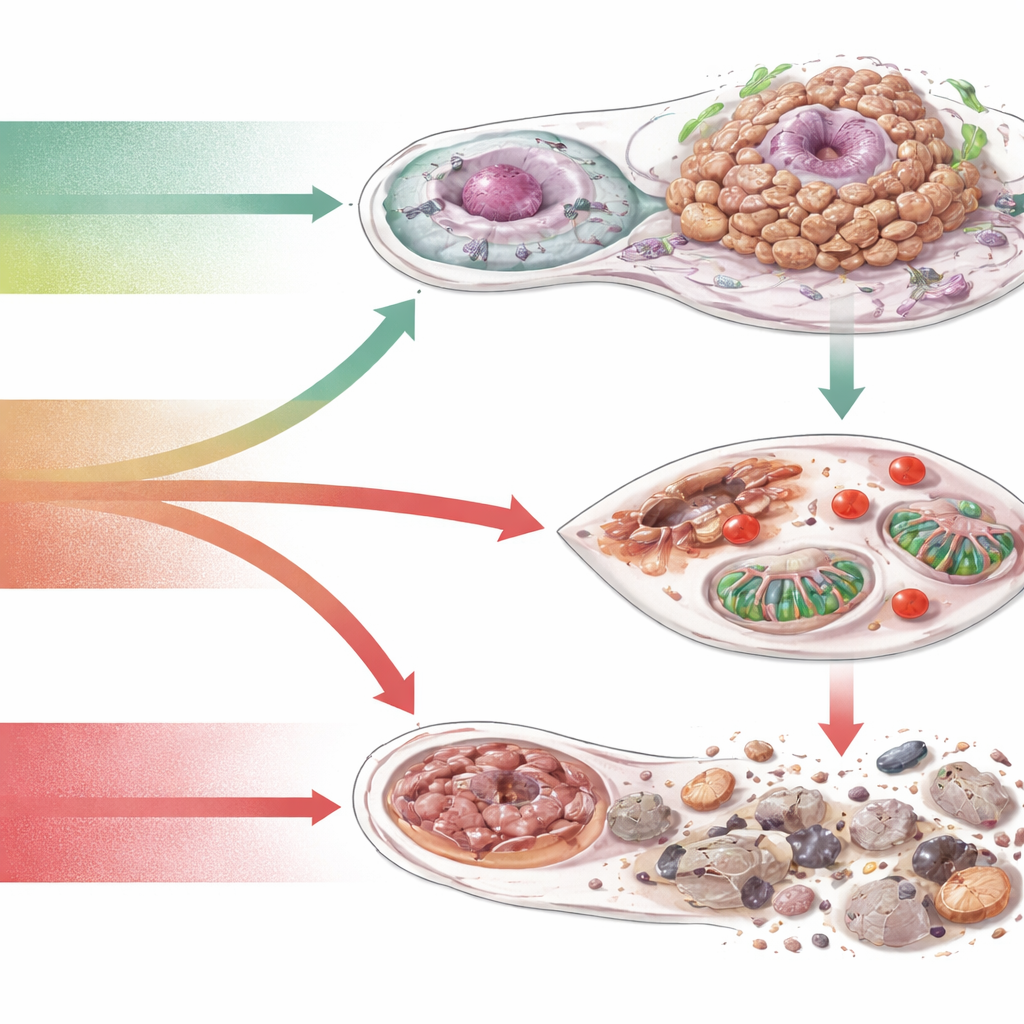
Transformando fragilidades redox em estratégia terapêutica
Porque as células cancerosas caminham sobre um fio entre usar ERO e serem envenenadas por elas, os autores veem o equilíbrio das ERO como uma alavanca terapêutica. Uma estratégia ampla é reduzir as ERO danosas ou fortalecer os antioxidantes, principalmente para prevenção ou para proteger tecidos saudáveis durante o tratamento. Outra é fazer o oposto nos tumores: inibir sistemas antioxidantes ou aumentar a produção de ERO até que as células cancerosas ultrapassem um limiar letal, especialmente quando combinado com radiação, drogas alvo ou imunoterapia. Uma terceira abordagem é não alterar os níveis de ERO, mas bloquear os interruptores sensíveis às ERO — proteínas de sinalização, enzimas metabólicas ou vias de morte — dos quais os tumores dependem. Em todas essas ideias corre o tema da personalização: diferentes cânceres apresentam diferentes “assinaturas redox”, então terapias futuras podem necessitar de exames de sangue ou tecido para dano oxidativo, capacidade antioxidante e genes relacionados às ERO para escolher o tratamento redox direcionado adequado para cada paciente.
O que isso significa para os pacientes
Em termos simples, este artigo argumenta que as ERO não são nem puramente ruins nem puramente boas; são ferramentas poderosas usadas pelas células e pelos cânceres. As células cancerosas tendem a operar mais próximas de um ponto de inflexão de estresse oxidativo do que as células saudáveis, o que pode criar uma janela terapêutica. No entanto, porque antioxidantes e pró-oxidantes podem tanto ajudar quanto prejudicar dependendo da dose, do momento e do tipo de tumor, o uso indiscriminado de suplementos ou drogas que aumentam ERO é arriscado. Os autores concluem que o futuro está em terapias e diagnósticos cuidadosamente projetados que leiam o estado redox de cada tumor e então nudgem as ERO e os sistemas antioxidantes o suficiente — seja para baixo, para proteger tecidos normais, ou para cima, para levar as células cancerosas além de seu ponto de ruptura.
Citação: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
Palavras-chave: espécies reativas de oxigênio, estresse oxidativo, metabolismo do câncer, terapia redox, microambiente tumoral