Clear Sky Science · pt
Antígeno nuclear exógeno 1 do vírus Epstein–Barr induz resistência tumoral dirigida por ADAR1 contra imunoterapia
Por que um vírus comum importa para o tratamento do câncer
Muitos cânceres hoje são tratados com drogas de imunoterapia que liberam o próprio sistema imunológico do corpo. Ainda assim, a maioria dos pacientes não se beneficia, porque seus tumores aprendem a se esconder do ataque imune. Este estudo revela como um vírus muito comum, o vírus Epstein–Barr (EBV), ajuda tumores a desligar defesas imunes e resistir a essas drogas potentes — e como um novo tipo de molécula projetada pode religar essas defesas.
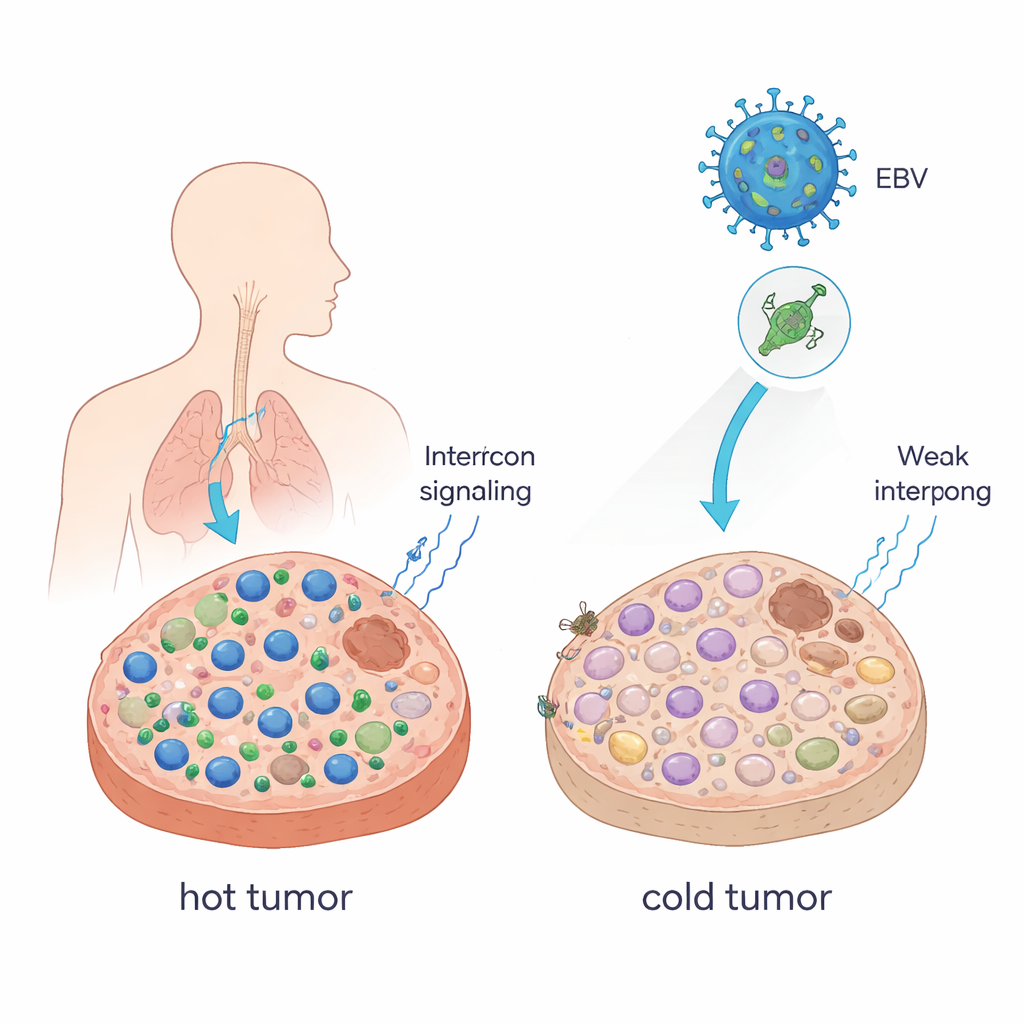
Transformando tumores “quentes” em “frios”
Médicos costumam descrever tumores como “quentes” quando estão cheios de células T que matam o câncer, e “frios” quando essas células são escassas. Tumores quentes geralmente respondem bem a drogas que bloqueiam pontos de verificação imune (ICB), como anticorpos anti–PD-1; tumores frios frequentemente não. Os autores demonstraram que uma única proteína do EBV, chamada EBNA1, pode empurrar tumores para esse estado mais frio e evasivo. Quando forçaram células tumorais de camundongos a produzir EBNA1 e as cultivaram em camundongos com sistema imune intacto, os tumores cresceram mais, continham menos células CD8+ T e células natural killer, e tinham mais macrófagos que suprimem o sistema imune. Sinais chamados interferons — mensageiros-chave que ajudam a mobilizar células imunes — também foram fortemente reduzidos. Em amostras de pacientes com carcinoma nasofaríngeo, um câncer fortemente ligado ao EBV, tumores que expressavam EBNA1 mostraram de forma semelhante menos células CD8+ T do que o tecido normal.
Um atalho viral para a maquinaria de controle de RNA da célula
Para entender como EBNA1 remodela o ambiente tumoral, os pesquisadores buscaram proteínas humanas que interajam fisicamente com ela. Eles se concentraram em uma proteína chamada IGF2BP3, que lê pequenas marcas químicas (m6A) em RNAs mensageiros e pode aumentar sua estabilidade ou tradução em proteína. EBNA1 ligou-se fortemente ao IGF2BP3 em vários tipos celulares, inclusive em células cancerosas positivas para EBV. Dados de tumores de pacientes mostraram que altos níveis de IGF2BP3 andavam de mãos dadas com atividade fraca de genes relacionados a interferon e menor infiltração de células T CD8+, sugerindo que essa aliança vírus-hospedeiro poderia abafar a imunidade antitumoral.
Potencializando um editor de RNA que silencia sinais de perigo
Análises mais profundas destacaram um alvo-chave dessa interação: ADAR1, uma enzima que edita RNA de fita dupla mudando certas letras “A” para “I”. Essa edição pode fazer com que RNA com aparência viral dentro das células pareça menos perigoso para sensores internos, reduzindo respostas de interferon. Os autores descobriram que EBNA1, IGF2BP3 e um fator de tradução chamado EIF4G1 formam um complexo tripartido sobre o mRNA de ADAR1. Esse complexo aumenta a marcação m6A, recruta a maquinaria de tradução e eleva seletivamente a produção da proteína ADAR1 sem aumentar seus níveis de RNA. Como resultado, células tumorais realizam mais edição de RNA em elementos genéticos repetidos localizados perto de genes relacionados a interferon. Essas edições reduzem o conjunto de RNA de fita dupla não editado que normalmente alertaria sensores como MDA5 e PKR, enfraquecendo a produção de interferon e ajudando os tumores a se esconderem do ataque imune.
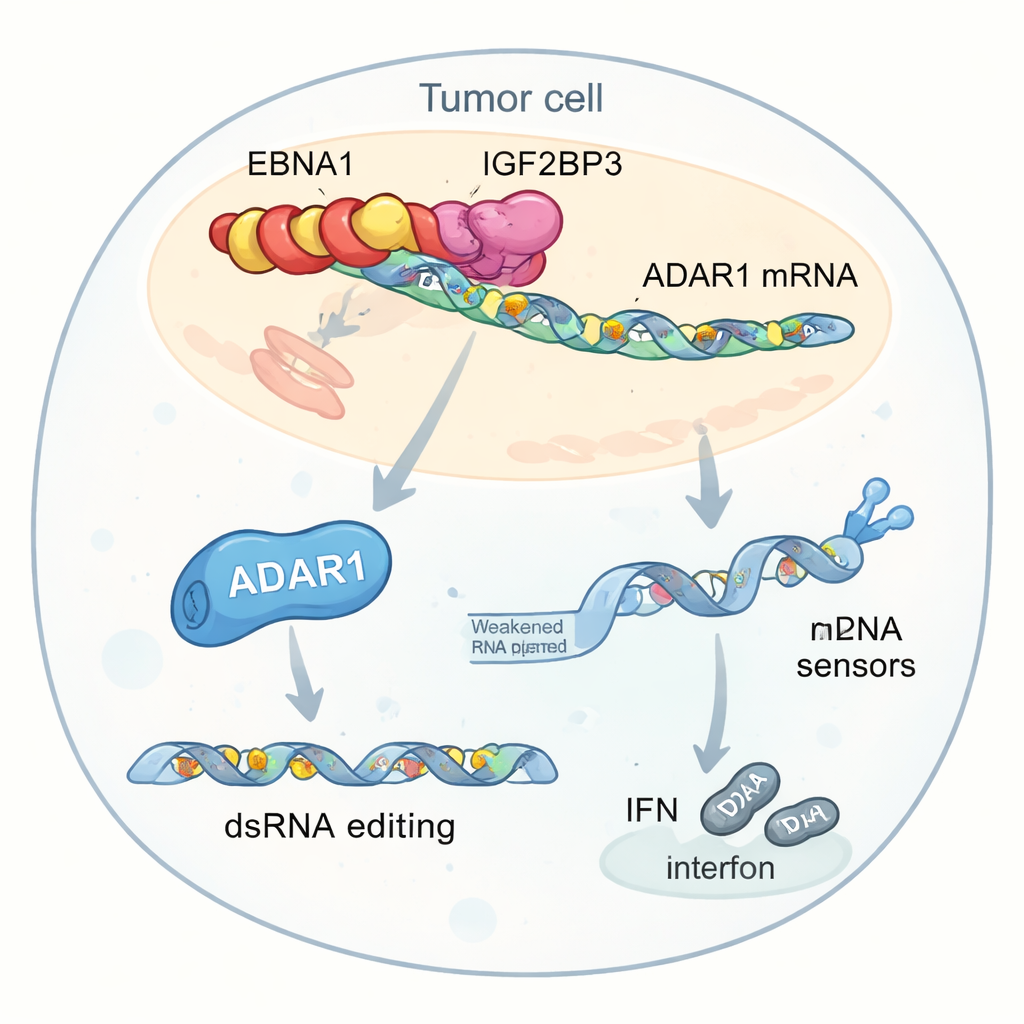
Menos interferon, imunoterapia mais fraca
Quando células tumorais que expressavam EBNA1 foram expostas a células T e anticorpos anti–PD-1 em laboratório, elas foram mais difíceis de matar do que células controle e liberaram menos interferon. Mesmo quando tratadas diretamente com interferon, células portadoras de EBNA1 foram menos sensíveis, e seus sensores internos de RNA foram menos ativados. Reduzir os níveis de ADAR1 reverteu parcialmente esses efeitos, restaurando a atividade dos sensores e a sinalização de interferon. Experimentos genéticos e de sequenciamento confirmaram que células que expressam EBNA1 apresentaram mais eventos de edição A-para-I em regiões específicas de RNA, particularmente após estimulação por interferon, apoiando a ideia de que o aumento viral de ADAR1 ajuda a neutralizar sinais de perigo que, de outra forma, desencadeariam respostas imunes fortes.
Um degrader projetado que reativa o ataque imune
A equipe então perguntou se remover EBNA1 dos tumores poderia restaurar sua vulnerabilidade à imunoterapia. Eles projetaram uma molécula PROTAC, EP-1215, que marca EBNA1 para destruição pelo sistema de descarte da própria célula. Em baixas doses, EP-1215 degradou eficientemente EBNA1 e reduziu os níveis da proteína ADAR1. Em experimentos com camundongos, EP-1215 sozinho teve impacto limitado em tumores positivos para EBNA1, e anti–PD-1 sozinho também foi fraco. Mas quando combinados, os dois tratamentos reduziram fortemente os tumores, aumentaram a infiltração de células T CD8+ e elevaram as células T produtoras de interferon. Em modelos de camundongos humanizados com células imunes humanas e tumores relacionados ao EBV, a combinação novamente superou os tratamentos individuais, sem toxicidade evidente ao fígado ou rins.
O que isso significa para o futuro do tratamento do câncer
Para não especialistas, a mensagem é que um vírus comum pode silenciosamente reconfigurar células cancerosas para atenuar sistemas internos de alarme, desligando sinais químicos que, de outra forma, atrairiam e ativariam células imunes. EBNA1 faz isso sequestrando um leitor de RNA do hospedeiro (IGF2BP3) e um fator de tradução (EIF4G1) para superproduzir o editor de RNA ADAR1, que edita as próprias estruturas de RNA que os sensores imunes foram construídos para reconhecer. Ao degradar EBNA1 com um PROTAC sob medida como o EP-1215, os autores foram capazes de restaurar esses sinais de perigo e tornar tumores resistentes novamente sensíveis às drogas de checkpoint existentes. Se estratégias semelhantes se mostrarem seguras e eficazes em humanos, direcionar ajudantes virais como EBNA1 pode oferecer uma nova maneira de converter tumores frios ligados ao EBV em alvos quentes que as imunoterapias modernas finalmente consigam atingir.
Citação: Liu, C., Sun, Z., Li, C. et al. Exogenous Epstein–Barr virus nuclear antigen 1 induces ADAR1-driven tumor resistance against immunotherapy. Sig Transduct Target Ther 11, 63 (2026). https://doi.org/10.1038/s41392-026-02574-y
Palavras-chave: Vírus Epstein-Barr, resistência à imunoterapia, ADAR1, edição de RNA, carcinoma nasofaríngeo