Clear Sky Science · pt
Mecanismo molecular da fusão de membrana dependente de colesterol na entrada do SARS-CoV-2
Por que o colesterol importa para um vírus respiratório
O vírus que causa a COVID-19, o SARS-CoV-2, entra em nossas células fundindo seu revestimento externo com as membranas das células hospedeiras. Este artigo investiga uma pergunta aparentemente simples, mas com grandes implicações: em que medida o colesterol — uma substância gordurosa mais conhecida por seu papel nas doenças cardíacas — influencia essa etapa de fusão? Os autores mostram que o colesterol na membrana viral não apenas altera a eficiência da infecção; ele na verdade ajuda a organizar as proteínas spike do vírus em plataformas de acoplamento potentes que facilitam a entrada e a tornam mais confiável.
Construindo um modelo mínimo de entrada viral
Para dissecar esse processo, os pesquisadores reconstruíram o encontro vírus–célula em um tubo de ensaio usando pequenas bolhas de gordura chamadas lipossomos. Um conjunto de lipossomos carregava a proteína spike do SARS-CoV-2 e representava a membrana viral; o outro carregava o receptor ACE2, imitando a superfície da célula hospedeira. Ao serem misturadas e ativadas por enzimas específicas que "cortam" a spike em sua forma pronta para fusão, essas membranas artificiais se fundiam, permitindo que um corante fluorescente se movesse de uma bolha para outra. Esse sistema simplificado permitiu que a equipe ajustasse com precisão a composição lipídica — incluindo os níveis de colesterol — em cada lado e observasse como a fusão ocorria passo a passo. 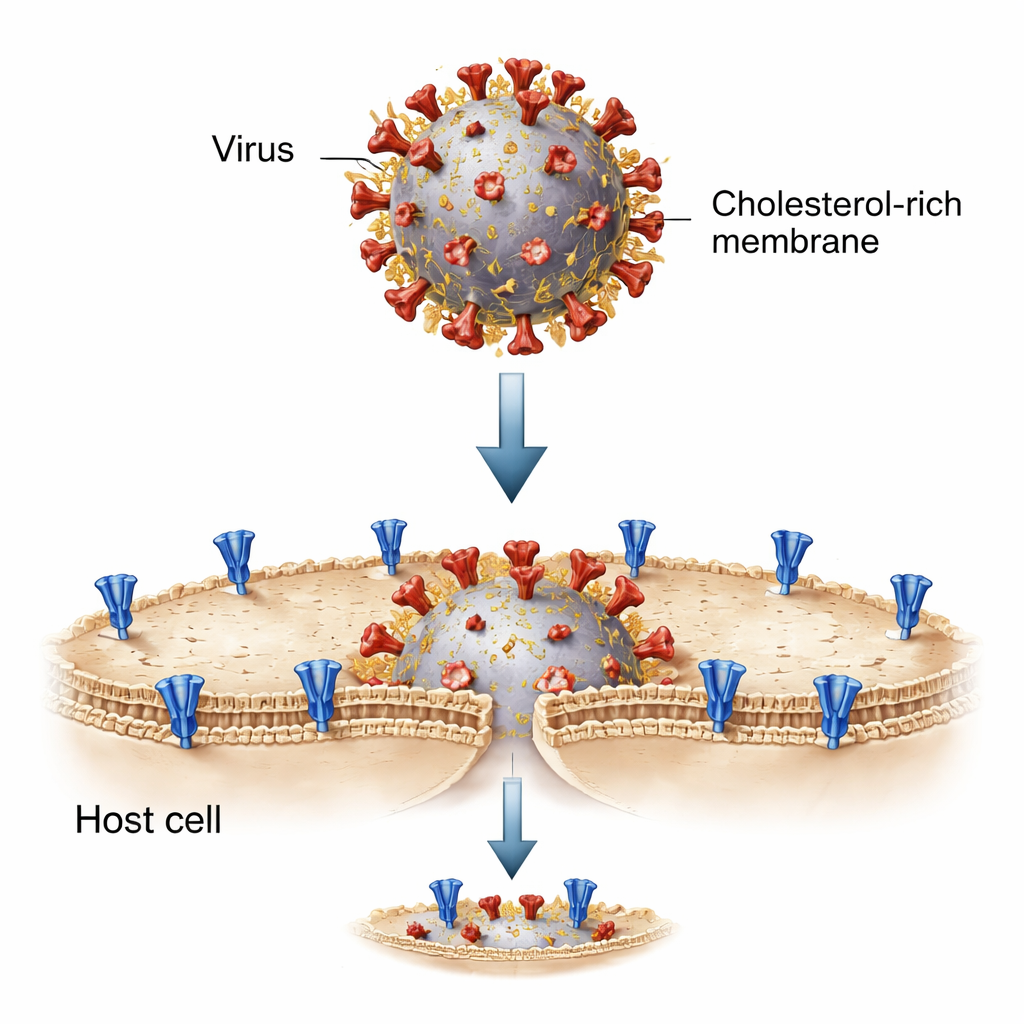
Colesterol aumenta o acoplamento mais do que a fusão
Ao variar a quantidade de colesterol, a equipe descobriu que adicionar colesterol à membrana que continha a spike tornava a fusão mais frequente, mas não do modo que se poderia esperar. Alto colesterol não alterou dramaticamente a chance de que duas membranas já acopladas realmente se fundissem. Em vez disso, aumentou fortemente a frequência com que vesículas com spike primeiro se acoplavam às vesículas com ACE2. Imagens de partícula única mostraram muito mais eventos de acoplamento bem-sucedidos quando a spike estava em membranas ricas em colesterol, enquanto a probabilidade de um par acoplado avançar até a fusão completa permaneceu aproximadamente constante. Curiosamente, enriquecer com colesterol o lado do ACE2 teve pouco benefício e, em níveis muito altos, até prejudicou a fusão, indicando o colesterol viral — e não o do hospedeiro — como o principal motor desse efeito.
De membranas modelo para células vivas
Os pesquisadores então investigaram se o mesmo padrão ocorria em células vivas. Eles engenheiraram células humanas para expressarem ou a spike ou o ACE2 e observaram a formação de grandes estruturas fundidas, os sincícios, quando as células eram misturadas. Remover o colesterol das células que expressavam a spike quase aboliu a formação de sincícios, enquanto restaurar o colesterol resgatou a fusão. Em experimentos paralelos com "pseudovírus" do SARS-CoV-2 (partículas virais inofensivas que utilizam a spike do coronavírus para entrar em células), retirar o colesterol da membrana viral reduziu fortemente a infecção, e reabastecê-lo aumentou a infecção de forma dependente da dose. Em contraste, alterar o colesterol apenas em células que expressavam ACE2 produziu pouca mudança. Em todos os ensaios, a mensagem foi consistente: o colesterol na membrana que contém a spike é essencial para uma entrada eficiente.
Agrupamentos de spike: a arma secreta do colesterol
Por que o colesterol do lado viral teria tanta importância? Imagens de alta resolução das membranas celulares revelaram que as proteínas spike tendem a formar aglomerados densos quando o colesterol é abundante, mas permanecem mais dispersas quando ele está esgotado. Medições de molécula única foram além, mostrando que esses aglomerados contêm mais cópias da spike em condições ricas em colesterol. Os autores atribuíram esse efeito a uma região rica em cisteínas (CRR) na extremidade da cauda da spike, dentro da membrana viral. Esse segmento é modificado por palmitoilação — um tipo de "âncora" lipídica que favorece domínios ricos em colesterol. Quando a equipe truncou a cauda da spike ou mutou todas as dez cisteínas para bloquear a palmitoilação, a spike deixou de se agrupar com o colesterol e o aumento de acoplamento e fusão dependente de colesterol desapareceu. 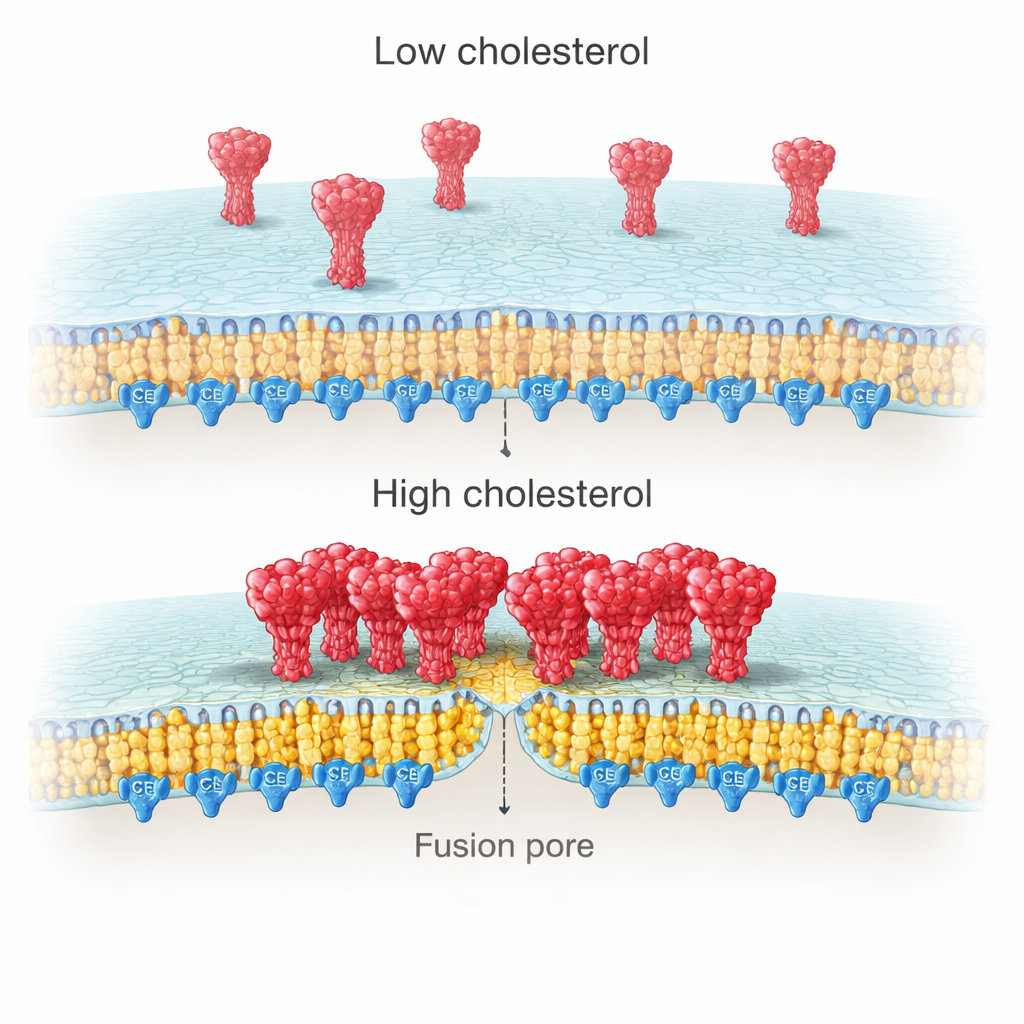
Como isso pode ajudar tratamentos futuros
Em termos simples, o estudo conclui que o colesterol transforma a membrana viral em uma plataforma de fusão ao reunir muitas proteínas spike em aglomerados compactos por meio de sua região de cauda palmitoilada e rica em cisteínas. Esses aglomerados acoplam-se de forma mais eficiente ao ACE2 nas células hospedeiras, aumentando as chances de que um dado encontro resulte em fusão e infecção bem-sucedidas. Para o público em geral, a conclusão-chave é que o colesterol não é apenas um componente passivo do revestimento viral; ele atua como organizador ativo da maquinaria spike. Isso torna a cauda sensível ao colesterol e rica em cisteínas da spike — e as enzimas que a palmitoilam — alvos promissores para estratégias antivirais amplas que poderiam funcionar contra diferentes variantes do coronavírus.
Citação: Li, W., Wu, M., Feng, S. et al. Molecular mechanism of cholesterol-dependent membrane fusion in SARS-CoV-2 entry. Sig Transduct Target Ther 11, 57 (2026). https://doi.org/10.1038/s41392-026-02573-z
Palavras-chave: colesterol, spike do SARS-CoV-2, fusão de membrana, entrada viral, palmitoilação