Clear Sky Science · pt
PKC-eta promove a metástase do câncer de mama regulando a via de sinalização Hippo–YAP
Por que esta pesquisa é importante
O câncer de mama triplo‑negativo (TNBC) é uma das formas mais perigosas de câncer de mama porque se espalha precocemente e não tem tratamentos direcionados. Este estudo revela como uma enzima específica dentro das células tumorais, chamada PKC‑eta (PKCη), funciona como um interruptor mestre que ajuda os tumores a se desprenderem, viajar pelo corpo e gerar novos focos tumorais. Ao entender esse interruptor, os pesquisadores também identificam um pequeno peptídeo natural capaz de desativá‑lo, apontando para uma possível nova abordagem terapêutica contra esta doença agressiva. 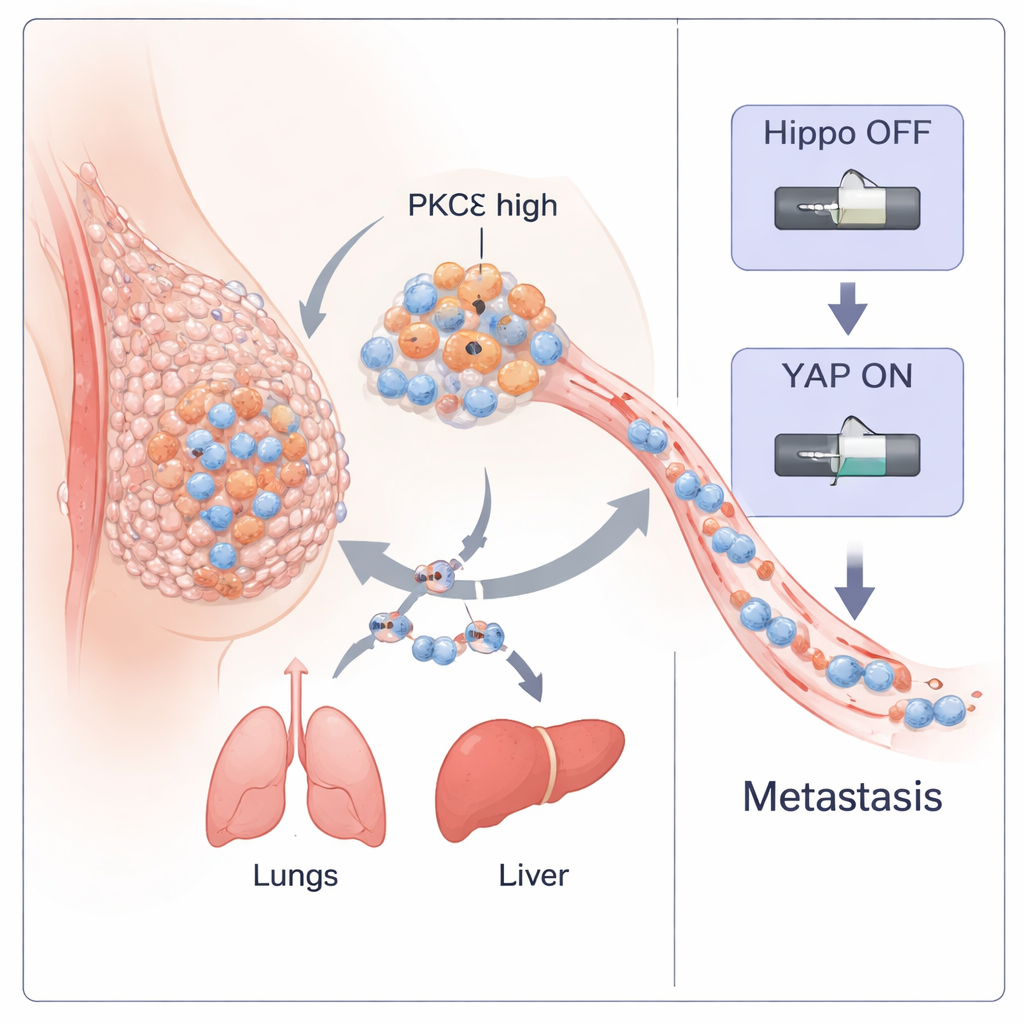
Um motor oculto em tumores mamários agressivos
A equipe começou minerando grandes conjuntos de dados de pacientes com câncer de mama. Eles descobriram que o gene que codifica a PKCη (PRKCH) está especialmente elevado em um subtipo de tumor conhecido como “claudin‑low”, que se sobrepõe fortemente ao TNBC e é rico em células com características de células‑tronco e alta mobilidade. Em múltiplas coortes de pacientes, tumores com altos níveis de PRKCH exibiram fortes assinaturas de transição epitélio‑mesenquimal (EMT) — um processo no qual células antes organizadas perdem suas aderências, mudam de forma e tornam‑se mais invasivas. Os níveis de PRKCH também foram maiores em amostras metastáticas do que nos tumores primários originais, e a coloração proteica de tecidos humanos de TNBC mostrou PKCη mais ativa, com localização perinuclear, em cânceres de grau mais alto e mais avançados. Em conjunto, esses achados sugerem que a PKCη está intimamente ligada à agressividade tumoral e à disseminação.
Do prato de laboratório ao camundongo: demonstrando que PKCη alimenta o espalhamento
Para testar causa e efeito, os pesquisadores usaram edição gênica CRISPR para remover a PKCη de duas linhas celulares de TNBC altamente metastáticas, uma de camundongo (4T1) e outra humana (MDA‑MB‑231). Sem PKCη, as células deslocaram‑se para um estado mais “epitelial”: aumentaram proteínas de adesão como E‑cadherina e EpCAM, e reduziram marcadores mesenquimais clássicos incluindo vimentina e N‑cadherina. Essas células deficientes em PKCη formaram menos e menores colônias, migraram e invadiram com menos eficiência, foram mais sensíveis à morte celular quando destacadas e mostraram uma queda acentuada em características de células‑tronco cancerígenas, incluindo menos células CD44high/CD24low e ALDH‑positivas e menor capacidade de formar esferas. Quando injetadas em camundongos, células sem PKCη produziram tumores primários menores e muito menos metástases para pulmões, fígado, cérebro e outros órgãos; os camundongos também sobreviveram por mais tempo. Restaurar a PKCη reverteu essas mudanças, confirmando que a enzima promove ativamente a progressão e a disseminação do TNBC.
Como a PKCη sequestra uma via de controle do crescimento
O estudo então aprofundou como a PKCη exerce esse poder promotor de metástase. Dados de pacientes revelaram que os níveis de PKCη sobem e descem em sincronia com YAP, uma potente proteína reguladora controlada pela via Hippo — um “freio de segurança” celular que normalmente restringe o crescimento. Altos níveis de PRKCH ou de YAP1 previam piores desfechos para os pacientes, e altos níveis de ambos juntos estavam ligados a uma sobrevida livre de metástase à distância particularmente ruim. Em células de TNBC, a remoção de PKCη reduziu os níveis totais de YAP e o deslocou do núcleo para o citoplasma, onde fica inativo. Experimentos bioquímicos mostraram que a PKCη se liga fisicamente à YAP e adiciona especificamente um grupo fosfato no sítio Ser128. Essa modificação estabiliza a YAP e facilita sua entrada no núcleo para ativar genes que impulsionam EMT, características de células‑tronco e metástase. Na ausência de PKCη, a YAP é fosforilada em outros sítios (Ser127 e Ser397) que a fazem ligar‑se às proteínas 14‑3‑3, ficar retida no citoplasma e, por fim, ser degradada. A PKCη também aumenta o PTEN — um inibidor natural da enzima AKT — mantendo assim a atividade de AKT baixa e suprimindo as quinases upstream da via Hippo que, de outra forma, inativariam a YAP. Dessa forma, a PKCη tanto ativa diretamente a YAP quanto indiretamente mantém o “freio” Hippo desligado. 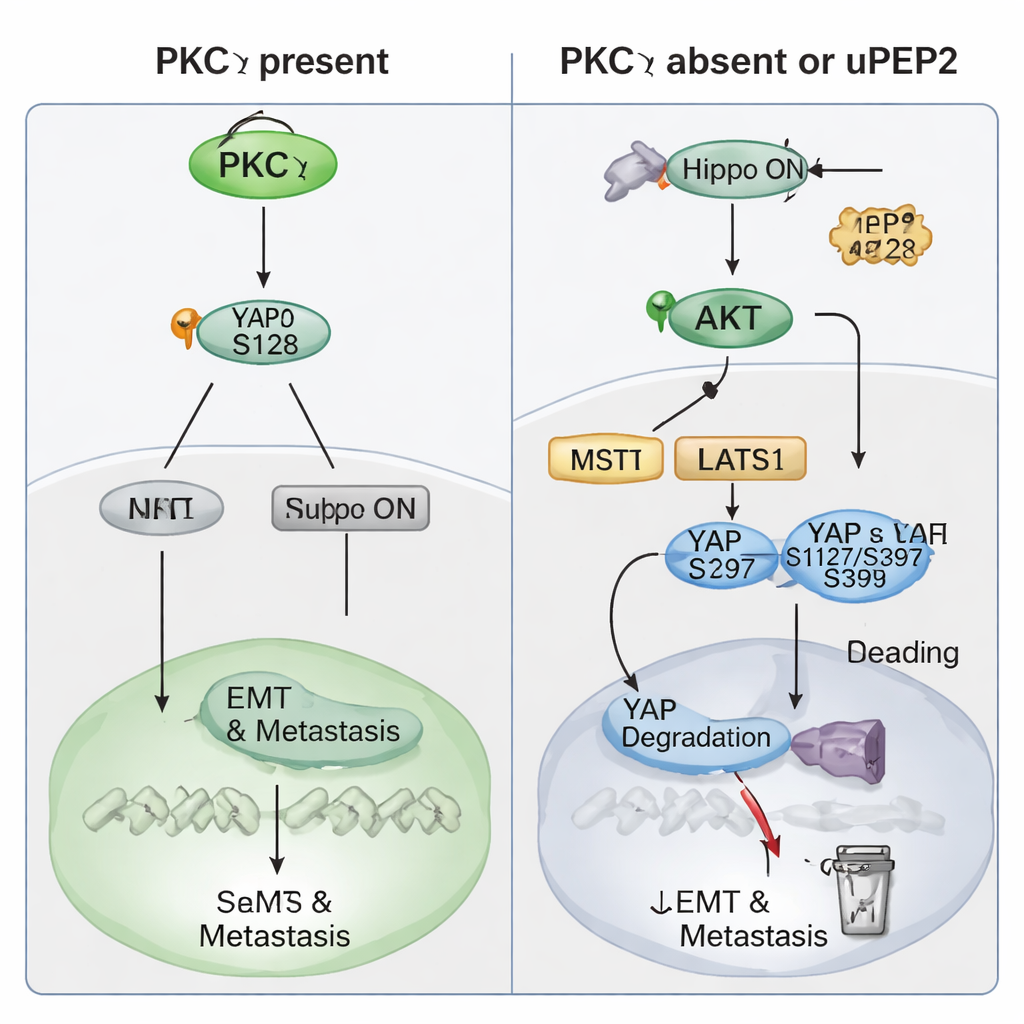
Um peptídeo minúsculo que desarma o interruptor do câncer
Curiosamente, o gene PKCη carrega um pequeno quadro de leitura aberto a montante (uORF) que codifica um micropeptídeo chamado uPEP2. Trabalhos anteriores mostraram que o uPEP2 pode se ligar e inibir a PKCη e enzimas relacionadas. Aqui, o tratamento de células de TNBC com uPEP2 sintético imitou os efeitos da deleção de PKCη: migração, invasão e comportamento com características de célula‑tronco diminuíram, marcadores de EMT mudaram para um perfil menos agressivo, e os níveis de YAP caíram enquanto suas marcas de fosforilação “desligadas” aumentaram. Em tumores de camundongo, o uPEP2 reduziu PKCη e YAP nos tumores primários, aumentou a inativação da YAP e esteve associado a menos micrometástases no fígado e nos pulmões. Mecanisticamente, o uPEP2 promove a degradação da PKCη, ligando novamente a via Hippo e forçando a YAP a permanecer no citoplasma e ser degradada.
O que isso significa para tratamentos futuros
Para um leitor leigo, a mensagem principal é que os pesquisadores identificaram a PKCη como uma peça central que ajuda os cânceres de mama mais agressivos a se desprenderem, se moverem e colonizarem órgãos distantes ao desativar um sistema natural de controle do crescimento e ativar o “acelerador” YAP. Ao eliminar a PKCη ou usar o pequeno peptídeo natural uPEP2 para degradá‑la, foi possível restaurar o freio Hippo, silenciar a YAP e reduzir largamente a metástase em modelos pré‑clínicos. Embora este trabalho ainda esteja em estágio experimental e tenha sido realizado em linhagens celulares e camundongos imunodeficientes, ele destaca a PKCη e sua interação com a YAP como alvos promissores para novas terapias contra o TNBC, e sugere que fármacos do tipo uPEP2 poderiam um dia ajudar a prevenir ou limitar a disseminação deste câncer de difícil tratamento.
Citação: Liju, V.B., Waidha, K., Muraleedharan, A. et al. PKC-eta promotes breast cancer metastasis by regulating the Hippo–YAP signaling pathway. Sig Transduct Target Ther 11, 58 (2026). https://doi.org/10.1038/s41392-026-02572-0
Palavras-chave: câncer de mama triplo-negativo, PKC-eta, via Hippo-YAP, transição epitélio-mesenquimal, metástase do câncer