Clear Sky Science · pt
Linfócitos T CD4+ citotóxicos: origem, funções biológicas, doenças e alvos terapêuticos
Quando células auxiliares viram assassinas
O sistema imune costuma ser descrito em papéis simples: algumas células detectam problemas, outras realizam a luta. Este artigo concentra-se em um grupo surpreendente que desfoca essa linha — os linfócitos T CD4 citotóxicos. Conhecidos por muito tempo principalmente como células “auxiliares” que coordenam as defesas, certos linfócitos CD4 podem, eles mesmos, tornar-se efetores armados. Entender como surgem essas células metamórficas, o que elas fazem e como contribuem para doenças como câncer, infecções virais, distúrbios autoimunes e doenças cardíacas pode abrir novas vias para tanto reforçar a imunidade quanto acalmar inflamações nocivas. 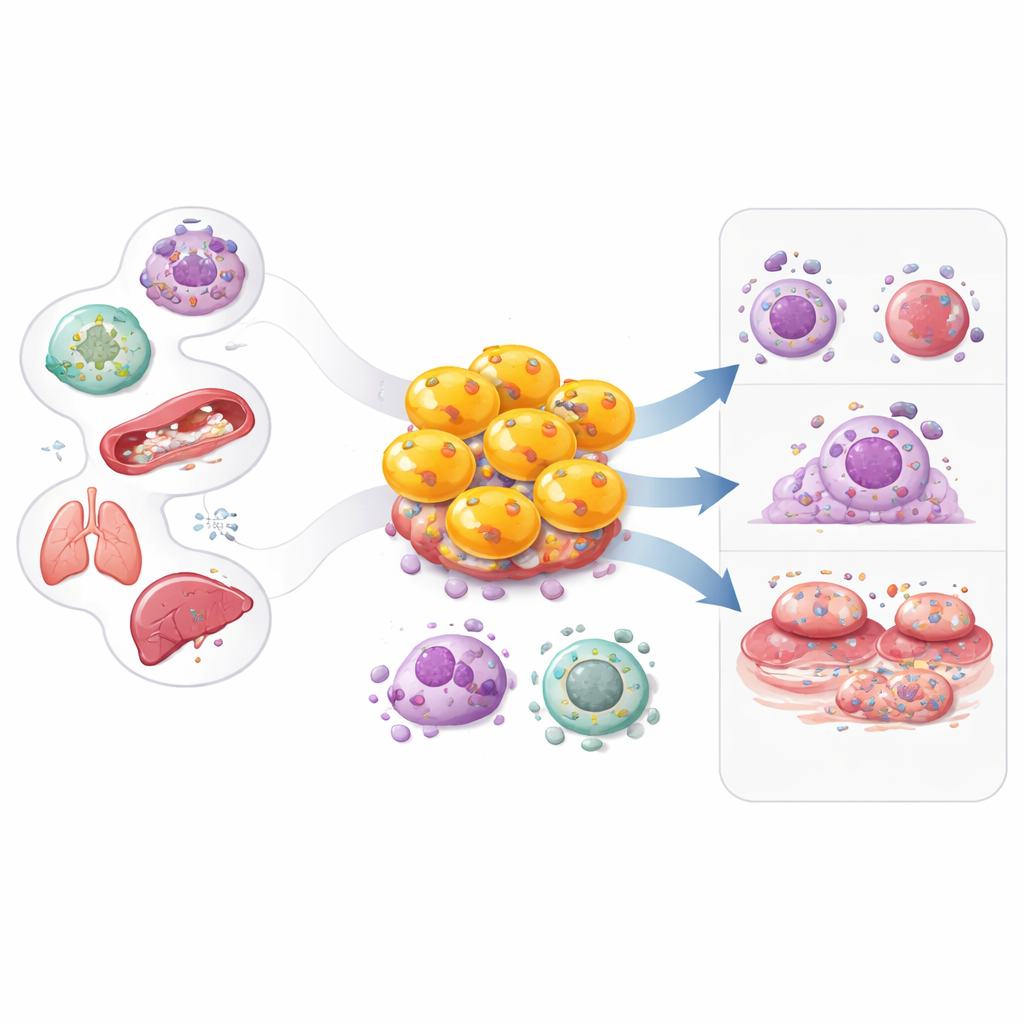
Como emergiu um defensor flexível
Trabalhos iniciais no final dos anos 1970 e na década de 1980 mostraram que uma fração dos linfócitos T CD4 poderia matar diretamente outras células que exibiam os sinais imunes certos, de modo parecido com os clássicos linfócitos T CD8 “assassinos”. A princípio, muitos cientistas descartaram essas observações como artefatos de cultura em laboratório. Nas décadas seguintes, modelos animais de influenza e estudos em pessoas com artrite reumatoide, doença cardíaca, infecções virais crônicas e câncer confirmaram que os linfócitos T CD4 citotóxicos são reais e clinicamente importantes. Ferramentas modernas, como citometria de fluxo e sequenciamento de RNA em célula única, mapearam desde então sua diversidade, revelando que essas células se expandem em infecções crônicas, tumores, envelhecimento e em várias doenças inflamatórias, onde podem persistir por longos períodos.
De onde vêm essas auxiliares assassinas
A revisão explica que os linfócitos T CD4 citotóxicos provavelmente surgem por dois caminhos principais. Uma ideia é que eles se assemelham em parte a células natural killer porque compartilham muitos dos mesmos receptores de superfície e moléculas citotóxicas, sugerindo uma via de desenvolvimento relacionada. Entretanto, evidências crescentes favorecem outra visão: a maioria dessas células começa como linfócitos T CD4 auxiliares comuns — especialmente células do tipo Th1 — que, sob exposição crônica a antígeno e sinais inflamatórios fortes, se “reprogramam” para um estado citotóxico terminalmente diferenciado. Essa mudança é controlada por uma rede de sinais externos (tais como interleucinas 2, 7 e 15) e interruptores internos (incluindo Runx3, T-bet, Eomes, Blimp-1 e Hobit) que juntos ativam genes para perfurina, granzimas e ligantes indutores de morte.
Como matam e moldam a inflamação
Funcionalmente, os linfócitos T CD4 citotóxicos atuam por duas rotas principais de ataque. Na via das grânulos, eles formam um contato estreito com a célula-alvo e liberam pacotes contendo perfurina e granzimas, que abrem furos e desencadeiam morte celular programada de dentro. Na via dos ligantes de morte, exibem na superfície moléculas como ligante Fas e TRAIL, que engajam receptores correspondentes na célula-alvo para lançar um programa interno de suicídio. Além da morte direta, essas células liberam mensageiros inflamatórios como interferon-gama, fator de necrose tumoral e fatores de crescimento que recrutam e ativam outras células imunes, remodelam vasos sanguíneos e alteram o comportamento do tecido local. Ao contrário das auxiliares clássicas, elas frequentemente resistem aos “freios” normais, como as células T reguladoras, e têm menor propensão à apoptose, permitindo que se acumulem em doenças crônicas. 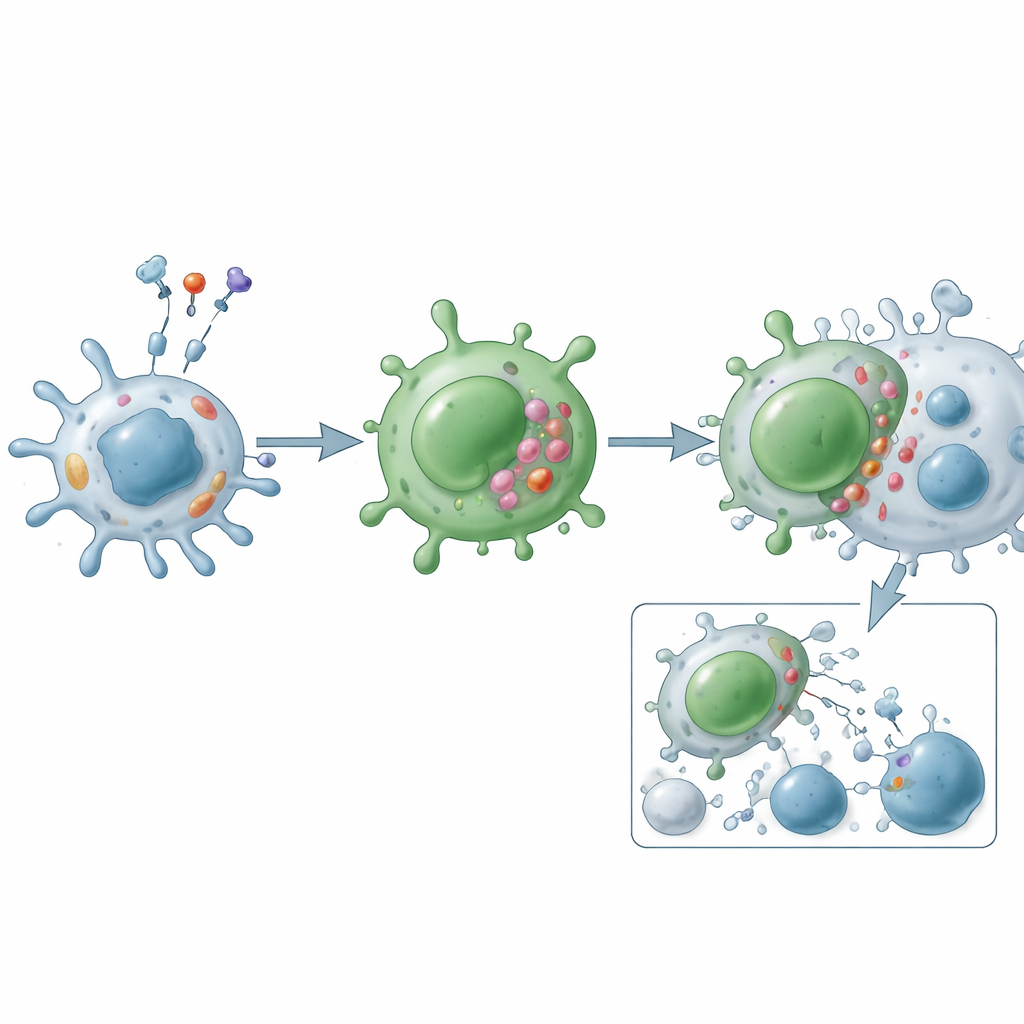
Aliadas em infecção e câncer, inimigas na autoimunidade e na doença cardíaca
Esse comportamento de dois gumes aparece em muitas condições. Em hepatite B crônica, HIV e COVID-19, os linfócitos T CD4 citotóxicos ajudam a controlar vírus quando os CD8 estão exauridos, e sua presença pode acompanhar melhor controle ou recuperação. Em tumores sólidos e neoplasias hematológicas, eles podem reconhecer diretamente células tumorais que exibem os marcadores imunes ou sinais de estresse adequados e podem melhorar respostas a imunoterapias, como inibidores de pontos de checagem e tratamentos com células CAR-T. Ao mesmo tempo, esses mesmos mecanismos podem causar dano: em lúpus, artrite reumatoide, doença inflamatória intestinal, doença arterial coronariana, fibrilação atrial, arterite de células gigantes e rejeição de transplante, linfócitos T CD4 citotóxicos expandidos infiltram tecidos, danificam vasos ou órgãos e amplificam inflamação de longa duração, frequentemente correlacionando-se com pior prognóstico.
Transformando uma ferramenta arriscada em terapia
Porque os linfócitos T CD4 citotóxicos podem ser protetores ou destrutivos, o artigo destaca estratégias terapêuticas emergentes que visam afinar, em vez de simplesmente erradicar, essa população. Uma abordagem é atenuar sua atividade prejudicial usando inibidores seletivos que miram receptores coestimuladores (como OX40 ou 4-1BB), citocinas inflamatórias, canais iônicos ou vias de sobrevivência. Outra é aproveitar seu poder citotóxico em terapias celulares adotivas, incluindo células T editadas geneticamente e CAR-T, nas quais células CD4 citotóxicas frequentemente apresentam maior persistência do que produtos compostos apenas por CD8. Uma terceira estratégia propõe redirecionar linfócitos CD4 citotóxicos de longa duração e específicos para vírus em direção a tumores usando vacinas ou peptídeos derivados de patógenos apresentados por células cancerosas. Juntas, essas linhas de trabalho colocam os linfócitos T CD4 citotóxicos não apenas como uma curiosidade biológica, mas como uma alavanca central para tratamentos futuros que poderiam aumentar de forma mais precisa a defesa contra infecções e câncer, ao mesmo tempo que reduzem a inflamação que danifica tecidos.
Uma nova alavanca para futuras terapias imunes
Para não especialistas, a mensagem-chave é que as células “auxiliares” CD4 são muito mais versáteis do que se pensava: algumas podem mudar para assassinas totalmente armadas que nos protegem de infecções persistentes e do câncer, mas também contribuem para autoimunidade, dano vascular e rejeição de transplantes. A revisão argumenta que aprender a rastrear essas células, prever quando irão ajudar ou prejudicar e ajustar seu comportamento com drogas ou terapias engenheadas pode remodelar o tratamento de uma ampla gama de doenças crônicas — da hepatite e HIV até artrite, colite, doença cardíaca e leucemia. Em vez de simplesmente aumentar ou diminuir o sistema imune, terapias futuras poderão trabalhar cada vez mais guiando tipos celulares poderosos, como os linfócitos T CD4 citotóxicos, para alvos benéficos e afastando-os de nossos próprios tecidos.
Citação: Lai, L., Ran, S., Li, Y. et al. Cytotoxic CD4+ T cells: origin, biological functions, diseases and therapeutic targets. Sig Transduct Target Ther 11, 85 (2026). https://doi.org/10.1038/s41392-025-02533-z
Palavras-chave: linfócitos T CD4 citotóxicos, plasticidade das células imunes, inflamação crônica, imunoterapia contra o câncer, doença autoimune