Clear Sky Science · pt
IFFO1 inibe o câncer de mama coordenando a fissão mitocondrial e a síntese de ácidos graxos via o eixo LaminA/C-PGC1α
Por que esta pesquisa importa
O câncer de mama continua sendo uma das principais causas de morte por câncer em mulheres, em grande parte porque alguns tumores seguem crescendo, espalhando-se e superando tratamentos disponíveis. Este estudo revela um “freio” celular antes subestimado, chamado IFFO1, que desacelera o câncer de mama ao domar dois motores centrais do crescimento tumoral: as usinas de energia da célula, as mitocôndrias, e a capacidade de produzir e armazenar lipídios. Compreender esse freio oferece uma nova perspectiva para terapias que podem ser eficazes em vários subtipos de câncer de mama.
Um guardião oculto dentro das células mamárias
Os pesquisadores começaram examinando amostras de 30 mulheres com câncer de mama, além de grandes bancos de dados públicos sobre câncer. Eles descobriram que os níveis da proteína IFFO1 eram consistentemente mais baixos no tecido tumoral do que no tecido mamário normal adjacente. Quanto mais avançado o estágio do câncer, menor a presença de IFFO1, e pacientes cujos tumores apresentavam níveis mais altos de IFFO1 tendiam a viver mais. Em células de câncer de mama cultivadas, forçar a produção extra de IFFO1 reduziu fortemente a capacidade de crescimento, divisão e migração — comportamentos necessários para que tumores se expandam e se disseminem. IFFO1 também atenuou um programa celular conhecido como transição epitélio–mesênquima, que ajuda células cancerosas a se desprenderem e invadirem outros tecidos.
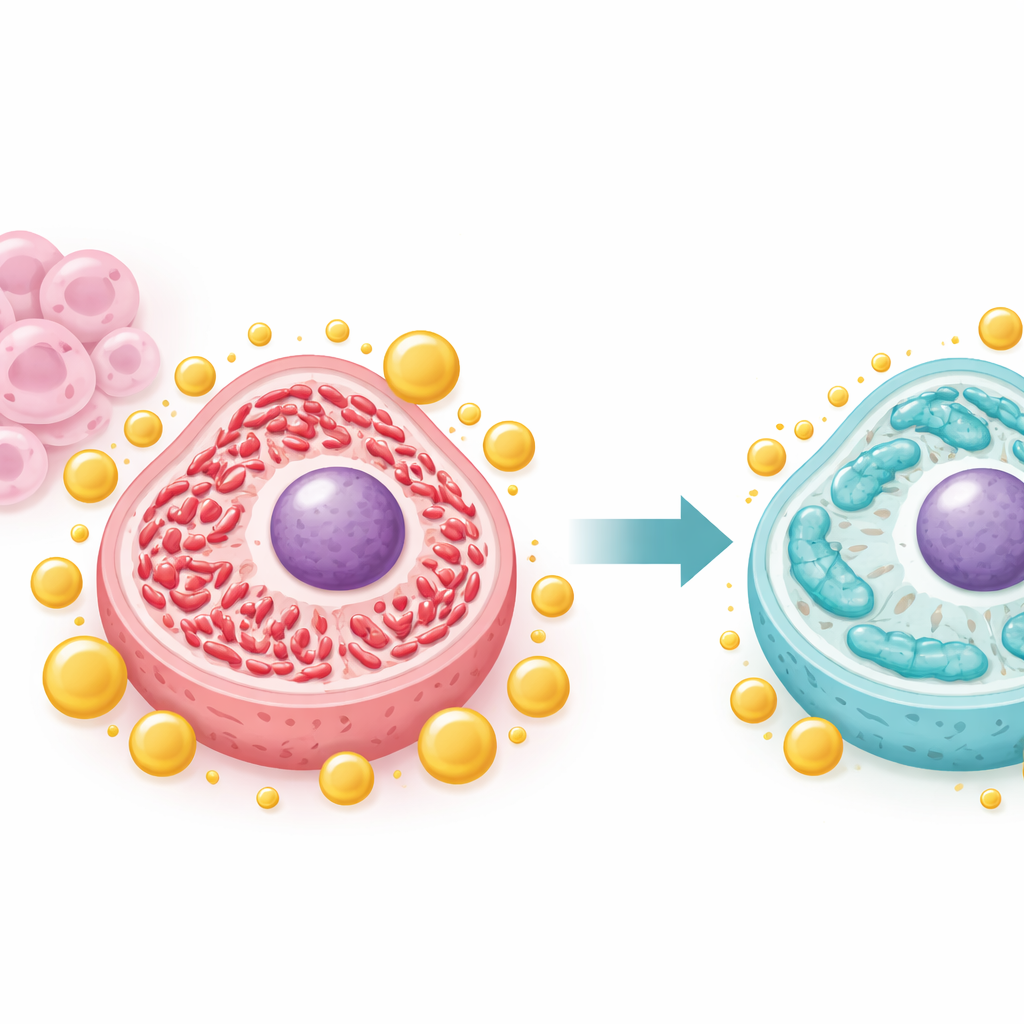
Acalmando usinas de energia hiperativas
Células cancerosas frequentemente remodelam suas mitocôndrias, as pequenas centrais elétricas das células, para alimentar o crescimento rápido. A equipe mostrou que IFFO1 desloca esse equilíbrio de um estado fortemente fragmentado de “fissão” para um estado mais alongado de “fusão”, geralmente associado a mitocôndrias mais saudáveis e estáveis. Quando IFFO1 estava em níveis elevados, proteínas-chave de fissão como Drp1 e Fis1 diminuíram, enquanto proteínas de fusão aumentaram. A microscopia revelou mitocôndrias mais longas e menos fragmentadas, e medidas de DNA mitocondrial e produção de energia caíram em relação aos níveis anormalmente altos observados em células agressivas. Essas mudanças sugerem que IFFO1 impede que as mitocôndrias entrem em uma configuração hiperativa que sustenta o crescimento tumoral descontrolado.
Cortando a linha de suprimento de lipídios
Tumores de crescimento rápido não precisam apenas de energia; também exigem um suprimento contínuo de lipídios para construir novas membranas e moléculas sinalizadoras. O estudo encontrou que IFFO1 também reprime esse acelerador metabólico. Em células com excesso de IFFO1, proteínas centrais da biossíntese de lipídios — incluindo FASN, SREBP‑1, SCD1 e outras — estavam reduzidas. Testes enzimáticos confirmaram menor atividade sintetizadora de lipídios, e ensaios químicos mostraram quedas em ácidos graxos livres, triglicerídeos e colesterol. Corantes de imagem que destacam reservas de gordura revelaram menos gotículas lipídicas e menor quantidade total de gordura neutra dentro das células cancerosas. Por outro lado, aumentar a proteína de fissão Drp1 teve o efeito oposto, impulsionando a produção de lipídios, enquanto silenciar Drp1 a reduziu — apoiando uma ligação direta entre a forma mitocondrial e o suprimento de lipídios no câncer.
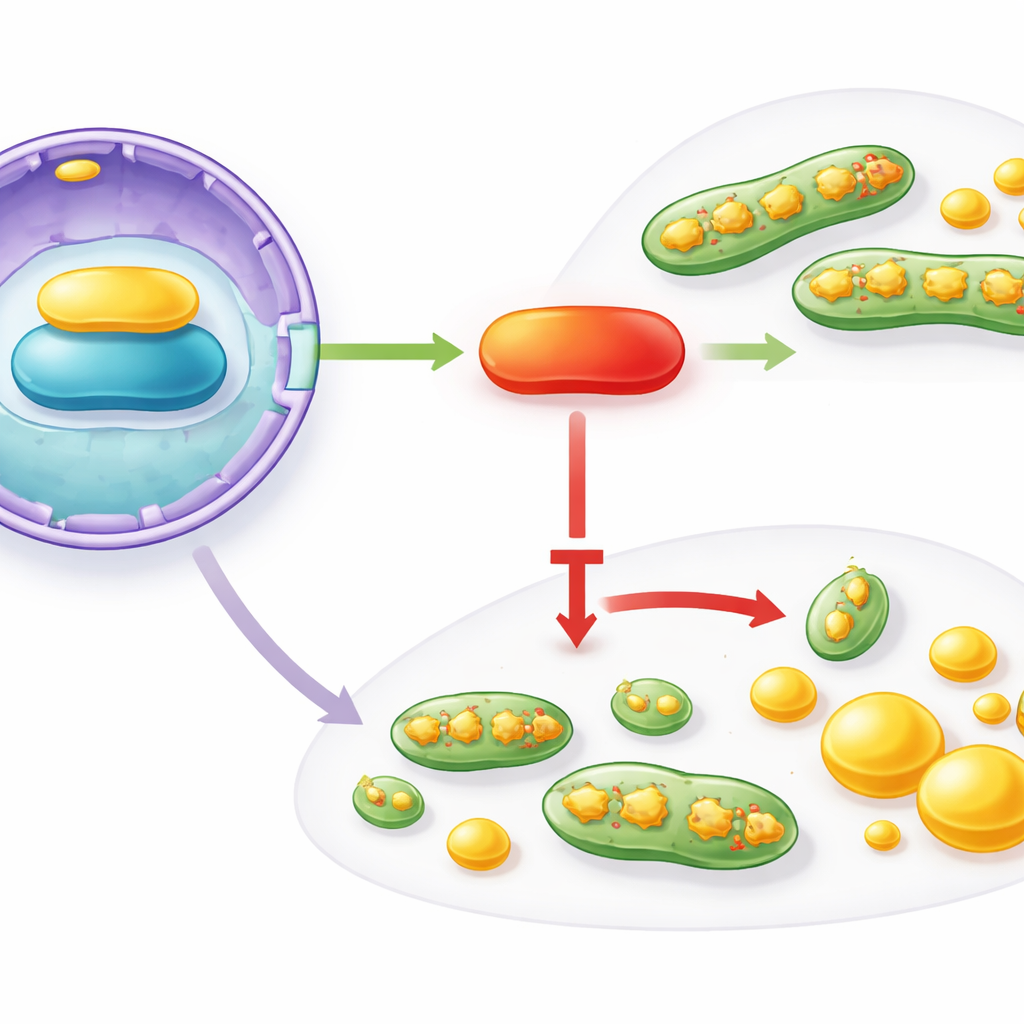
Uma cadeia de sinalização do núcleo às mitocôndrias
Como IFFO1 orquestra essas mudanças amplas? Os autores traçaram uma cadeia de interações que começa no núcleo da célula e termina nas mitocôndrias e na maquinaria de síntese de lipídios. IFFO1 se liga fisicamente a uma proteína estrutural do envelope nuclear chamada Lamin A/C, e aumenta seus níveis. Lamin A/C, por sua vez, apoia a atividade de PGC1α, um regulador mestre que supervisiona a saúde mitocondrial e o metabolismo. Em tecidos e células de câncer de mama, tanto Lamin A/C quanto PGC1α foram encontrados reduzidos, espelhando a perda de IFFO1. Quando os cientistas aumentaram IFFO1 artificialmente, Lamin A/C e PGC1α subiram, a fissão mitocondrial diminuiu e a síntese de lipídios enfraqueceu. A redução de Lamin A/C eliminou esses benefícios, mas restaurar PGC1α os recuperou, identificando um eixo funcional IFFO1 → Lamin A/C → PGC1α que limita as alterações mitocondriais e lipídicas promotoras de tumor.
Testando o freio em animais vivos
Para verificar se esses efeitos celulares se traduzem em tumores reais, a equipe implantou células humanas de câncer de mama com ou sem IFFO1 extra em camundongos. Tumores com IFFO1 reforçado cresceram mais lentamente, pesaram menos ao final do experimento e mostraram sinais reduzidos de acúmulo de gordura. Em um modelo separado, onde células cancerosas foram injetadas na corrente sanguínea para gerar metástases pulmonares, células que superproduziam IFFO1 formaram um número bem menor de nódulos tumorais nos pulmões. As análises teciduais desses camundongos refletiram os achados em cultura celular: maior Lamin A/C e PGC1α, menos fissão mitocondrial e menor síntese de lipídios.
O que isso significa para tratamentos futuros
Em conjunto, o trabalho apresenta IFFO1 como um supressor tumoral em múltiplos níveis que conecta o arcabouço estrutural da célula, suas usinas de energia e sua maquinaria de produção de lipídios. Ao estabilizar Lamin A/C e aumentar PGC1α, IFFO1 impede que as mitocôndrias se fragmentem excessivamente e corta a produção exagerada de lipídios da qual as células cancerosas dependem. Para leigos, a mensagem-chave é que esta proteína age como um freio interno tanto na energia quanto nos blocos de construção que alimentam o crescimento e a disseminação do câncer de mama. Drogas que aumentem os níveis de IFFO1 ou imitem seus efeitos sobre a via Lamin A/C–PGC1α podem, um dia, oferecer novas opções, especialmente para formas agressivas ou resistentes ao tratamento do câncer de mama.
Citação: Cai, H., He, J. IFFO1 inhibits breast cancer by coordinating mitochondrial fission and fatty acid synthesis via the LaminA/C-PGC1α axis. Oncogenesis 15, 16 (2026). https://doi.org/10.1038/s41389-026-00609-1
Palavras-chave: câncer de mama, dinâmica mitocondrial, síntese de ácidos graxos, metabolismo tumoral, via PGC1α