Clear Sky Science · pt
O controle oncogênico da síntese de nucleotídeos
Por que as células cancerosas se importam com os blocos de construção
O câncer costuma ser descrito como células que não param de se dividir. Mas para se copiarem, essas células precisam de um suprimento constante de pequenos blocos de construção chamados nucleotídeos, que compõem o DNA e o RNA e também alimentam muitos processos celulares. Esta revisão explica como genes que causam câncer reprogramam a química celular para manter alta a produção de nucleotídeos, como os tumores alternam entre diferentes formas de obter essas moléculas e como os médicos podem explorar essas estratégias com drogas antigas e novas.
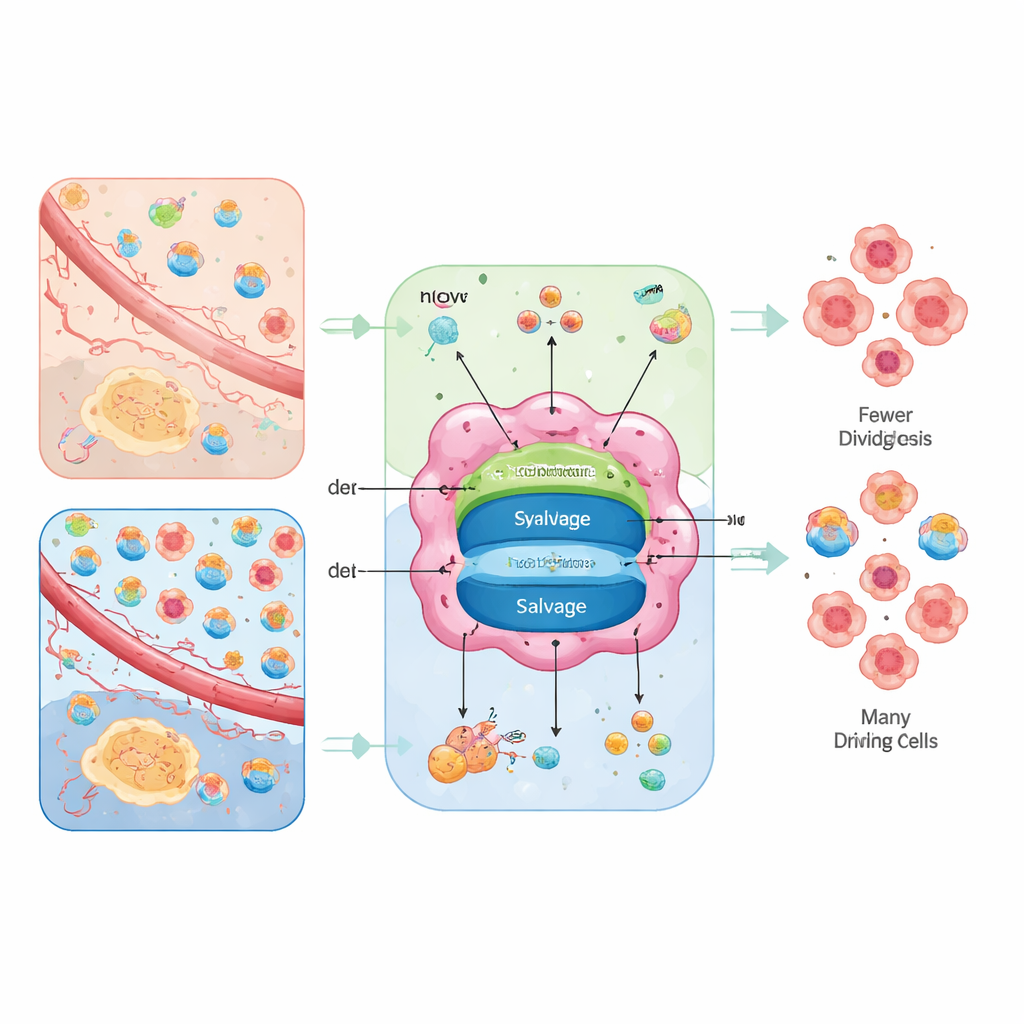
DuAS rotas para os mesmos blocos de construção
As células podem fabricar nucleotídeos do zero ou reciclá-los. A via “do zero”, chamada síntese de novo, monta os anéis a partir de nutrientes básicos como glicose, aminoácidos, dióxido de carbono e bicarbonato, usando reações em vários passos que consomem muita energia. A via de reciclagem, chamada salvage, aproveita bases e nucleosídeos degradados vindos do exterior ou de resíduos celulares e os reconverte em nucleotídeos utilizáveis a um custo energético muito menor. Os tumores usam ambas as opções, mas o equilíbrio entre elas depende do suprimento interno de energia e do que o tecido circundante fornece.
Como o microambiente tumoral orienta a escolha
Os autores enquadram o fornecimento de nucleotídeos como um problema de “roteamento moldado pelo ambiente”. Em regiões mal nutridas, onde aminoácidos estão presentes mas nucleosídeos livres são escassos, as células cancerosas dependem fortemente das vias de novo e ficam vulneráveis a drogas que bloqueiam essas etapas. Em regiões melhor perfundidas, onde o sangue entrega abundância de nucleosídeos ou onde as mitocôndrias estão fracas, os tumores podem depender mais do salvage, tornando‑se sensíveis a bloqueadores de transportadores que impedem a captação de nucleosídeos. Quando ambas as opções estão disponíveis, os tumores mostram flexibilidade metabólica e podem escapar de drogas isoladas; quando ambas estão fechadas, as células travam a replicação do DNA, acumulam danos e podem morrer ou se diferenciar em estados mais maduros e menos agressivos.
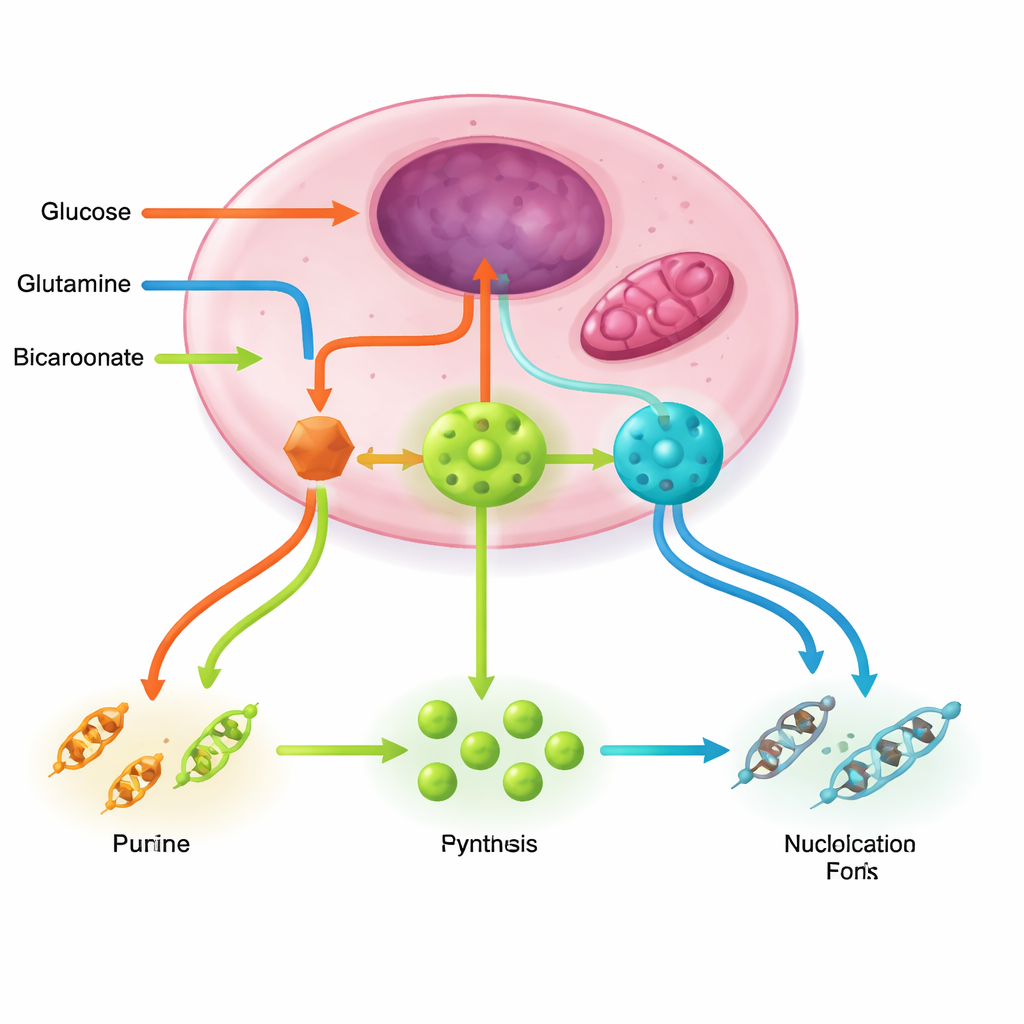
Linhas de suporte ocultas que alimentam o suprimento de nucleotídeos
Manter as “fábricas” de nucleotídeos em funcionamento requer vários circuitos de apoio. A via das pentoses fornece a espinha de açúcar e poder redutor; glutamina e o ciclo energético nas mitocôndrias fornecem nitrogênio e aspartato; a química da serina, glicina e folato doa unidades de um carbono que completam os anéis; o bicarbonato traz carbonos essenciais. Motoristas do câncer como PI3K–AKT–mTORC1, RAS–MAPK e MYC intensificam essas vias em conjunto, aumentam enzimas chave e até montam complexos multi‑enzimáticos que canalizam intermediários instáveis com eficiência. Em contraste, sensores de estresse como LKB1–AMPK e p53 normalmente atuam como freios, reduzindo a produção de nucleotídeos quando a energia ou a integridade do DNA estão ameaçadas — freios que muitos tumores desativam.
Quimioterapia antiga, nova lógica metabólica
Porque células de crescimento rápido dependem tanto de nucleotídeos, algumas das primeiras quimioterapias miraram essa fragilidade. Drogas clássicas como metotrexato, 5‑fluorouracil, citarabina, gemcitabina e vários análogos de purina bloqueiam o uso de folato, inibem enzimas específicas ou se passam por blocos de construção defeituosos que envenenam DNA e RNA. A revisão reexamina esses fármacos pela ótica do modelo de roteamento, explicando por que efeitos colaterais e resistência são comuns: tecidos não cancerosos também precisam de nucleotídeos, e os tumores frequentemente conseguem redirecionar o fluxo pela via de salvage ou por rotas paralelas quando um ponto é bloqueado.
Estratégias de nova geração e questões em aberto
Abordagens mais recentes buscam ser mais seletivas ao atingir as peças da rede com maior viés cancerígeno. Fármacos experimentais estão sendo desenvolvidos contra enzimas mitocondriais de um carbono como MTHFD2, a enzima pirimidina DHODH e enzimas de purina como IMPDH e PAICS, muitas vezes em combinações que também bloqueiam transportadores de salvage. Os autores propõem marcadores práticos — como níveis de transportadores, densidade vascular, aptidão mitocondrial e expressão de enzimas metabólicas específicas — para decidir quais tumores dependem mais de de novo ou do salvage e para combinar pacientes com terapias direcionadas às vias. Olhando adiante, destacam perguntas-chave, incluindo como essas rotas mudam no espaço e no tempo dentro de tumores reais, como células imunes e estromais vizinhas moldam a disponibilidade de nucleotídeos e como desenhar esquemas de tratamento toleráveis que explorem o estresse de replicação sem sobrecarregar tecidos normais. Em conjunto, este trabalho argumenta que entender e direcionar o metabolismo de nucleotídeos pode transformar um requisito básico da divisão celular em uma alavanca poderosa e personalizada contra o câncer.
Citação: Vidal-Cruchez, O., Ben-Sahra, I. The oncogenic control of nucleotide synthesis. Oncogenesis 15, 17 (2026). https://doi.org/10.1038/s41389-026-00608-2
Palavras-chave: metabolismo de nucleotídeos, metabolismo do câncer, síntese de novo, vias de reciclagem, terapias metabólicas