Clear Sky Science · pt
Perfilagem transcriptômica de células tumorais e hospedeiras co-cultivadas identifica a hipóxia como motor do efeito antiproliferativo das células do músculo esquelético sobre células cancerosas
Por que alguns tecidos resistem à disseminação do câncer
O câncer torna-se geralmente fatal quando células tumorais escapam do sítio original e se instalam em órgãos distantes. Curiosamente, alguns tecidos, como os pulmões, são locais frequentes de colonização, enquanto outros, como o músculo esquelético, quase nunca são invadidos apesar de representarem grande parte do peso corporal. Este estudo faz uma pergunta simples, mas importante para pacientes e médicos: o que há no músculo que o torna um ambiente tão pobre para o crescimento de células cancerosas, e compreender essa defesa natural poderia mudar a forma como pensamos em tratar a metástase?
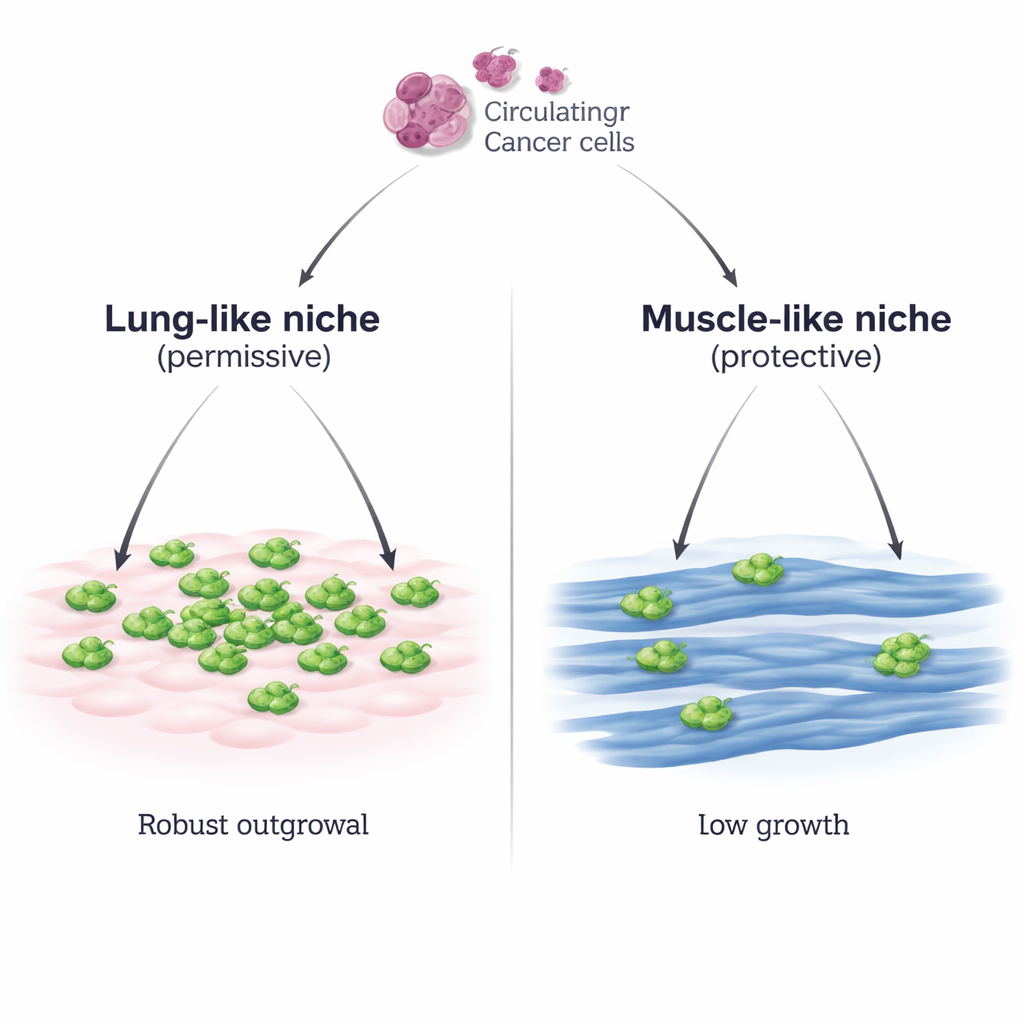
Dois bairros para células tumorais em trânsito
Os pesquisadores construíram um sistema de laboratório controlado que imita dois bairros diferentes que uma célula de câncer de mama pode encontrar: um ambiente semelhante ao pulmão formado por células do tecido conjuntivo pulmonar (MLg) e um ambiente semelhante ao músculo composto por fibras musculares esqueléticas maduras (miotubos C2C12). Eles colocaram células de câncer de mama de camundongo sobre cada camada e observaram o que acontecia. Nas células semelhantes às do pulmão, as células cancerosas aderiram bem e depois se multiplicaram rapidamente, formando manchas densas. Nas células musculares, elas aderiram igualmente bem, mas seu crescimento permaneceu escasso e lento, mesmo quando o número inicial de células cancerosas foi muito aumentado ou quando foi usada uma segunda linhagem de câncer de mama. Uma linhagem separada de músculo esquelético (Sol8) mostrou a mesma capacidade de conter o crescimento tumoral, enfatizando que essa é uma propriedade geral das células musculares e não uma peculiaridade de um tipo celular.
Como células tumorais e hospedeiras redesenham sua atividade
Para entender o que ocorria dentro das células, a equipe isolou as células tumorais e as células hospedeiras dessas culturas mistas e sequenciou seu RNA, um indicador de quais genes estão ativados ou desativados. As células cancerosas sobre fibras musculares sofreram mudanças muito mais extensas na atividade gênica do que aquelas crescendo sobre células pulmonares, sugerindo que o ambiente muscular as força a se adaptar fortemente. No ambiente muscular, as células tumorais ativaram programas ligados a características semelhantes às do músculo, ao processamento de energia e, surpreendentemente, respostas a baixo oxigênio (hipóxia). Ao mesmo tempo, os programas gênicos usuais que impulsionam a rápida divisão celular foram reduzidos. Em contraste, as células cancerosas sobre células pulmonares mantiveram um perfil fortemente focado no crescimento e precisaram de muito menos reprogramação, consistente com a ideia de que o nicho semelhante ao pulmão é permissivo e fácil de ser explorado por células tumorais.
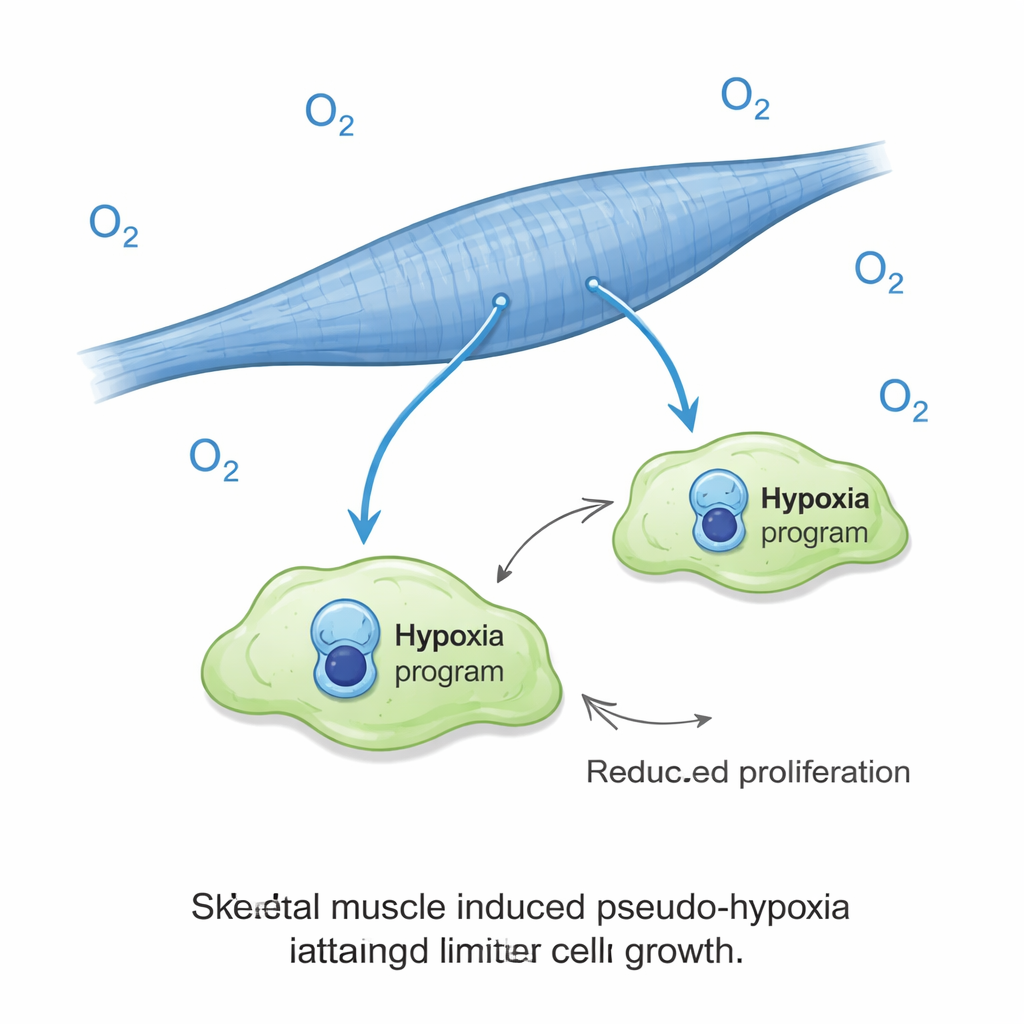
Um papel surpreendente para sinais de baixo oxigênio
Uma das descobertas mais marcantes foi que as células tumorais sobre fibras musculares ativaram uma assinatura gênica semelhante à de hipóxia, embora tenham sido cultivadas sob níveis normais de oxigênio. Na maioria dos tumores, a hipóxia é um mau sinal, geralmente associada a comportamento agressivo e prognóstico ruim. Aqui, ela se associou ao oposto: crescimento reduzido. Os cientistas então expuseram as culturas a baixo oxigênio verdadeiro e descobriram que isso quase eliminou a expansão de células cancerosas no ambiente muscular, enquanto na verdade aumentava o crescimento nas culturas semelhantes ao pulmão. Em outras palavras, o mesmo sinal que normalmente ajuda tumores a prosperar tornou-se um freio quando as células cancerosas estavam em um ambiente muscular. Esse efeito do oxigênio não parece ser explicado por mudanças simples em lactato, acidez ou disponibilidade de açúcar no meio de cultura.
Mais do que apenas fatores secretados
A equipe também testou se substâncias solúveis liberadas pelas células musculares poderiam explicar seu efeito protetor. Adicionar lactato extra, alterar a acidez, mudar os níveis de glicose ou cultivar células cancerosas em meio que previamente tinha sido usado por células musculares não reproduziu a forte supressão observada nas co-culturas em contato direto. Isso sugere que o contato físico próximo, ou sinais de muito curto alcance na superfície celular, são fundamentais para a forma como as células musculares empurram as células cancerosas para um estado de baixo crescimento, possivelmente dormente. Interessantemente, as próprias células musculares permaneceram relativamente estáveis em sua atividade gênica ao enfrentar o câncer, enquanto as células pulmonares foram mais facilmente reprogramadas, destacando o músculo como um tecido robusto e “resistente à metástase”.
O que isso significa para pacientes e terapias
No conjunto, o estudo revela que o músculo esquelético age como um habitat hostil que força as células cancerosas a um modo semelhante à hipóxia e de baixa proliferação, mesmo quando há oxigênio em abundância. Isso ajuda a explicar por que o músculo é um local tão raro de metástase. Também oferece uma mensagem de cautela para o desenvolvimento de fármacos: terapias projetadas para bloquear a sinalização de hipóxia por todo o corpo podem, inadvertidamente, enfraquecer essa defesa natural baseada no músculo, facilitando o crescimento de células cancerosas onde normalmente não o fariam. Entender e preservar, ou mesmo imitar, as características protetoras do tecido muscular pode abrir novas vias para prevenir ou controlar a doença metastática.
Citação: Aunan, A., Claeyssen, C., Abdelhalim, M. et al. Transcriptomic profiling of co-cultured cancer-host cells identifies hypoxia as a driver of the skeletal muscle cell’s anti-proliferative effect on cancer cells. Oncogenesis 15, 7 (2026). https://doi.org/10.1038/s41389-026-00601-9
Palavras-chave: metástase do câncer, músculo esquelético, hipóxia, microambiente tumoral, dormência do câncer