Clear Sky Science · pt
Mutaçãoes genéticas comuns em 103 linhagens celulares autenticadas de câncer colorretal
Por que essas linhagens celulares de câncer importam
O câncer colorretal é um dos tipos de câncer mais comuns no mundo, e grande parte do que sabemos sobre seu comportamento e tratamento vem de estudos em linhagens celulares cultivadas em laboratório. Mas esses modelos podem derivar e mudar ao longo do tempo. Este estudo verificou e catalogou cuidadosamente 103 linhagens de câncer colorretal amplamente usadas, mapeando mutações gênicas chave que impulsionam o crescimento tumoral. O resultado é um “guia de campo” detalhado que ajuda os pesquisadores a escolher o modelo certo para a pergunta certa, com o objetivo final de aumentar a probabilidade de que descobertas feitas em laboratório beneficiem pacientes no futuro.
Um catálogo de modelos de câncer
Os pesquisadores reuniram 103 linhagens celulares de câncer colorretal que, em conjunto, espelham os principais subtipos genéticos observados em pacientes. A maioria provinha de tumores primários do cólon ou reto, e o restante de metástases. A equipe primeiro verificou se cada linhagem era realmente o que dizia ser, usando marcadores de DNA semelhantes a impressões digitais chamados repetições curtas em tandem (short tandem repeats). Em seguida, utilizaram sequenciamento direcionado em profundidade, lendo trechos selecionados de DNA em média 575 vezes, para examinar 20 genes conhecidos por sua importância no câncer colorretal. Essa alta profundidade permitiu detectar até mutações relativamente raras dentro de uma população celular e estimar quão comuns eram essas mutações entre as células de uma determinada linha.
Diferentes caminhos para o caos genético
Os cânceres colorretais podem seguir rotas genéticas distintas em seu desenvolvimento. Cerca de quatro em cada cinco tumores apresentam instabilidade cromossômica, com grandes trechos de DNA ganhos ou perdidos. Outros são “hipermutados”, acumulando muitas pequenas alterações no DNA. Este estudo capturou ambos os padrões. Dezesseis linhagens apresentaram instabilidade de microssatélites, uma forma de hipermutação causada por falha no reparo de incompatibilidades do DNA, levando a inserções e deleções pequenas frequentes. Outras cinco tinham defeitos no gene de prova e correção do DNA POLE, gerando uma grande carga de mudanças de uma única letra no DNA. As linhagens não-hipermutadas restantes tinham menos mutações, mas mudanças mais frequentes em grande escala no número de cópias de DNA. Essas assinaturas distintas se assemelharam estreitamente às observadas em tumores reais de pacientes.
Genes condutores chave e combinações perigosas
Entre os 20 genes pesquisados, os padrões de mutação corresponderam a grandes estudos clínicos de câncer colorretal. Genes supressores tumorais como APC, TP53 e SMAD4 foram frequentemente atingidos por mutações truncantes que rompem a proteína, enquanto genes clássicos promotores de câncer como KRAS e BRAF apresentaram com mais frequência mudanças de um único aminoácido que ativam vias de sinalização. Linhagens não-hipermutadas tendiam a carregar uma maior parcela de mutações claramente deletérias, ou patogênicas, presentes na maioria ou em todas as células da cultura. Em contraste, as linhagens hipermutadas exibiam muitas mudanças “passageiras” extras e mais mutações subclonais que aparecem apenas em uma fração das células, refletindo evolução contínua na placa de cultura.
Padrões ocultos na interação entre genes
Ao observar quais mutações tendem a aparecer juntas ou a se evitar, os cientistas puderam identificar combinações genéticas associadas a doença particularmente agressiva. Por exemplo, a mutação de hotspot comum BRAF p.V600 raramente coocorreu com mutações em KRAS ou NRAS, mas em algumas linhagens apareceu ao lado de mutações truncantes em APC, evocando um subtipo de prognóstico ruim observado em pacientes. Muitas linhagens apresentaram triplas alterações em APC, TP53 e genes RAS, outro marcador de tumores de alto risco. O estudo também revelou um padrão distintivo de “duplo impacto” em APC: duas mutações truncantes posicionadas de modo que ao menos uma região de ligação à β-catenina permanece, consistente com um nível “na medida certa” de ativação da via WNT que favorece o crescimento tumoral. A análise do número de cópias mostrou ampliações frequentes de genes relacionados ao crescimento como MYC e EGFR, e perda de cópias inteiras de genes supressores tumorais, especialmente em linhagens não-hipermutadas.
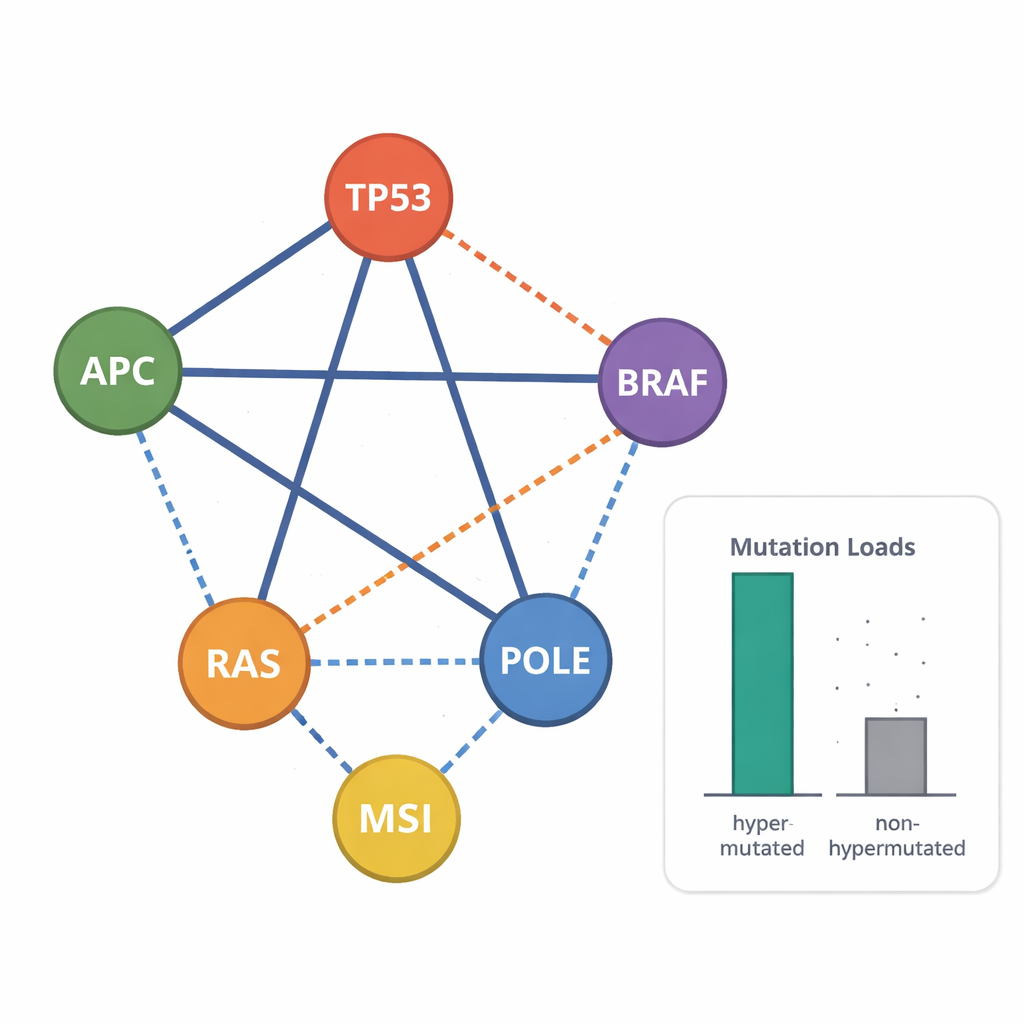
O que isso significa para pesquisas futuras
Para cientistas que planejam experimentos, a mensagem é que nem todas as linhagens celulares de câncer colorretal são iguais. Modelos hipermutados são geneticamente mais complexos e podem conter muitas alterações de baixo nível que diluem o impacto de uma única mutação. Linhagens não-hipermutadas, por outro lado, tendem a carregar alterações condutoras menos numerosas, porém mais fortes e mais uniformes. Ao fornecer um mapa cuidadosamente validado de quais genes estão alterados, como estão alterados e quão comuns são essas mutações em cada cultura, este trabalho capacita os pesquisadores a escolher os modelos mais apropriados para testar drogas, investigar a biologia e desenvolver novas abordagens direcionadas ou imunoterapias para o câncer colorretal.
Citação: Kranjec, C., Eilertsen, I.A., Nunes, L. et al. Common gene mutations in 103 authenticated colorectal cancer cell lines. Oncogenesis 15, 8 (2026). https://doi.org/10.1038/s41389-026-00599-0
Palavras-chave: câncer colorretal, linhagens celulares de câncer, mutações genéticas, subtipos tumorais, oncologia de precisão