Clear Sky Science · pt
Reorganização do citoesqueleto induzida por uma nova fusão de queratinas K6-K14 promove propriedades de célula-tronco do câncer e plasticidade celular via seleção cGAS-STING
Como células cancerosas que mudam de forma ludibriam seu entorno
Células cancerosas não apenas crescem de maneira descontrolada; elas também aprendem a dobrar e torcer seu próprio “esqueleto” interno para sobreviver, esconder-se e se espalhar. Este estudo revela como uma falha estrutural específica dentro de células de câncer de cabeça e pescoço pode romper seus núcleos, disparar um alarme de perigo interno, empurrá-las para um estado dormente e, em última instância, ajudá-las a retornar como células mais agressivas, invasivas e semelhantes a células-tronco. Entender essa via mecânica da evolução do câncer pode abrir novas formas de bloquear recidiva e metástase.
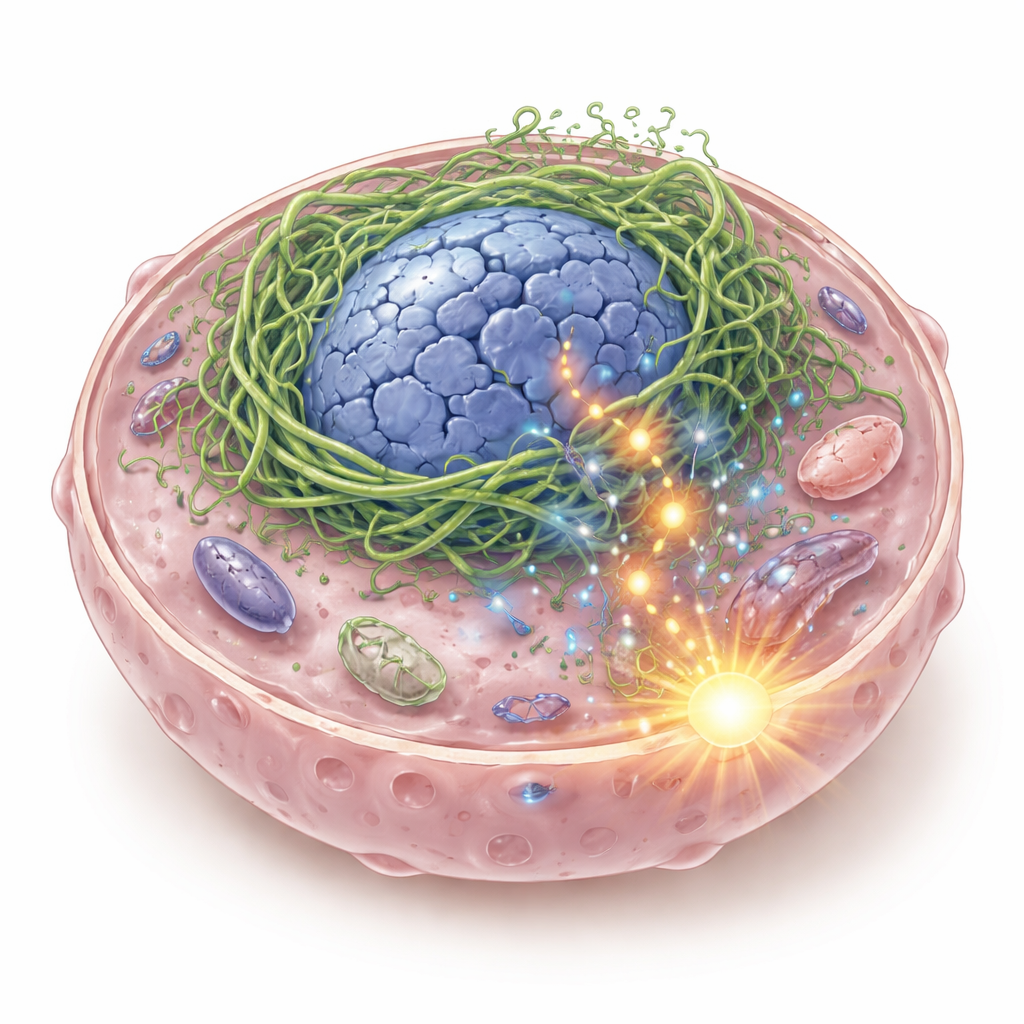
Um andaime interno quebrado com consequências perigosas
Dentro de cada célula existe um andaime flexível feito de filamentos protéicos que mantém a célula e seu núcleo em forma e a ajuda a perceber forças físicas. Os autores focaram nas queratinas, uma família de proteínas de suporte comuns em tecidos epiteliais, incluindo os que revestem a boca e a garganta. Em alguns carcinomas de células escamosas de cabeça e pescoço, eles descobriram uma queratina híbrida chamada K6-K14/V5, formada quando dois genes de queratina se fundem. Quando essa proteína de fusão é ativada nas células cancerosas, ela não forma uma rede de suporte suave. Em vez disso, agrupa-se firmemente ao redor do núcleo, distorcendo-o em estruturas ocas e deformadas e causando quebras no DNA. Fragmentos de DNA vazam para o citosol, onde são detectados por um sistema sensor imune chamado cGAS–STING, que normalmente dispara o alarme quando detecta DNA viral.
Da pressão para morrer à sobrevivência oculta
O efeito imediato desse dano nuclear é prejudicial para as células cancerosas: seu crescimento desacelera e muitas morrem. No entanto, uma fração consegue persistir. Esses sobreviventes são fortemente influenciados pelo seu entorno físico. Em placas plásticas planas padrão, eles gradualmente desaparecem, porém quando cultivados em um gel de colágeno macio — mais próximo da textura dos tecidos reais — eles persistem e ressurgem como uma nova população, chamada 3D-V5. Análises de expressão gênica mostram que essas células respondem ao alarme contínuo de dano ao DNA ativando autofagia, um programa de autolimpeza que recicla partes danificadas, especialmente mitocôndrias defeituosas. Essa resposta os ajuda a entrar em um estado dormente de baixa atividade que lhes permite resistir ao estresse em vez de serem eliminados.
Células dormentes reprogramam-se e se preparam para migrar
Enquanto dormentes, esses sobreviventes silenciosamente reescrevem seus programas internos. Eles mudam a composição de queratinas e adotam um estado de transição epitelial–mesenquimal “parcial” (pEMT) — uma identidade intermediária que mantém algumas características epiteliais, mas ganha flexibilidade e motilidade. Tornam-se muito melhores em formar esferas e semear novos aglomerados celulares, um marco da propriedade de célula-tronco do câncer. Com o tempo, suas propriedades mecânicas se recuperam: reendurecem seus núcleos, reconstróem fortes fibras de actina e desenvolvem longas protrusões que sondam e aderem à matriz circundante. Também aumentam a produção de enzimas chamadas metaloproteinases da matriz (MMPs), que degradam a malha extracelular e abrem caminhos para a invasão.
Conversando com células vizinhas para construir um nicho de suporte
Essas células cancerosas reprogramadas não atuam isoladamente. A equipe observou que as células 3D-V5 liberam grande número de pequenas partículas chamadas vesículas extracelulares para o entorno. Quando essas vesículas atingem fibroblastos orais próximos — células do tecido conjuntivo — os fibroblastos alteram sua própria atividade gênica, tornando-se mais semelhantes a fibroblastos associados ao câncer que suportam o crescimento tumoral. Muitos dos sinais trocados giram em torno do eixo FGF–FGFR, uma família de fatores de crescimento e seus receptores conhecidos por impulsionar proliferação, plasticidade e resistência. Em culturas de laboratório e em tumores de camundongos, bloquear a atividade de FGFR reduziu essa vantagem de crescimento. Em animais, tumores formados a partir de células 3D-V5 eram pouco diferenciados, mais invasivos, ricos em marcadores de célula-tronco e mais propensos a se espalhar além do local de injeção.
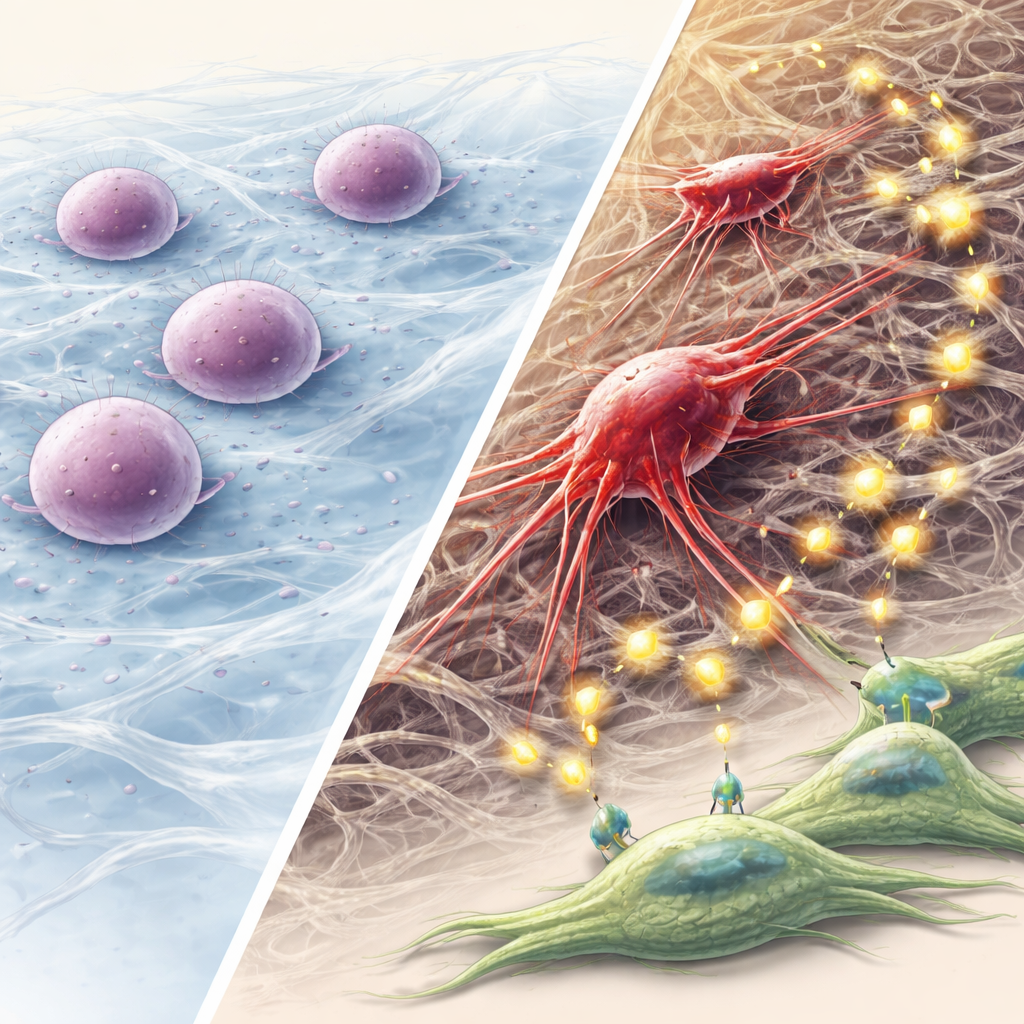
Por que essa via mecânica para câncer agressivo importa
Este trabalho propõe um modelo em etapas: uma fusão de queratina desorganiza o andaime interno da célula, comprime o núcleo e dispara um alarme de dano ao DNA; a autofagia então permite que algumas células entrem em dormência em vez de morrer; ao longo do tempo, esses sobreviventes reorganizam seu esqueleto, adquirem traços semelhantes a células-tronco e invasivos, e remodelam seu ambiente por meio de vesículas e sinalização FGF. Para leitores não especializados, a mensagem principal é que forças físicas e proteínas estruturais dentro das células podem ser tão importantes quanto genes e compostos químicos na condução da evolução do câncer. Mirar essa via mecânica estresse–autofagia–FGF, especialmente em cânceres de cabeça e pescoço com fusões de queratina, pode oferecer novas estratégias para evitar que células tumorais dormentes voltem à atividade e se disseminem.
Citação: Chen, IH., Ravichandran, S., Lai, MT. et al. Cytoskeleton reorganization induced by a novel K6-K14 keratin fusion promotes cancer stemness and cellular plasticity via cGAS-STING selection. Oncogenesis 15, 5 (2026). https://doi.org/10.1038/s41389-026-00598-1
Palavras-chave: propriedades de célula-tronco do câncer, citoesqueleto celular, dormência tumoral, câncer de cabeça e pescoço, mecanotransdução