Clear Sky Science · pt
O papel da desmetilase de histona PHF2 como supressor tumoral no carcinoma hepatocelular por meio da regulação de SRXN1
Por que este estudo sobre câncer de fígado é importante
O câncer de fígado é um dos mais letais no mundo, e os medicamentos atuais prolongam a vida de forma modesta para muitos pacientes. Este estudo faz uma pergunta diferente: em vez de mirar nos genes clássicos responsáveis pelo câncer, podemos explorar a forma como o DNA é embalado e quimicamente marcado dentro das células hepáticas para encontrar novas opções de tratamento mais precisas? Os pesquisadores focalizam uma proteína pouco conhecida chamada PHF2 e revelam como ela pode ajudar a impedir que células do fígado se tornem cancerosas.
Procurando vulnerabilidades no sistema de controle do câncer
O câncer não é movido apenas por genes quebrados; ele também é alimentado por controles “epigenéticos” defeituosos — as marcas químicas e complexos proteicos que decidem quais genes ficam ativados ou desativados. No carcinoma hepatocelular, a forma mais comum de câncer de fígado, muitos desses reguladores estão perturbados. A equipe testou sistematicamente 497 reguladores epigenéticos em seis linhagens de células de câncer de fígado, usando ferramentas de RNA para reduzir temporariamente cada regulador um a um e depois medindo a sobrevivência das células cancerosas. Essa triagem em grande escala foi projetada para revelar de quais reguladores os cânceres dependem para crescer e quais normalmente funcionam como freios à formação tumoral.
Encontrando novos aceleradores e protetores do câncer
A triagem revelou dois grupos amplos: potenciais “aceleradores” do câncer (oncogenes) cuja perda prejudicou a sobrevivência das células tumorais, e potenciais “freios” (supressores tumorais) cuja perda fez as células cancerosas crescerem melhor. Ao combinar seus dados de laboratório com grandes conjuntos de dados públicos de pacientes, os pesquisadores reduziram a lista a alguns candidatos clinicamente relevantes. Dois reguladores, SUPT7L e SMARCC1, tenderam a estar mais ativos em tumores e se associaram a pior sobrevida. Em contraste, um regulador — PHF2 — frequentemente estava menos ativo em tumores hepáticos, e pacientes cujos tumores mantinham níveis mais altos de PHF2 geralmente viveram mais. Esses padrões sugeriram que PHF2 pode atuar como supressor tumoral no câncer de fígado humano.
Como a perda de PHF2 altera as células de câncer de fígado
Para testar PHF2 mais a fundo, a equipe engenheirou células de carcinoma hepatocelular para produzir de forma estável menos dessa proteína e acompanhou seu comportamento ao longo do tempo. Células com PHF2 reduzida cresceram mais rápido e exibiram níveis mais altos de Ki-67, um marcador de divisão celular ativa, indicando que PHF2 normalmente ajuda a conter a proliferação. Esses efeitos foram mais pronunciados em linhagens de câncer de fígado já agressivas, o que implica que a simples perda de PHF2 pode não iniciar o câncer por si só, mas pode acelerar o crescimento de células malignas uma vez que os tumores se formam.
Uma ligação surpreendente com as defesas contra estresse celular
Em seguida, os pesquisadores usaram métodos modernos de perfil proteico para catalogar milhares de proteínas cujos níveis mudaram quando PHF2 foi reduzida. Entre muitas alterações sutis, um padrão se destacou: os níveis de uma proteína de proteção ao estresse chamada SRXN1 caíram consistentemente quando PHF2 foi perdida. SRXN1 ajuda as células a gerenciar espécies reativas de oxigênio — subprodutos quimicamente reativos que podem danificar DNA e proteínas, mas também podem forçar células tumorais a se adaptarem. Os dados sugeriram que PHF2 ajuda a manter os níveis de SRXN1, e que alterar esse equilíbrio pode influenciar como as células de câncer de fígado respondem ao estresse interno e, em última instância, quão rápido elas crescem.
Agindo fora de uma via de estresse bem conhecida
SRXN1 costuma ser controlada por um interruptor mestre da resposta ao estresse chamado Nrf2, que ativa muitos genes antioxidantes quando as células enfrentam estresse oxidativo. Como SRXN1 caiu quando PHF2 foi suprimida, a equipe questionou se PHF2 poderia simplesmente atuar por meio dessa via conhecida de Nrf2. Eles examinaram genes e proteínas-chave relacionados ao Nrf2, trataram células com fármacos que ativam Nrf2 bloqueando seu inibidor Keap1, e usaram ferramentas genéticas para reduzir Keap1 diretamente. Em todos esses testes, a resposta das células deficientes em PHF2 se assemelhou bastante à das células normais, e análises mais amplas de vias e fatores de transcrição não destacaram Nrf2 como um ator principal. Em vez disso, outros fatores, incluindo ZNF384 e Nrf1 — ambos previamente ligados ao câncer de fígado — emergiram como candidatos. Em conjunto, as evidências sugerem que o controle de PHF2 sobre SRXN1 e respostas antioxidantes pode contornar a sinalização clássica de Nrf2, insinuando uma rota distinta de regulação do estresse nesses tumores.
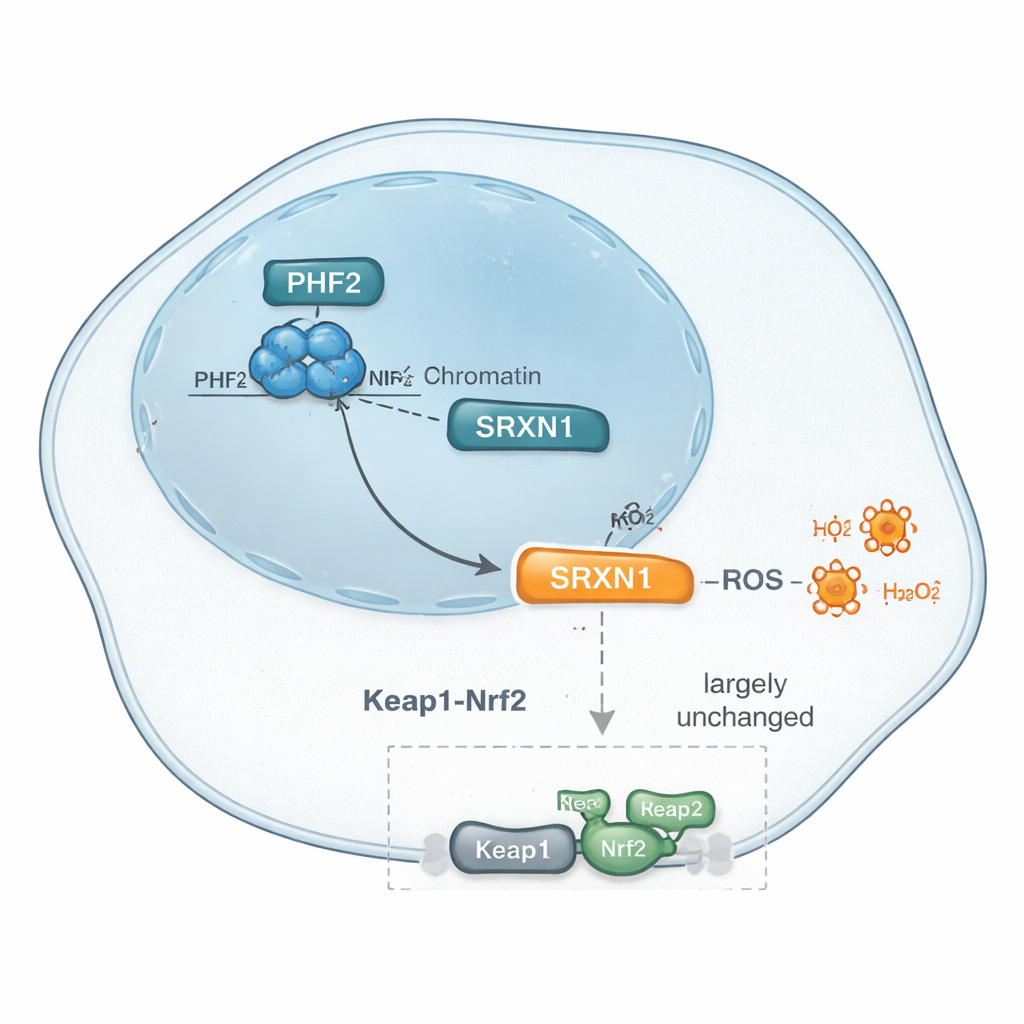
O que isso pode significar para futuros tratamentos
Para o não especialista, a conclusão chave é que este estudo identifica PHF2 como um fator protetor promissor no câncer de fígado: quando PHF2 está presente e ativa, as células tumorais crescem mais devagar; quando está diminuída, elas ganham vantagem de crescimento e alteram a forma como lidam com o estresse celular. Como PHF2 em si pode ser difícil de bloquear ou aumentar com fármacos convencionais de pequena molécula, os autores apontam para estratégias emergentes, como terapias baseadas em RNA ou drogas que potencializam a atividade de PHF2 por meio de parceiros de sinalização a montante. Eles também enfatizam que os efeitos de PHF2 são dependentes do contexto — seu impacto pode variar com outras mutações, como o status de p53 — de modo que qualquer terapia futura provavelmente exigirá uma seleção cuidadosa de pacientes. No geral, o trabalho refina nossa compreensão de como reguladores epigenéticos moldam o comportamento do câncer de fígado e abre novas vias para projetar tratamentos que restaurem ou imitem a influência supressora tumoral de PHF2.
Citação: Thng, D.K.H., Hooi, L., Yong, W.K. et al. The role of histone demethylase PHF2 as a tumour suppressor in hepatocellular carcinoma by regulating SRXN1. Oncogenesis 15, 6 (2026). https://doi.org/10.1038/s41389-026-00597-2
Palavras-chave: carcinoma hepatocelular, regulação epigenética, PHF2, SRXN1, terapia contra câncer de fígado