Clear Sky Science · pt
Degradação mediada por TRIM21 de HILPDA supera resistência à imunoterapia anti‑PD‑1 no câncer de mama ao limitar a palmitoilação de PD‑L1
Por que algumas imunoterapias contra o câncer deixam de funcionar
Drogas que liberam o sistema imunológico, como terapias anti–PD‑1, transformaram o tratamento de vários cânceres, inclusive formas agressivas de câncer de mama. Ainda assim, muitos tumores ou nunca respondem ou acabam encontrando maneiras de escapar. Este estudo investiga uma dessas rotas de escape no câncer de mama triplo‑negativo e mostra como reconfigurar o metabolismo lipídico tumoral — e um medicamento reposicionado chamado fenretinida — pode reabrir a porta para o sistema imunológico quando a imunoterapia padrão falha. 
Um ajudante oculto que protege os tumores
Os pesquisadores focaram em uma proteína pouco conhecida chamada HILPDA, previamente associada à forma como as células lidam com gorduras sob estresse. Ao comparar tumores mamários de camundongos que permaneceram sensíveis à terapia anti‑PD‑1 com tumores que se tornaram resistentes, eles descobriram que os níveis de HILPDA eram muito maiores nos cânceres resistentes. Análises de grandes bancos de dados de pacientes e amostras de tumores de mulheres com câncer de mama confirmaram que HILPDA é mais abundante em tumores do que no tecido mamário normal, especialmente na doença triplo‑negativa, e que pacientes cujos tumores expressam mais HILPDA tendem a ter prognóstico pior. Tumores de pessoas que não se beneficiaram dos medicamentos bloqueadores de PD‑1 também apresentaram mais HILPDA, ligando essa proteína diretamente à falha do tratamento.
Como os tumores viram o cenário imune contra nós
Para ver o que HILPDA realmente faz dentro dos tumores, a equipe engenheirou células de câncer de mama para superproduzir ou não expressar a proteína e então as cultivou com células imunes humanas ou em camundongos. Quando HILPDA estava alto, os tumores atraíam mais células T reguladoras, células supressoras derivadas de mieloides e macrófagos do tipo M2 — tipos de células imunes que atenuam o ataque e ajudam os cânceres a se esconderem. Ao mesmo tempo, o número e a vigorosidade das células CD8 citotóxicas e das células NK caíram, e sua capacidade de liberar moléculas tóxicas e sinais inflamatórios foi reduzida. Silenciar HILPDA inverteu esse quadro: os tumores abrigaram menos células supressoras, mais células assassinas ativas, crescimento mais lento e menos metástases. Crucialmente, quando animais com tumores de baixo HILPDA receberam terapia anti‑PD‑1, seus tumores encolheram mais e os camundongos viveram mais, mostrando que HILPDA controla quão bem a imunoterapia funciona.
Fabricação de gordura, armadura molecular e escape imune
Aprofundando-se, os cientistas descobriram como HILPDA remodela o metabolismo tumoral para endurecer as defesas imunes. Dentro das células cancerosas, HILPDA se liga a uma proteína chaperona chamada HSP90 para estabilizar um fator de transcrição, KLF5, que impulsiona a produção de lipídios. Esse trio aumenta a síntese de ácidos graxos, especialmente palmitato, e enche as células tumorais com gotículas lipídicas. Uma dessas gorduras é então anexada ao PD‑L1, a proteína de checkpoint que fica na superfície tumoral e envia um sinal de “não atacar” às células imunes. A equipe mostrou que adicionar palmitato a um ponto específico do PD‑L1 age como uma cola molecular: ajuda o PD‑L1 a permanecer estável na membrana celular e impede que ele seja degradado. Mutar esse único sítio de ligação despojou o PD‑L1 de sua estabilidade e enfraqueceu sua capacidade de proteger as células cancerosas, mesmo quando HILPDA era abundante. Em outras palavras, a produção de gordura impulsionada por HILPDA fornece uma modificação química no PD‑L1 que transforma o escudo imune do tumor de frágil em aço reforçado.
O freio embutido que pode ser acionado
Todo acelerador precisa de um freio, e aqui o freio é outra proteína chamada TRIM21. Os autores descobriram que TRIM21 reconhece HILPDA e a marca com “sinais” moleculares que a enviam para a maquinaria de eliminação da célula. Em tumores de mama de pacientes, os níveis de TRIM21 tendiam a ser baixos quando HILPDA estava alto, e TRIM21 baixo foi associado a desfechos piores, sugerindo que esse sistema de freio natural costuma estar enfraquecido no câncer. A equipe então buscou drogas que pudessem fortalecer a TRIM21 e identificou a fenretinida, um retinoide já testado em humanos. Em modelos celulares e animais de câncer de mama triplo‑negativo, a fenretinida aumentou a atividade de TRIM21, acelerou a degradação de HILPDA, reduziu a síntese de lipídios e a modificação protetora do PD‑L1, e retardou o crescimento e a disseminação tumoral. Mais impressionante, combinar fenretinida com terapia anti‑PD‑1 tornou os tumores mais vulneráveis ao ataque imune, aumentando células T citotóxicas e células NK enquanto reduzia células supressoras no microambiente tumoral. 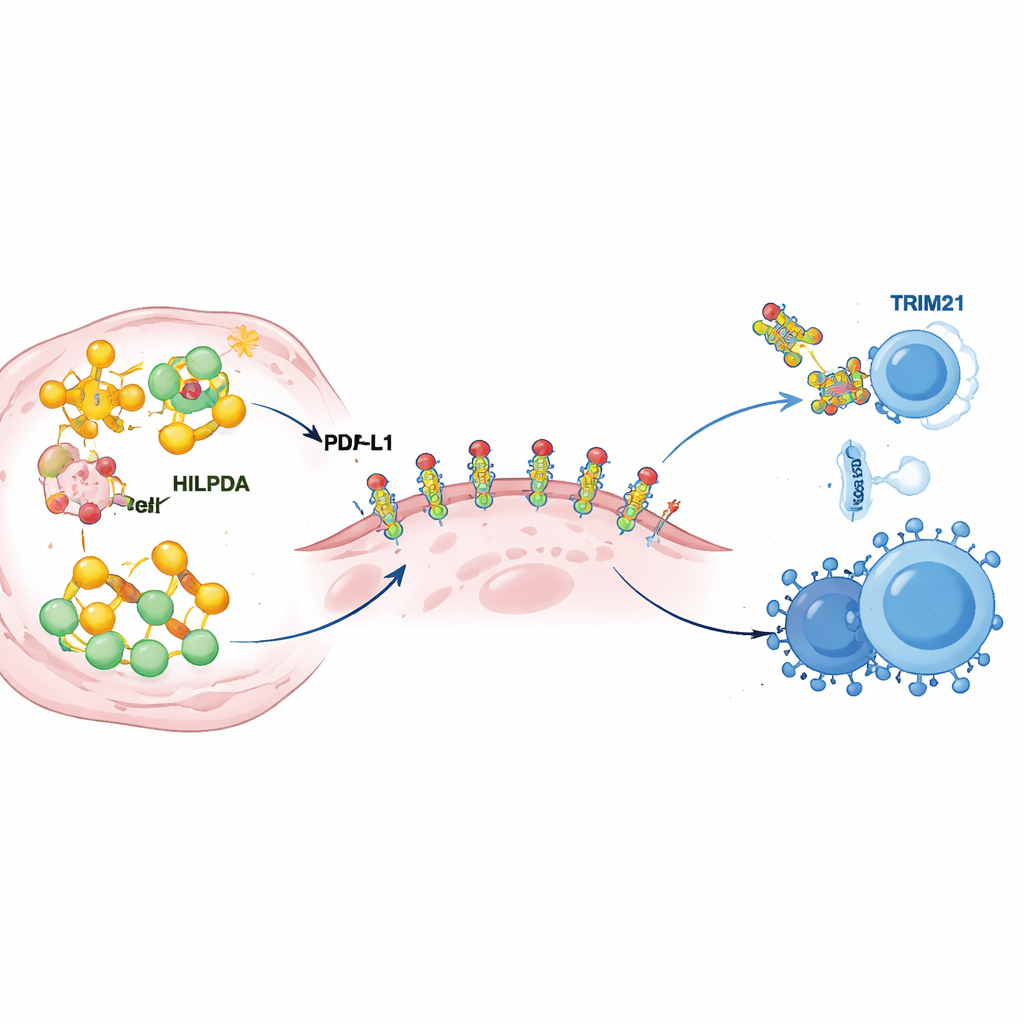
O que isto significa para o cuidado futuro do câncer
Este trabalho revela uma cadeia de eventos na qual células de câncer de mama estressadas aumentam HILPDA, intensificam a produção de lipídios e reforçam quimicamente o PD‑L1 em sua superfície, permitindo que continuem suprimindo células imunes mesmo diante de drogas bloqueadoras de PD‑1. TRIM21 atua como uma salvaguarda interna que pode desmontar o HILPDA, mas frequentemente está fraca nos tumores. Ao descobrir que a fenretinida pode reativar essa salvaguarda, o estudo aponta para uma forma prática de combinar um fármaco metabólico com a imunoterapia existente para superar a resistência. Se confirmado em ensaios clínicos, direcionar o eixo TRIM21–HILPDA–PD‑L1 poderia dar aos pacientes com câncer de mama triplo‑negativo de difícil tratamento uma segunda chance de se beneficiar de terapias baseadas no sistema imune.
Citação: Wang, X., Li, G., Wu, J. et al. TRIM21-mediated degradation of HILPDA overcomes anti-PD-1 immunotherapy resistance in breast cancer by limiting PD-L1 palmitoylation. Oncogene 45, 1338–1356 (2026). https://doi.org/10.1038/s41388-026-03728-6
Palavras-chave: câncer de mama triplo‑negativo, resistência à imunoterapia, palmitoilação de PD‑L1, metabolismo lipídico tumoral, fenretinida