Clear Sky Science · pt
Cereblon (CRBN) inibe a metástase do câncer de próstata ao regular negativamente a 6‑fosfogluconato desidrogenase (6PGD)
Por que esta pesquisa importa
Quando o câncer de próstata se espalha da próstata para outros órgãos, torna‑se muito mais difícil de tratar e frequentemente fatal. Este estudo revela como uma proteína celular pouco conhecida de “controle de qualidade”, cereblon (CRBN), ajuda a impedir a disseminação do câncer de próstata ao desmontar uma enzima metabólica que alimenta comportamentos agressivos. Compreender esse sistema de freio embutido sugere novas maneiras de retardar ou impedir a metástase, especialmente em formas de dificil tratamento da doença.
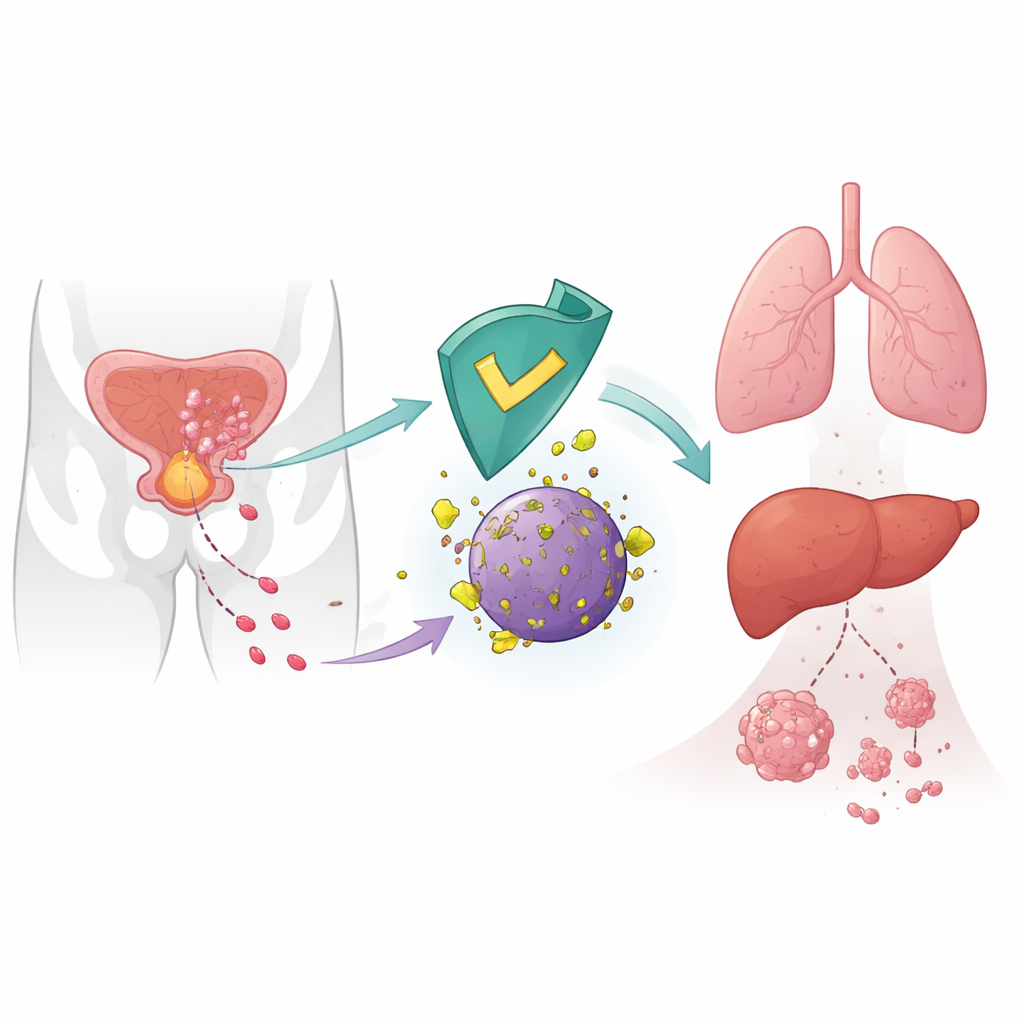
Um freio interno à propagação do câncer
As células tumorais não se espalham ao acaso; elas reprogramam sua maquinaria interna para se mover, invadir e colonizar órgãos distantes. Os autores concentraram‑se no CRBN, uma proteína mais conhecida por ser alvo de fármacos como talidomida usados em cânceres sanguíneos. Em células saudáveis, o CRBN faz parte de uma unidade molecular de descarte que marca certas proteínas para destruição. Trabalhos anteriores sugeriram que níveis baixos de CRBN em tumores estavam ligados a piores desfechos, mas seu papel direto na metástase era incerto. Aqui, os pesquisadores mostram que o CRBN atua como um supressor natural da disseminação do câncer de próstata ao direcionar uma enzima metabólica chamada 6‑fosfogluconato desidrogenase (6PGD) para a degradação.
Um motor metabólico que o câncer sequestra
A 6PGD participa de uma rota metabólica conhecida como via das pentoses fosfato oxidativa, que ajuda as células a gerar NADPH, uma molécula que fornece tanto blocos de construção quanto poder antioxidante. Muitos tumores aumentam essa via para crescer mais rápido e tolerar estresse. A equipe constatou que amostras de câncer de próstata de pacientes tendem a ter menos CRBN e mais 6PGD do que o tecido prostático normal, e que esse desequilíbrio é especialmente pronunciado em doenças agressivas. Em linhagens celulares de câncer de próstata, reduzir o CRBN ou degradá‑lo com um composto desenhado fez com que os níveis e a atividade enzimática da 6PGD aumentassem, elevando o NADPH. Restaurar o CRBN causou o efeito oposto, diminuindo 6PGD e NADPH sem alterar a mensagem gênica da 6PGD, apontando para um controle ao nível da proteína.
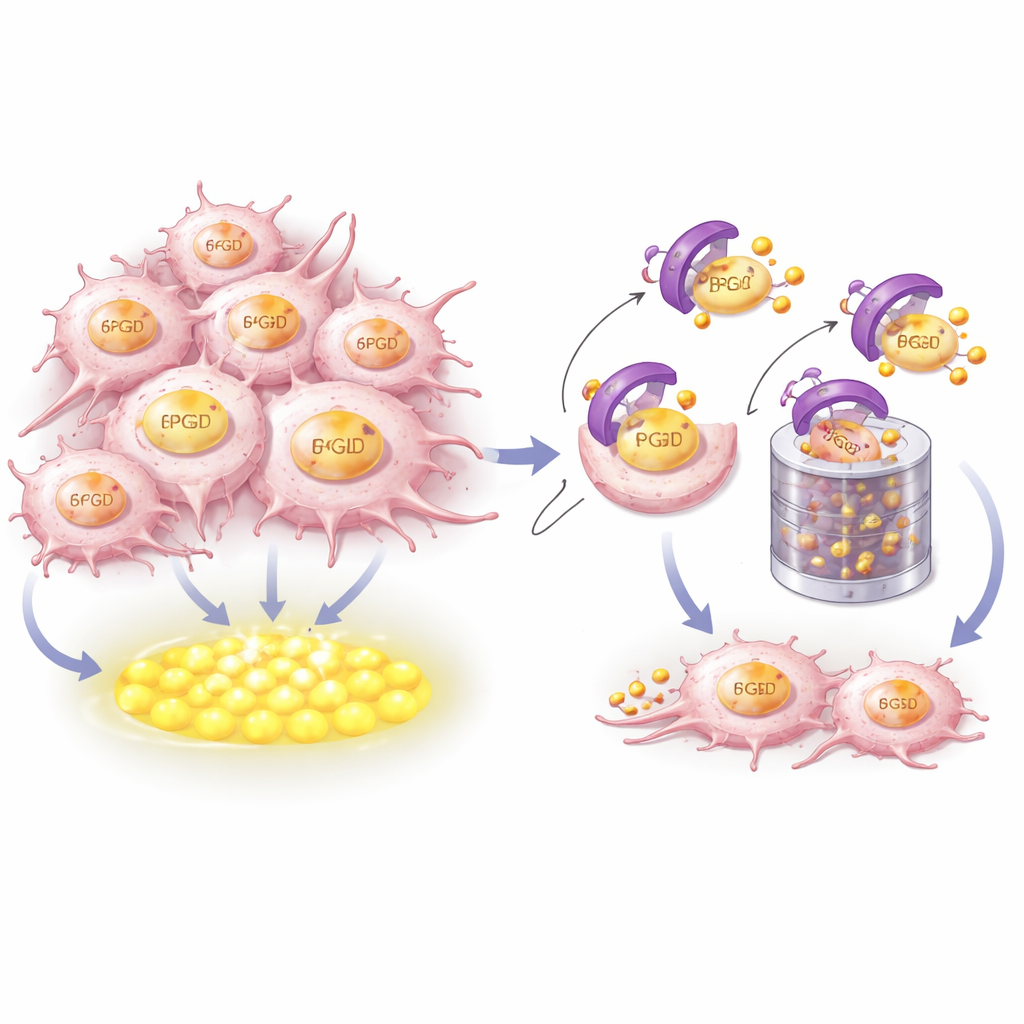
Como o CRBN reconhece e destrói a fonte de combustível
Para entender como o CRBN controla a 6PGD, os pesquisadores combinaram modelagem estrutural com experimentos bioquímicos. Eles mostraram que o CRBN agarra fisicamente um segmento helicoidal curto e altamente conservado próximo à extremidade final da 6PGD. Aminoácidos-chave em ambas as proteínas formam uma interface de encaixe precisa. Quando esses pontos de contato foram alterados, o CRBN não conseguiu mais se ligar à 6PGD, anexar as pequenas etiquetas de ubiquitina que a marcam para descarte, nem enviá‑la ao triturador celular conhecido como proteassoma. Notavelmente, essa superfície de reconhecimento é separada do bolso onde drogas imunomoduladoras se ligam ao CRBN, o que significa que o controle do CRBN sobre a 6PGD faz parte de seu papel nativo de manutenção, em vez de um efeito induzido por medicamentos.
De metabolismo alterado a células migratórias
As consequências desse aperto molecular se manifestam no comportamento celular. Em células de câncer de próstata sem CRBN, os níveis elevados de 6PGD e NADPH acompanharam aumento de movimento e invasão através de barreiras artificiais, características do potencial metastático. Quando o CRBN foi superexpresso, as células tornaram‑se menos móveis e invasivas, embora sua taxa de crescimento não tenha mudado. A análise de atividade gênica mostrou que o CRBN aumentou os níveis de CDH1, associado a células epiteliais compactas, e diminuiu os níveis de MMP1, ligado à degradação de tecido e migração. Importante, essas mudanças requereram ligação direta entre CRBN e 6PGD e puderam ser revertidas ao bloquear a atividade enzimática da 6PGD, ligando as alterações metabólicas às mudanças no comportamento metastático.
Evidências em modelos animais e outros cânceres
A equipe testou essas ideias em camundongos injetando células de câncer de próstata na corrente sanguínea ou no baço. Células projetadas para produzir CRBN extra formaram muito menos nódulos metastáticos no fígado e nos pulmões do que células controle, confirmando um papel antimetastático em animais vivos. Camundongos geneticamente sem CRBN mostraram níveis mais altos de proteína 6PGD em vários órgãos. Padrões semelhantes apareceram em linhagens de glioblastoma, câncer de pulmão e câncer renal: remover o CRBN aumentou 6PGD e impulsionou movimento e invasão celular, enquanto a inibição genética ou por fármacos da 6PGD conteve esse comportamento agressivo. Essas observações sugerem que o freio CRBN–6PGD sobre a metástase não é exclusivo do câncer de próstata.
O que isso pode significar para tratamentos futuros
No conjunto, o estudo propõe que o CRBN atua como um guardião metabólico que restringe o suprimento de energia necessário para que células cancerosas se soltem, migrem e semeiem novos tumores. Quando o CRBN é perdido ou está em níveis baixos, a 6PGD se acumula, a produção de NADPH aumenta e as células tornam‑se mais propensas a sofrer mudanças que favorecem a metástase. Para pacientes, isso aponta duas possibilidades: medir os níveis de CRBN e 6PGD pode ajudar a identificar tumores com alto risco metastático, e terapias que aumentem a função do CRBN — ou que atenuem seletivamente a 6PGD em tumores pobres em CRBN — podem oferecer novas formas de retardar ou prevenir a disseminação do câncer de próstata e de outros tipos.
Citação: Guchhait, K., Yoon, HS., An, HS. et al. Cereblon (CRBN) inhibits prostate cancer metastasis by negatively regulating 6-phosphogluconate dehydrogenase (6PGD). Oncogene 45, 1234–1246 (2026). https://doi.org/10.1038/s41388-026-03717-9
Palavras-chave: metástase do câncer de próstata, metabolismo do câncer, cereblon, enzima 6PGD, via do NADPH