Clear Sky Science · pt
A helicase de RNA multifuncional DDX39A impulsiona a progressão do glioblastoma modulando o splicing alternativo de WISP1 que induz a polarização imunossupressora de macrófagos
Por que este estudo sobre câncer cerebral importa
O glioblastoma é um dos cânceres cerebrais mais letais, conhecido por recidivar após o tratamento e resistir a medicamentos. Este estudo revela como um único “interruptor” molecular nas células tumorais não apenas ajuda o câncer a crescer, mas também convence células imunes próximas a deixarem de combater e começarem a proteger o tumor. Ao rastrear essa cadeia de eventos, os pesquisadores também identificam um antipsicótico já existente que pode ser reposicionado para interromper essa rede prejudicial.
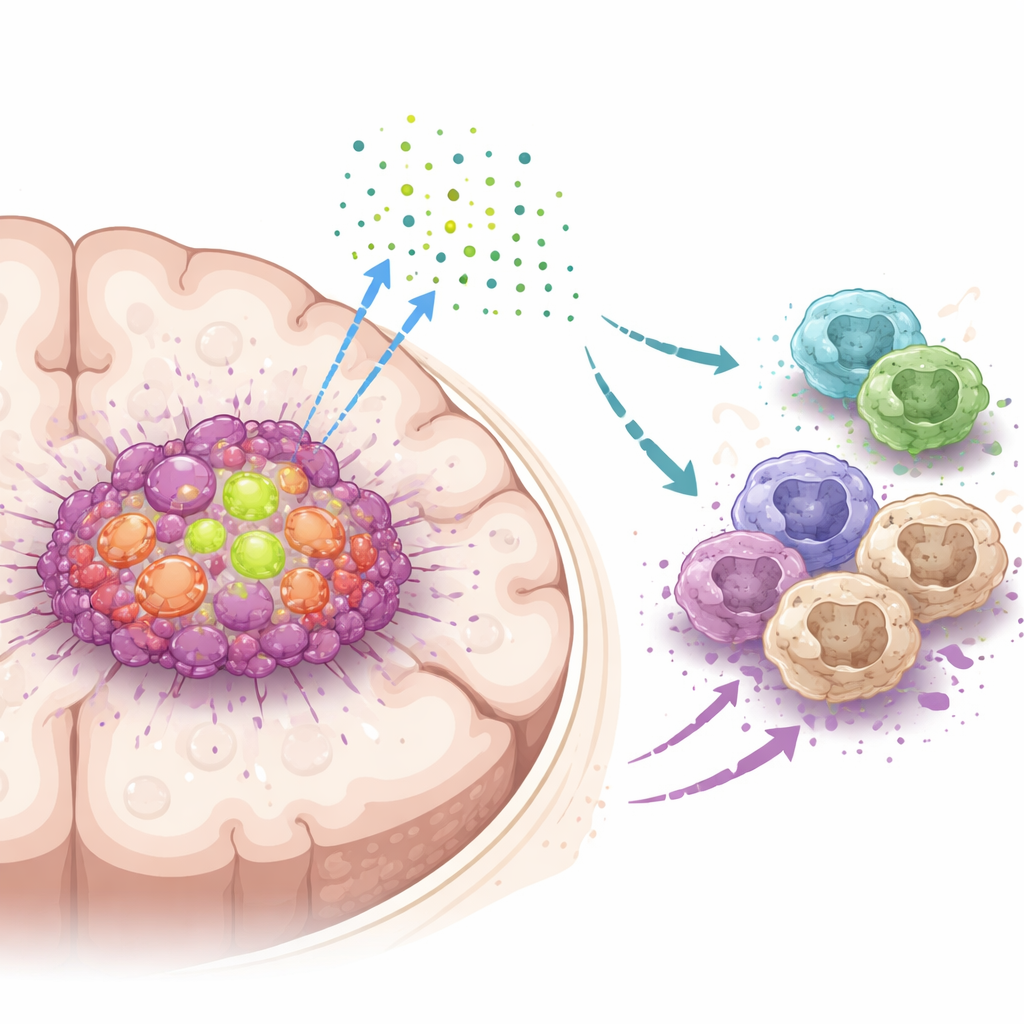
Um ajudante chave dentro das células do tumor cerebral
A equipe concentrou-se em uma proteína chamada DDX39A, uma máquina molecular que auxilia as células a processar RNA, a cópia funcional da informação genética. Ao analisar grandes conjuntos de dados de pacientes e amostras tumorais, descobriram que DDX39A está muito mais ativa no glioblastoma do que no tecido cerebral normal, e seus níveis aumentam com o grau do tumor. Análises em célula única mostraram que DDX39A é especialmente abundante em células tumorais de divisão rápida e em certos glóbulos imunes chamados macrófagos dentro da massa tumoral. Pacientes cujos tumores apresentavam níveis mais altos de DDX39A tendiam a ter desfechos piores, sugerindo que essa proteína está intimamente ligada à doença agressiva.
Como esse ajudante alimenta crescimento e disseminação
Para testar o que DDX39A realmente faz, os pesquisadores usaram ferramentas genéticas para reduzi-lo em células semelhantes a células-tronco de glioblastoma cultivadas em laboratório e em modelos murinos de tumor cerebral. Quando DDX39A foi diminuída, as células tumorais cresceram mais lentamente, invadiram menos os tecidos circundantes e tiveram maior propensão a sofrer morte celular programada. As células semelhantes a células-tronco tumorais também perderam grande parte da capacidade de formar novas esferas tumorais, sinal de que sua habilidade de autorrenovação foi prejudicada. Em camundongos, tumores com DDX39A reduzida foram menores e os animais viveram mais, confirmando que essa proteína impulsiona ativamente a progressão tumoral, e não apenas a marca.
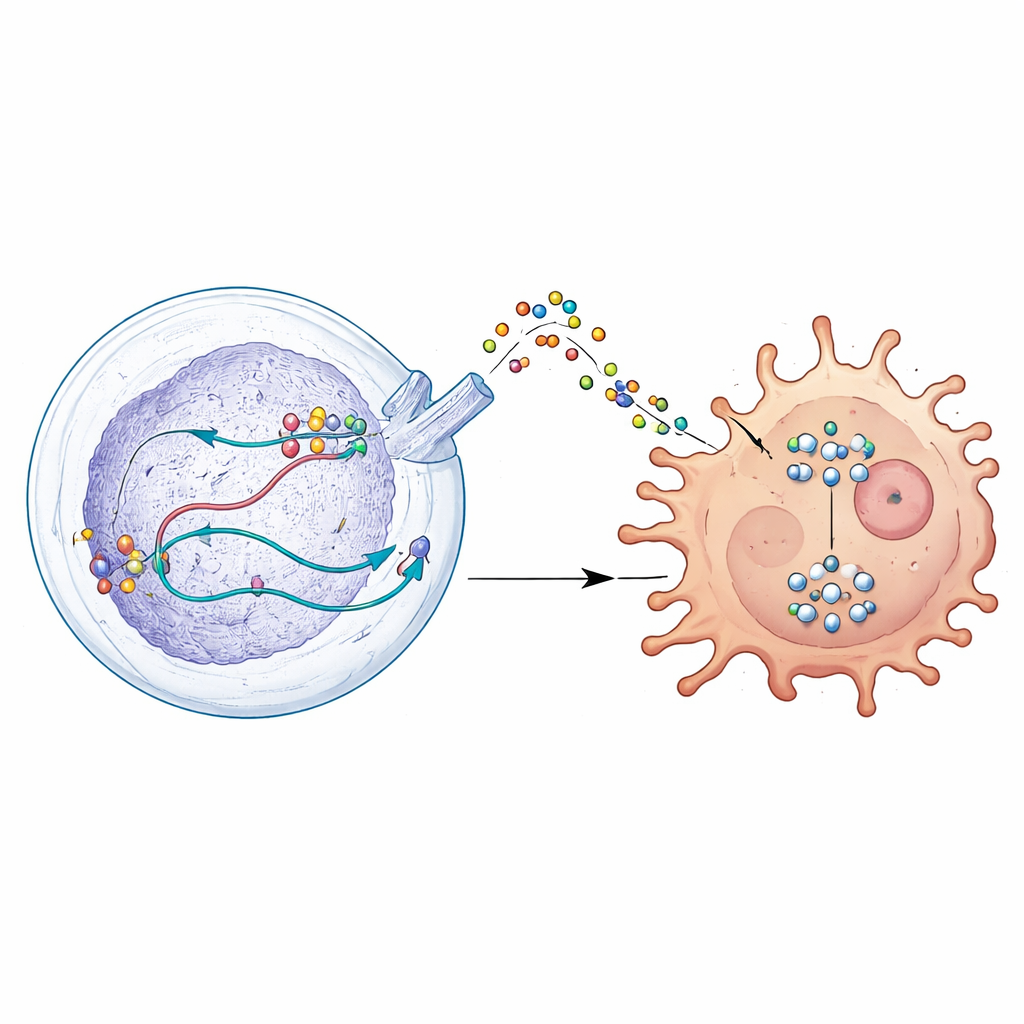
Um sinal secreto que desarma os defensores imunes
Ainda mais a fundo, os cientistas descobriram que DDX39A altera como um gene chamado WISP1 é processado. Em vez de simplesmente ligar ou desligar WISP1, DDX39A ajuda a moldar seu RNA de modo a estabilizar a mensagem e aumentar a produção da proteína WISP1. As células tumorais então liberam WISP1 em seu entorno, onde ela age como um sinal enganoso. Macrófagos próximos, que podem atacar tumores ou apoiá-los, respondem a esse sinal mudando para um estado imunossupressor que favorece o tumor. Essa mudança é conduzida pela ativação de uma via de controle de crescimento interna conhecida como AKT. Quando DDX39A ou WISP1 foi reduzido, essa via foi silenciada, as células tumorais ficaram menos agressivas e os macrófagos voltaram a um perfil mais voltado ao combate ao tumor.
Transformando um remédio psiquiátrico em arma contra o câncer
Munidos desse mapa de vias, os pesquisadores vasculharam bancos de dados de fármacos em busca de moléculas que pudessem interferir na atividade de DDX39A. Focaram na flufenazina, um antipsicótico de longa data conhecido por atingir o cérebro. Modelagem computacional e testes de ligação mostraram que a flufenazina pode se ligar diretamente à DDX39A. Nas células tumorais, o fármaco enfraqueceu a interação de DDX39A com o RNA de WISP1, reduziu os níveis de WISP1 e diminuiu a sinalização via AKT. As células tratadas cresceram menos, invadiram menos, formaram menos esferas tumorais e tornaram-se mais propensas à morte. Em modelos murinos, a flufenazina retardou o crescimento do tumor cerebral, reduziu o número de macrófagos que apoiam o tumor e prolongou a sobrevivência, tudo isso com doses semelhantes às já usadas em humanos para outras condições.
O que isso significa para tratamentos futuros
Em termos práticos, este estudo mostra que as células de glioblastoma exploram DDX39A para ajustar uma mensagem (WISP1) que tanto aumenta sua resistência quanto reprograma células imunes próximas em protetores em vez de combatentes. Bloquear esse ajudante, seja geneticamente ou com um fármaco como a flufenazina, enfraquece o câncer em duas frentes: as próprias células tumorais e o escudo protetor de macrófagos imunossupressores. Embora sejam necessários muitos testes adicionais antes que essa estratégia chegue aos pacientes, o trabalho abre uma via promissora para reposicionar um medicamento conhecido e atingir um ponto fraco recém-revelado em um dos cânceres cerebrais mais persistentes.
Citação: Zhang, Y., Xue, Z., Zhang, N. et al. The multifunctional RNA helicase DDX39A drives glioblastoma progression by modulating WISP1 alternative splicing that induces an immunosuppressive macrophage polarization. Oncogene 45, 1026–1041 (2026). https://doi.org/10.1038/s41388-026-03715-x
Palavras-chave: glioblastoma, splicing de RNA, microambiente tumoral, polarização de macrófagos, reposicionamento de fármacos