Clear Sky Science · pt
PMM2 interage com TRIM28 para recrutar E2F4 e promover a glicólise tumoral mediada por KIFC3 e a progressão do câncer colorretal
Por que esta história sobre câncer importa
O câncer colorretal está entre os tipos de câncer mais letais do mundo, em parte porque muitos tumores aprendem a sequestrar os sistemas energéticos do corpo para alimentar um crescimento descontrolado. Este estudo revela como uma enzima pouco conhecida, PMM2, ajuda tumores colorretais a queimar açúcar de forma mais agressiva e a se espalhar, e por que isso a torna um novo alvo promissor para futuros medicamentos e testes diagnósticos.
Um motor tumoral faminto por açúcar
As células cancerígenas frequentemente reprogramam a forma como utilizam a glicose, privilegiando uma forma de queima de açúcar de alta velocidade e baixa eficiência conhecida como glicólise. Os pesquisadores começaram comparando milhares de genes em amostras de tumor colorretal com tecido saudável adjacente. PMM2, uma enzima normalmente envolvida na ligação de cadeias de açúcar a proteínas, destacou-se como um dos genes mais fortemente aumentados no câncer. Células tumorais com excesso de PMM2 cresceram mais rápido, formaram mais colônias e se espalharam mais facilmente em placas de cultura, enquanto células nas quais PMM2 foi desligada apresentaram crescimento mais lento, menor migração e maior propensão a morrer.
Como as células tumorais turbinam o uso de açúcar
Quando a equipe reduziu os níveis de PMM2 em células de câncer colorretal, as células absorveram menos glicose, produziram menos ATP (sua principal moeda energética) e liberaram menos lactato, o resíduo da glicólise. Medições metabólicas sensíveis confirmaram que a acidificação global do meio ao redor diminuiu, enquanto o consumo de oxigênio aumentou, indicando que as células migraram da glicólise acelerada para uma respiração mais normal. Proteínas-chave auxiliares da glicólise, PKM2 e LDHA, também caíram. Surpreendentemente, mesmo uma versão cataliticamente “inativa” de PMM2 ainda podia impulsionar esse comportamento faminto por açúcar, mostrando que o papel da enzima no câncer não depende de sua química habitual, mas de com quem ela se liga dentro da célula.
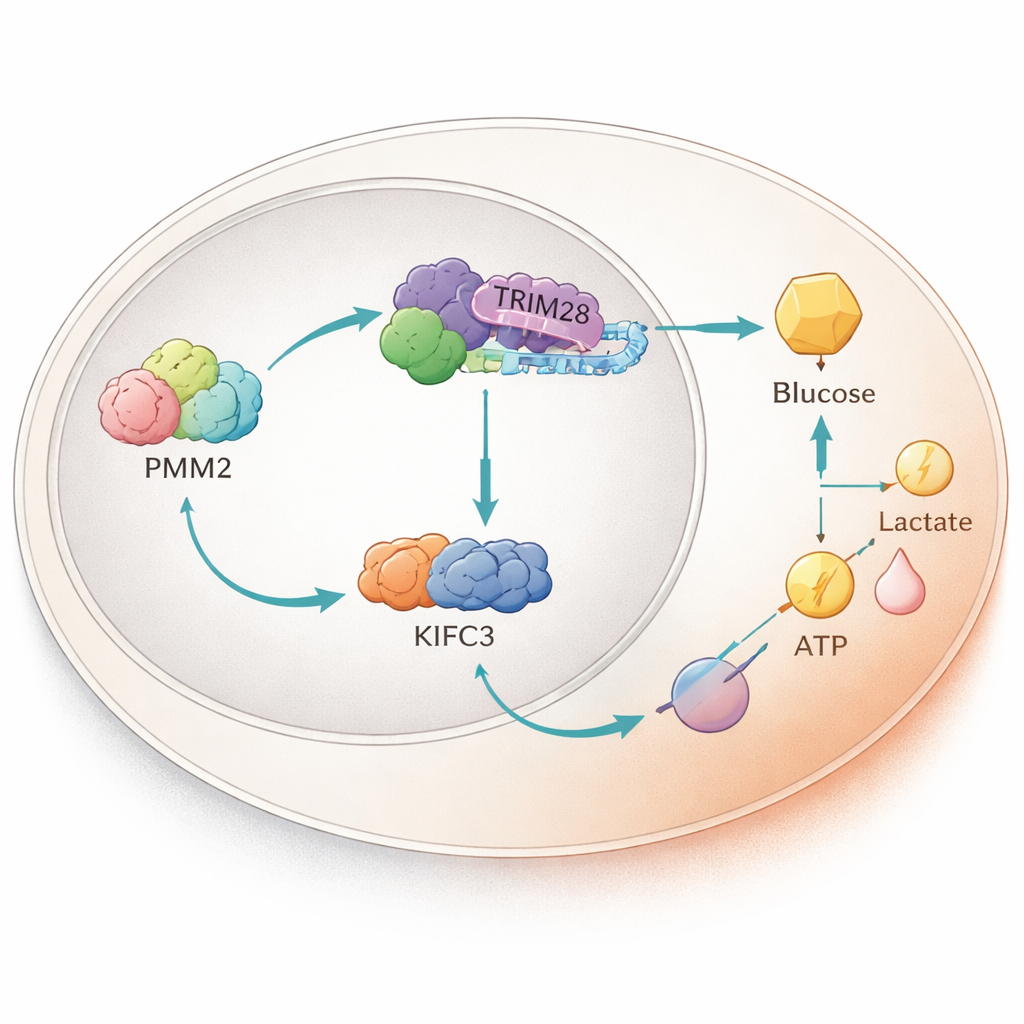
Um revezamento de proteínas dentro do núcleo
Aprofundando-se, os cientistas descobriram que PMM2 se liga fisicamente a outra proteína chamada TRIM28, que pode se mover para o núcleo celular e influenciar a atividade gênica. PMM2 ajuda TRIM28 a se acumular no núcleo, onde TRIM28 se junta a um fator de transcrição, E2F4. Juntos, esse trio aumenta a produção de uma proteína motora chamada KIFC3 ao se ligar a uma região específica do controle de DNA desse gene. Experimentos que deletaram a região de PMM2 necessária para a ligação com TRIM28 aboliram a capacidade da PMM2 de aumentar a glicólise e o crescimento celular, ressaltando que essa parceria de proteínas — e não a função enzimática clássica da PMM2 — é o que fornece a vantagem ao tumor.
Ligando um interruptor metabólico chave
KIFC3, mais conhecido por seu papel no transporte de cargas ao longo do andaime interno da célula, revelou-se um interruptor metabólico crucial. Quando os pesquisadores reduziram os níveis de KIFC3, as células de câncer colorretal consumiram menos glicose, produziram menos ATP e lactato, e apresentaram atividade glicolítica mais fraca, enquanto o uso de oxigênio aumentou. Importante, silenciar KIFC3 anulou parcialmente o aumento da glicólise e a vantagem de crescimento normalmente causados pela PMM2. Em camundongos implantados com células humanas de câncer colorretal, tumores com excesso de PMM2 cresceram mais, mas esse efeito foi atenuado quando KIFC3 foi silenciado. Amostras tumorais desses animais mostraram níveis elevados de PMM2, KIFC3 e marcadores de glicólise, conectando toda a cadeia de eventos em tecido vivo.
De modelos de laboratório a amostras de pacientes
Para aproximar o trabalho da clínica, a equipe criou mini tumores tridimensionais, conhecidos como organoides, a partir de cânceres colorretais de pacientes. Organoides com níveis mais altos de PMM2 e KIFC3 cresceram mais rápido e produziram mais ATP e lactato do que aqueles com níveis menores. Forçar organoides a expressar mais PMM2 aumentou KIFC3 e a glicólise, enquanto reduzir PMM2 teve os efeitos opostos. Análises de matrizes de tumores de pacientes mostraram ainda que níveis elevados de PMM2 estavam associados a doença mais avançada, disseminação para linfonodos e sobrevivência global mais curta, apontando PMM2 como um forte candidato a biomarcador.
O que isso significa para o cuidado futuro
Em termos simples, este estudo mostra que muitos tumores colorretais parecem conectar a PMM2 a um revezamento de proteínas nucleares — por meio de TRIM28 e E2F4 — para aumentar KIFC3 e, por consequência, sua maquinaria de queima de açúcar. Essa onda metabólica ajuda os cânceres a crescer e se espalhar. Como essa via depende de interações entre proteínas em vez da atividade enzimática habitual da PMM2, ela abre novas possibilidades terapêuticas: pequenas moléculas, peptídeos ou fármacos degradadores que interrompam a ligação de PMM2 a TRIM28, bloqueiem o acesso de E2F4 ao DNA ou reduzam a atividade de KIFC3 poderiam, em princípio, privar os tumores de seu combustível preferido. Embora tais tratamentos ainda não estejam disponíveis, a cadeia PMM2–TRIM28–E2F4–KIFC3 agora se destaca como um roteiro promissor para estratégias mais precisas e focadas no metabolismo contra o câncer colorretal.
Citação: Peng, Z., Ma, B., Song, Z. et al. PMM2 interacts with TRIM28 to recruit E2F4 and promote KIFC3-mediated tumor glycolysis and colorectal cancer progression. Oncogene 45, 1145–1160 (2026). https://doi.org/10.1038/s41388-026-03707-x
Palavras-chave: câncer colorretal, metabolismo tumoral, glicólise, sinalização oncogênica, biomarcador