Clear Sky Science · pt
Associação entre retinoides, receptores de ácido retinoico e epigenética no câncer de mama
Por que a vitamina A importa para o câncer de mama
A maioria das pessoas conhece a vitamina A como um nutriente importante para a visão, mas sua forma ativa no organismo, o ácido retinoico, também ajuda as células a decidir se devem crescer, se especializar ou se autodestruir quando danificadas. Este artigo de revisão examina como o ácido retinoico e suas “estações de ancoragem” celulares são alterados no câncer de mama, por que resultados promissores em laboratório ainda não se traduziram em medicamentos eficazes para pacientes e como novas percepções sobre o “software” da célula cancerosa — seu código epigenético — podem reviver essa estratégia terapêutica.
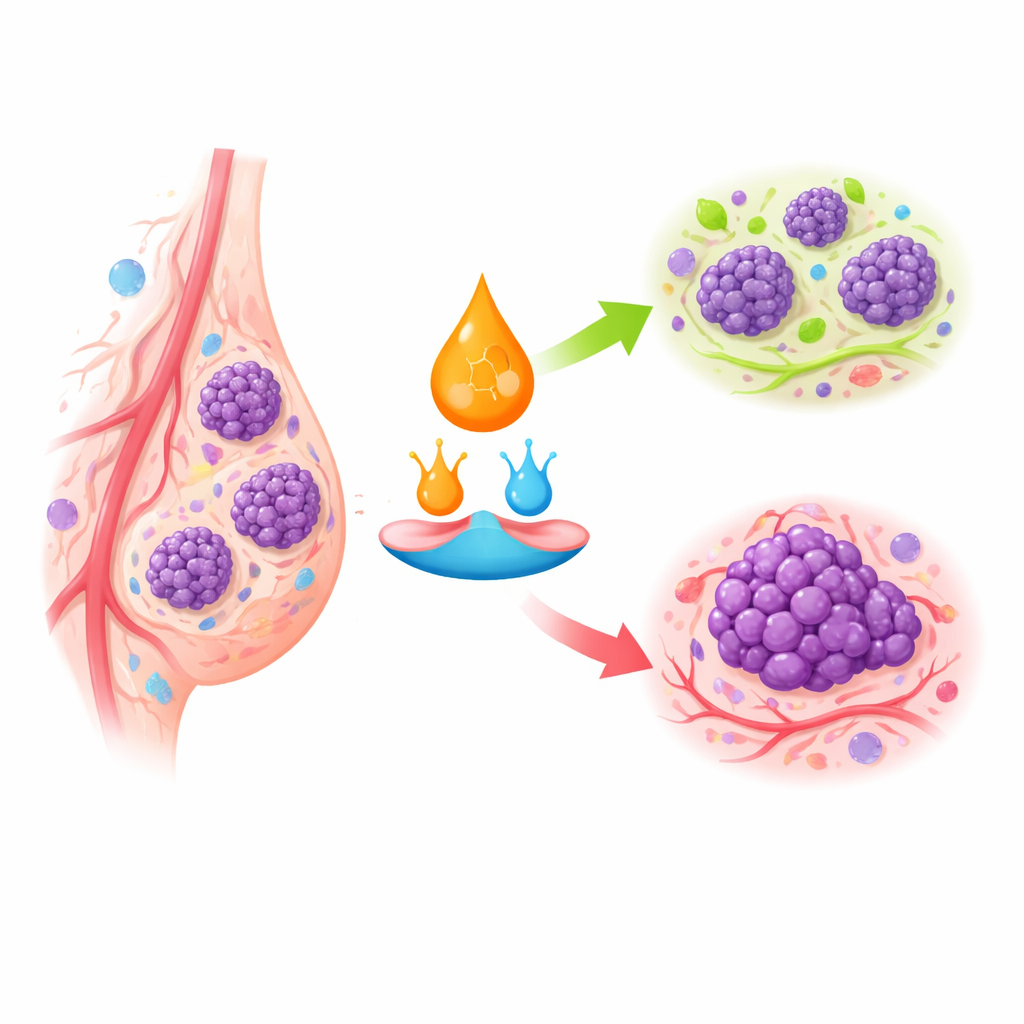
Sinais de trânsito celulares para crescimento e autodestruição
O ácido retinoico age ligando‑se a receptores específicos dentro das células, que então ligam ou desligam conjuntos inteiros de genes. No tecido mamário saudável, esse sistema incentiva as células a parar de se dividir, amadurecer em formas estáveis ou morrer se se tornarem anormais. No câncer de mama, especialmente nos subtipos mais agressivos, receptores chave estão ausentes ou silenciados, e o transporte interno do ácido retinoico é redirecionado. Em vez de ser entregue a receptores que freiam o crescimento, pode ser desviado para vias que favorecem sobrevivência e proliferação. Isso ajuda a explicar por que alguns tumores mamários respondem pouco aos medicamentos retinoides, embora os mesmos fármacos sejam altamente eficazes em certos cânceres hematológicos.
Interruptores ocultos no software da célula cancerosa
Os autores concentram‑se na epigenética — marcas químicas no DNA e nas proteínas de sua embalagem que funcionam como configurações de software para o genoma. Em muitos cânceres de mama, essas marcas travam receptores importantes do ácido retinoico, especialmente um chamado RARβ2, na posição “desligado” sem alterar a sequência subjacente do DNA. Grupos metil adicionais no DNA e o apertamento do enrolamento proteico fecham esse receptor, enquanto outras enzimas remodelam o panorama da cromatina para favorecer crescimento e migração. RNAs não codificadores, que não produzem proteínas mas influenciam a atividade gênica, ainda deslocam mais o sinal para longe da morte celular e da diferenciação. Juntas, essas alterações conferem às células cancerosas flexibilidade para resistir ao tratamento e adaptar‑se ao estresse.
Reprogramando as vias de sinalização
É importante que esses bloqueios epigenéticos sejam reversíveis. Em modelos laboratoriais, fármacos que removem a metilação do DNA ou afrouxam a cromatina podem restaurar o RARβ2 e outros componentes da via do ácido retinoico. Quando combinados com o próprio ácido retinoico e quimioterapia padrão, esses agentes de “preparação” reduzem tumores de forma mais eficaz e diminuem o reservatório de células com características de células‑tronco, suspeitas de alimentar recidivas. A forma como o ácido retinoico é transportado dentro da célula também importa: uma proteína transportadora o direciona para receptores supressores de crescimento, enquanto outra o entrega a vias pró‑crescimento. Ajustar o equilíbrio entre esses transportadores pode transformar o ácido retinoico de um “adubo” em um “freio”.
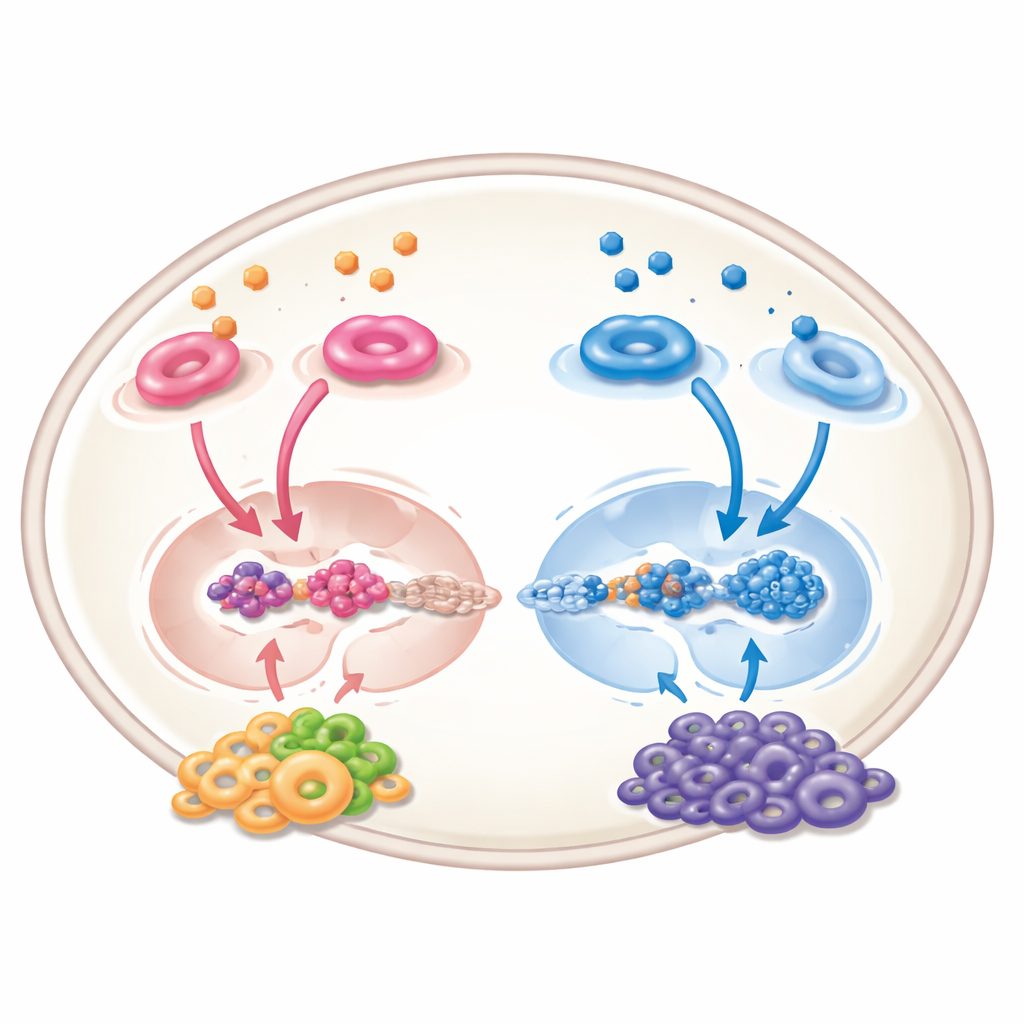
Além do tumor: o efeito do bairro
O ácido retinoico não age apenas nas células tumorais; ele também remodela o “bairro” ao redor do tumor — vasos sanguíneos, células imunes e células de suporte. Em sistemas experimentais, pode reduzir a formação de novos vasos, direcionar células imunes para um estado mais ativo e antitumoral, e limitar células supressoras que normalmente atenuam as defesas do organismo. Ainda assim, a história não é inteiramente positiva: em certos tipos de células do estroma que cercam o tumor, a ativação da sinalização do ácido retinoico pode, na verdade, promover o crescimento canceroso ao fortalecer canais de comunicação química que atraem e sustentam células malignas. Esses efeitos opostos significam que qualquer terapia futura deve ser cuidadosamente ajustada para atingir os tipos celulares corretos da maneira correta.
Desenhando ensaios mais inteligentes para o futuro
Ensaios clínicos iniciais com retinoides no câncer de mama fracassaram em grande parte, mas foram realizados antes do entendimento atual sobre subtipos, biomarcadores e farmacologia complexa. Os autores defendem que novos ensaios devem selecionar pacientes cujos tumores exibam as marcas moleculares de sensibilidade aos retinoides, como expressão preservada de receptores ou padrões específicos de metilação do DNA, e devem combinar retinoides com fármacos que desbloqueiem barreiras epigenéticas, atinjam vias de crescimento ou aumentem o ataque imune. Formulações melhoradas que mantenham níveis estáveis do fármaco no organismo, juntamente com monitoramento cuidadoso do tumor e do tecido circundante, serão cruciais. Se esses obstáculos puderem ser superados, tratamentos à base de ácido retinoico ainda poderão encontrar um papel como ferramentas de precisão contra formas selecionadas de câncer de mama.
Citação: Szymański, Ł., Schenk, T., Ławiński, M. et al. Association of retinoids, retinoic acid receptors and epigenetics in breast cancer. Oncogene 45, 961–970 (2026). https://doi.org/10.1038/s41388-026-03699-8
Palavras-chave: ácido retinoico, câncer de mama, epigenética, terapia de diferenciação, microambiente tumoral