Clear Sky Science · pt
Modelando a comunicação entre tecido adiposo e câncer: uma perspectiva tridimensional
Por que a gordura e o câncer estão mais próximos do que você imagina
A maioria de nós pensa na gordura corporal como um acolchoamento extra ou energia estocada, mas pesquisas revelam que ela é um órgão ativo e comunicativo que pode moldar nossa saúde de maneiras surpreendentes. Este artigo de revisão explora como o tecido adiposo e as células cancerosas se comunicam, e como novos modelos laboratoriais tridimensionais (3D) ajudam os cientistas a imitar esse diálogo de forma mais realista do que nunca. Entender essa conversa oculta pode melhorar a prevenção do câncer, os testes de medicamentos e os tratamentos, especialmente em um mundo cada vez mais com excesso de peso. 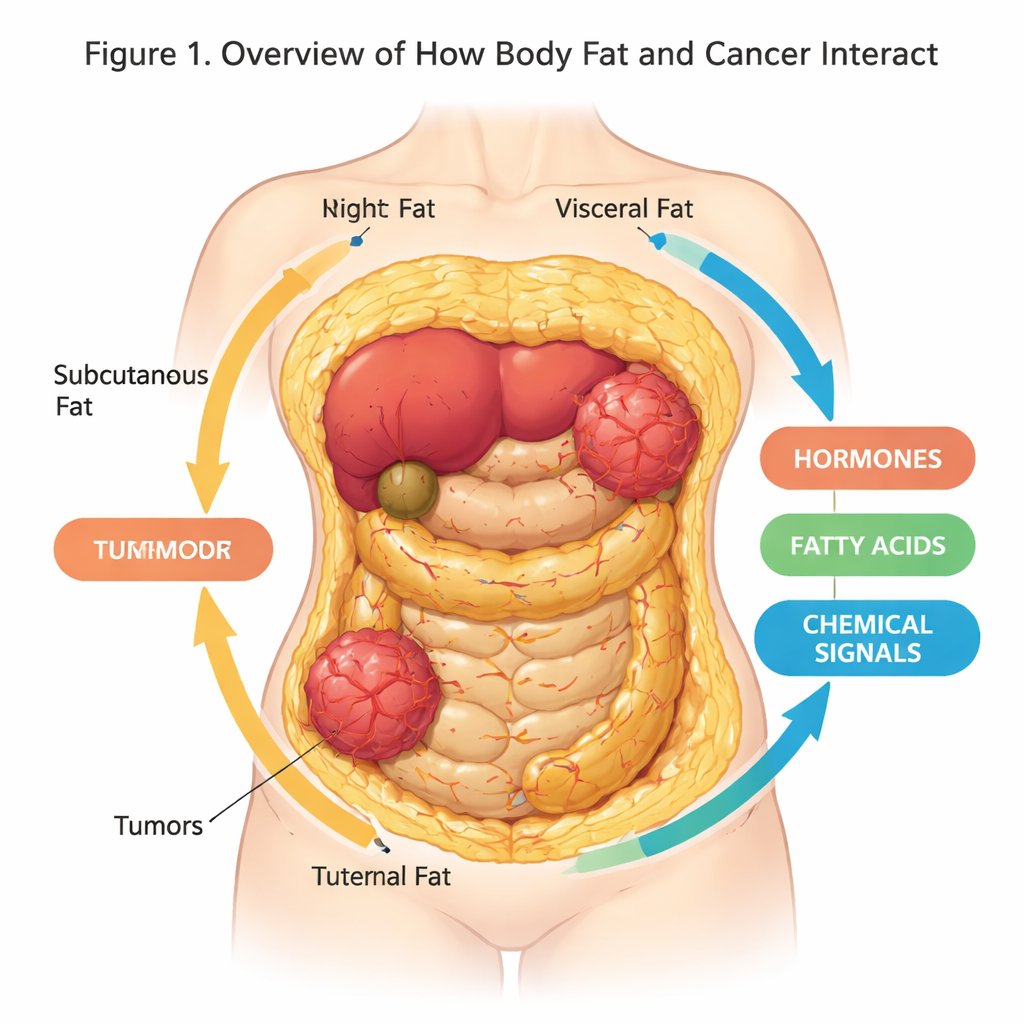
A gordura como um órgão vivo e comunicativo
O tecido adiposo — nossa gordura corporal — não é apenas um local passivo de armazenamento. É um órgão complexo composto por adipócitos, células imunes, vasos sanguíneos e células de suporte, todos inseridos em uma malha estrutural conhecida como matriz extracelular. Diferentes tipos de gordura existem em locais distintos: gordura subcutânea sob a pele, gordura visceral ao redor dos órgãos internos, e adipócitos brancos, marrons e bege que variam na forma como armazenam energia ou a queimam como calor. Essas células liberam constantemente um coquetel de hormônios, ácidos graxos e proteínas sinalizadoras que influenciam o metabolismo, a inflamação e, como sabemos agora, o risco e o comportamento do câncer.
Obesidade, inflamação e risco de câncer
Quando ganhamos peso demais, os adipócitos brancos aumentam de tamanho e número e o tecido fica estressado e inflamado. Essa gordura “não saudável” libera mais moléculas inflamatórias e ácidos graxos na corrente sanguínea, enquanto processa açúcar e gordura de forma menos eficiente. Grandes estudos epidemiológicos relacionaram a obesidade a maior risco e piores desfechos em muitos cânceres, incluindo mama, cólon, pâncreas e útero. A revisão explica como a gordura disfuncional pode abastecer tumores com combustível extra, tornar o tecido circundante mais rígido e recrutar outros tipos celulares que, juntos, criam um ambiente mais favorável ao câncer.
Uma conversa bidirecional entre gordura e tumores
O câncer é hoje visto como uma doença de um ecossistema inteiro, não apenas de células descontroladas. As células tumorais se aproveitam da gordura próxima para obter suporte, reprogramando adipócitos, células imunes e fibroblastos para ajudá-las a crescer e se espalhar. Em contrapartida, os adipócitos respondem quebrando lipídios armazenados e liberando ácidos graxos e hormônios que as células cancerosas podem usar prontamente. Essa comunicação pode ocorrer à distância por sinais circulantes, ou localmente onde os tumores crescem ao lado da gordura, como na mama ou no abdômen. Células tumorais podem até induzir adipócitos a perder sua identidade original e tornarem‑se mais parecidos com células formadoras de cicatriz ou com fenótipo imune, que remodelam o tecido e promovem a invasão. 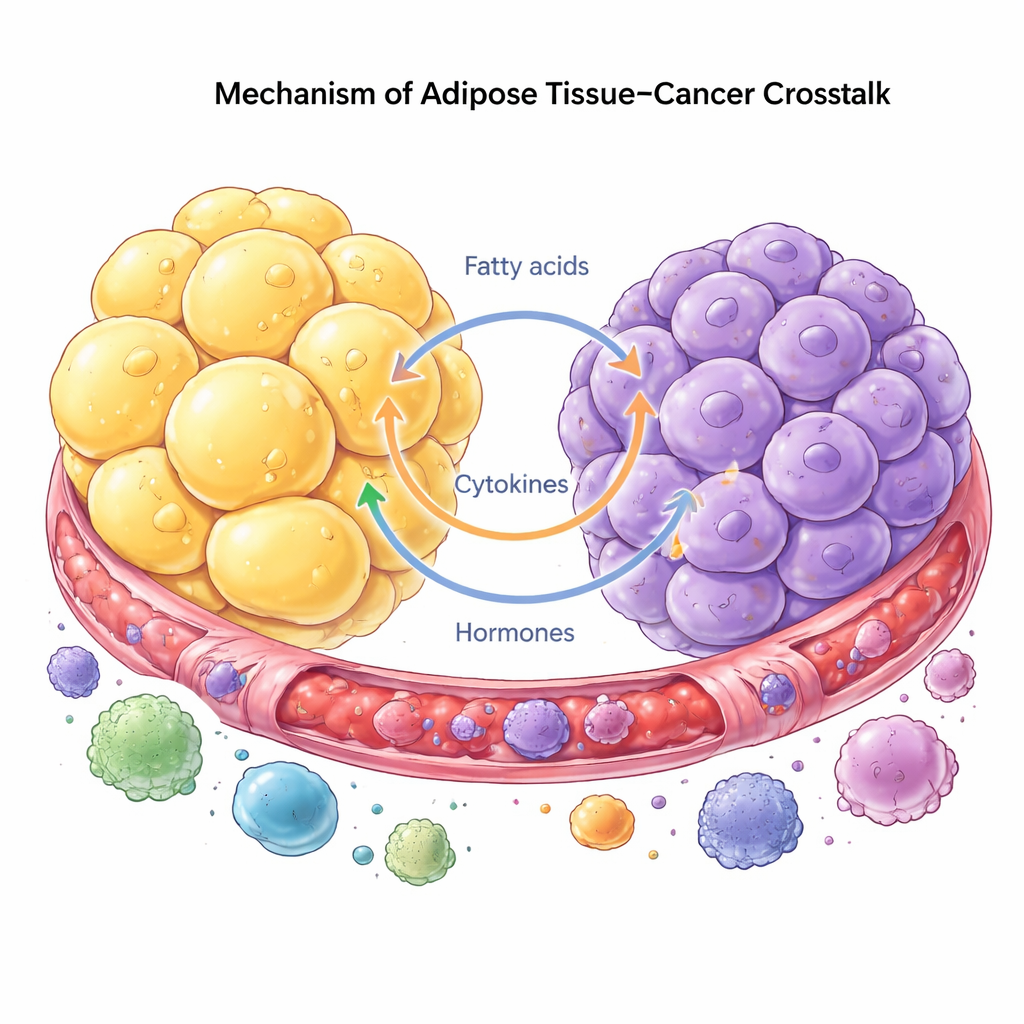
Construindo mini tecidos em 3D
Os tradicionais cultivos celulares planos (2D) e modelos animais frequentemente não capturam essas interações complexas. Os autores descrevem uma nova geração de sistemas 3D que se assemelham melhor ao tecido real. Esferoides são aglomerados celulares simples que se autoorganizam em pequenas esferas; scaffolds (andaimes) são materiais projetados que fornecem suporte 3D para o crescimento celular; organoides são versões miniaturizadas e autoorganizadas de tecidos; e assembloides combinam múltiplos organoides ou esferoides em “mini‑órgãos” compostos. Pesquisadores estão agora usando essas abordagens 3D para co‑cultivar adipócitos e células cancerosas, estudar como condições semelhantes à obesidade alteram seu comportamento e testar como medicamentos podem interromper o diálogo prejudicial entre eles.
Promessas e lacunas atuais
Cada modelo oferece compensações. Esferoides são baratos e de alto rendimento, mas relativamente simples. Scaffolds permitem controle rigoroso de propriedades físicas como rigidez, que pode influenciar a disseminação do câncer, mas são mais exigentes tecnicamente. Organoides e assembloides capturam o maior nível de realismo, com múltiplos tipos celulares interagindo, porém são caros, difíceis de padronizar e frequentemente carecem de redes vasculares completas ou componentes imunes. A revisão enfatiza que os sistemas atuais ainda ficam aquém de reproduzir perfeitamente o tecido adiposo e tumoral humano, particularmente ao replicar plenamente a matriz extracelular, adipócitos maduros e a participação das células imunes.
Para onde vai essa pesquisa
Os autores concluem que melhorar os modelos 3D das interações gordura–câncer é essencial para testes de drogas mais precisos e para desvendar como a obesidade promove o câncer. À medida que esses “mini‑tecidos” se tornam mais realistas — combinando gordura verossímil, células tumorais, vasos sanguíneos e células imunes — eles poderão ajudar pesquisadores a prever quais tratamentos funcionarão em pacientes específicos, desenhar melhores estratégias para bloquear o uso da gordura corporal como combustível pelo câncer e, em última instância, orientar terapias que visem não apenas os tumores, mas os ambientes disfuncionais que os ajudam a prosperar.
Citação: Strusi, G., Suelzu, C.M. & Stebbing, J. Modelling adipose tissue-cancer crosstalk: a three-dimensional perspective. Oncogene 45, 905–913 (2026). https://doi.org/10.1038/s41388-026-03697-w
Palavras-chave: tecido adiposo, obesidade, microambiente tumoral, cultivo celular 3D, metabolismo tumoral