Clear Sky Science · pt
POM121 O-GlcNAcilação facilita metástase óssea em câncer de pulmão não pequenas células por meio do aumento da importação nuclear de c-MYC e reprogramação da matriz extracelular
Por que esta pesquisa importa
Quando o câncer de pulmão se espalha para os ossos, causa dor intensa, fraturas e reduz drasticamente a sobrevida, e ainda assim os médicos dispõem de poucas ferramentas para impedir esse passo letal. Este estudo investiga os mecanismos internos das células de câncer de pulmão para descobrir como algumas delas ganham uma vantagem especial que lhes permite viajar do pulmão ao osso e prosperar ali. Ao rastrear esse processo até pequenas modificações em uma única proteína porteira na borda do núcleo celular, os autores identificam uma nova cadeia de eventos que pode ser alvo para melhor prever, prevenir ou tratar metástases ósseas em pacientes com câncer de pulmão não pequenas células.
Uma etiqueta de açúcar que altera o comportamento do câncer
Os pesquisadores concentraram-se em modificações pós-traducionais, pequenas alterações químicas que as proteínas adquirem depois de sintetizadas. Uma dessas alterações, chamada O-GlcNAcilação, é a adição de um pequeno açúcar a pontos específicos das proteínas. Usando linhagens de células de câncer de pulmão e modelos em camundongos, a equipe comparou células tumorais comuns com subpopulações selecionadas repetidamente por sua capacidade de colonizar os ossos. Eles descobriram que essas células com afinidade óssea apresentavam níveis gerais de O-GlcNAcilação muito mais altos, impulsionados por aumento da atividade da enzima OGT, que instala essa etiqueta de açúcar. Entre centenas de proteínas modificadas, uma se destacou: POM121, um componente central do poro nuclear, a estrutura que controla o tráfego para dentro e fora do núcleo celular.
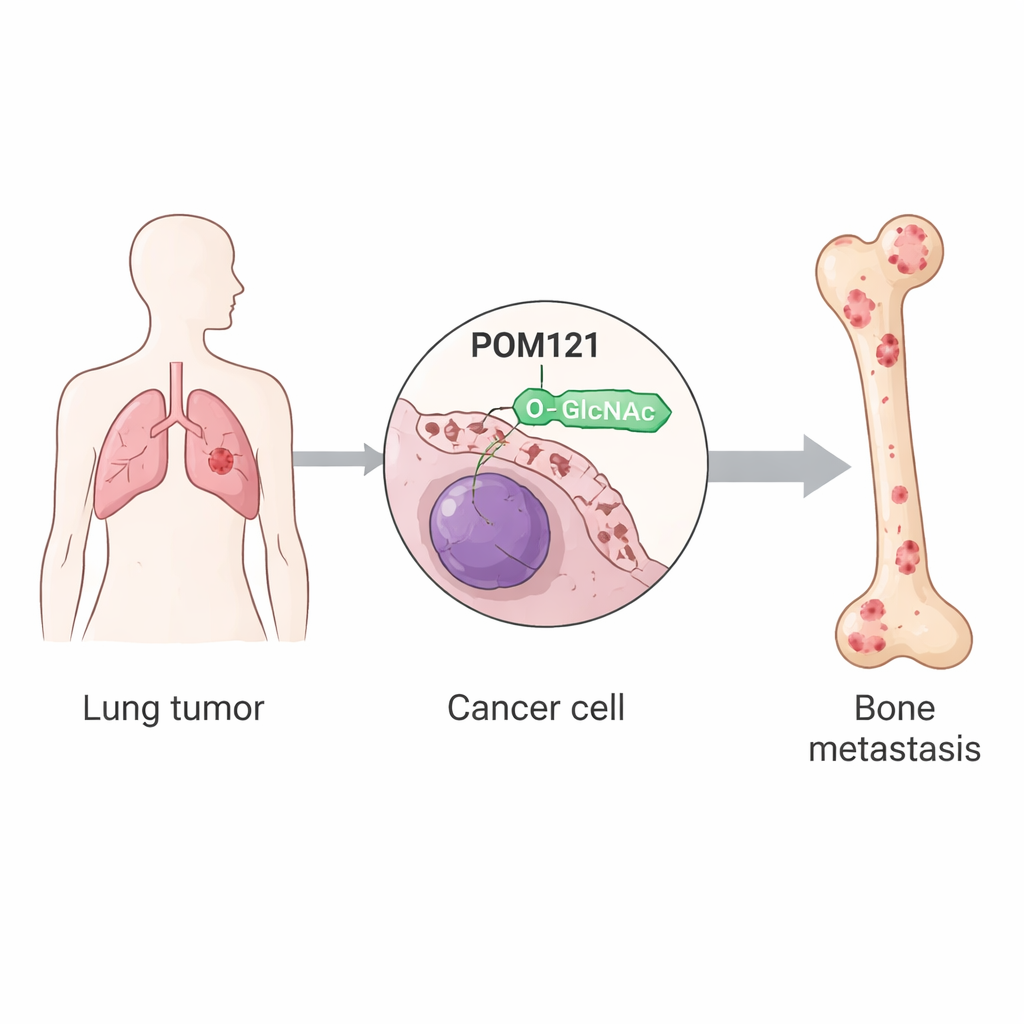
O porteiro nuclear POM121 é estabilizado
POM121 situa-se na membrana que envolve o núcleo, formando parte do canal pelo qual muitas proteínas de sinalização devem passar. Em células de câncer de pulmão metastáticas aos ossos, POM121 carregava uma alta carga de O-GlcNAc em uma única posição de aminoácido chamada serina 199. Quando esse sítio foi alterado de modo que não pudesse mais ser modificado, a proteína tornou-se instável e foi rapidamente degradada pelas vias de descarte da célula. O estudo mostra que a etiqueta de açúcar protege POM121 de ser marcada para destruição por uma enzima chamada TRIM21, que normalmente anexa rótulos de ubiquitina para eliminação. Com a O-GlcNAc presente, o TRIM21 não se liga bem, a ubiquitinação diminui e POM121 se acumula no poro nuclear sem mudar sua localização.
Abrindo a porta para um potente impulsionador do câncer
Que diferença faz um POM121 extraestável? A chave está em uma famosa proteína promotora de câncer, o fator de transcrição c-MYC. c-MYC precisa entrar no núcleo para ativar genes, mas sua passagem depende de componentes do poro nuclear como POM121. Os autores mostraram que, quando POM121 era abundante e O-GlcNAcilado, mais c-MYC estava presente dentro do núcleo; quando os níveis de POM121 foram reduzidos ou sua etiqueta de açúcar removida, a importação nuclear de c-MYC caiu acentuadamente. Em camundongos, células de câncer de pulmão com a mutação de POM121 não modificável formaram muito menos e menores metástases ósseas, enquanto restaurar c-MYC em células deficientes em POM121 recuperou grande parte de seu poder de colonização óssea. Isso posiciona POM121 a montante de c-MYC em uma via metastática crítica.
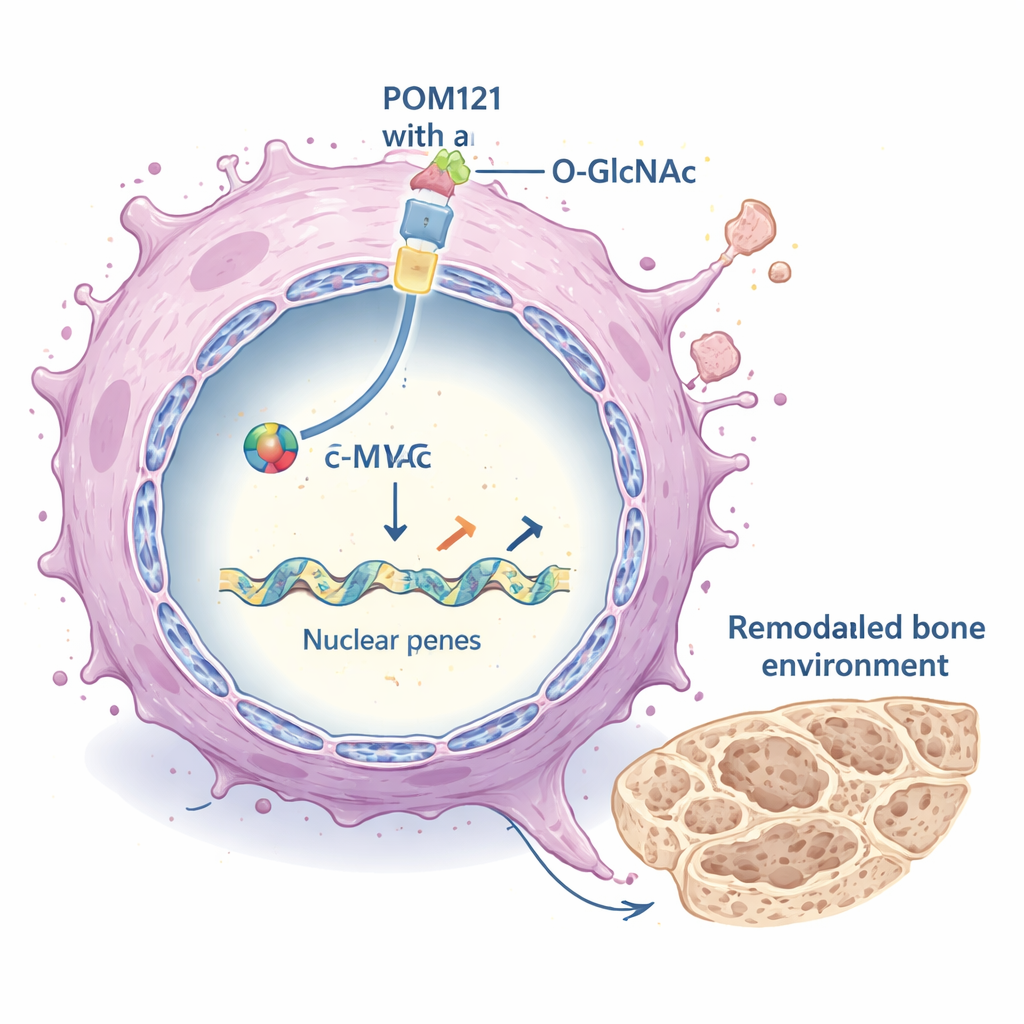
Reprogramando o ambiente tumoral
Uma vez dentro do núcleo, c-MYC atua como um interruptor mestre para muitos genes. Aqui, constatou-se que ele ativava fortemente um conjunto de genes que moldam a matriz extracelular (MEC) – o arcabouço de proteínas que envolve as células. Esses genes da MEC, que incluem vários colágenos e enzimas que remodelam a estrutura tecidual, foram reduzidos quando POM121 ou c-MYC foram bloqueados, e aumentaram quando a O-GlcNAcilação e POM121 estavam altas. A MEC alterada, por sua vez, potencializou vias de crescimento importantes dentro das células cancerosas, notadamente a cascata de sinalização PI3K–AKT–mTOR, que sustenta sobrevivência, crescimento e disseminação. Padrões semelhantes apareceram em diversos modelos de câncer de pulmão, sugerindo que esse mecanismo não está limitado a uma única linhagem celular.
Da descoberta em laboratório ao impacto para pacientes
Ao analisar dados de pacientes, os pesquisadores encontraram que altos níveis de OGT, POM121 e c-MYC, assim como dos genes da MEC que eles regulam, estavam relacionados a piores desfechos e a tumores pulmonares que já haviam se espalhado para os ossos. Em conjunto, o trabalho delineia um eixo OGT–POM121–c-MYC–MEC: a O-GlcNAcilação extra estabiliza o porteiro nuclear POM121, que transporta mais c-MYC para o núcleo, que então reprograma o arcabouço tecidual e os sinais de crescimento para favorecer a metástase óssea. Para os pacientes, isso sugere novos tipos de biomarcadores para sinalizar quem está em risco de disseminação óssea e novas abordagens terapêuticas – desde bloquear a função de OGT ou POM121 até atenuar c-MYC ou a remodelação da MEC – que um dia podem ajudar a impedir que o câncer de pulmão alcance o esqueleto.
Citação: Ren, YZ., Zhao, MN., Du, FL. et al. POM121 O-GlcNAcylation facilitates bone metastasis in non-small cell lung cancer through enhanced c-MYC nuclear import and ECM reprogramming. Oncogene 45, 728–743 (2026). https://doi.org/10.1038/s41388-026-03687-y
Palavras-chave: metástase óssea câncer de pulmão, POM121, O-GlcNAcilação, c-MYC, matriz extracelular