Clear Sky Science · pt
RO4938581, um modulador alostérico negativo de GABAA-α5 resgatou fenótipos comportamentais e de EEG em um modelo murino da síndrome Dup15q
Por que esta pesquisa cerebral importa
A síndrome Dup15q é uma condição genética rara que frequentemente causa autismo, crises epilépticas e dificuldades sérias de aprendizagem. As famílias dispõem de pouco além de cuidados de suporte, e não existe tratamento que ataque a biologia subjacente. Este estudo usou camundongos que carregam o mesmo segmento extra de DNA presente em pessoas com Dup15q para investigar o que dá errado no cérebro — e para testar se um fármaco experimental altamente direcionado pode reduzir esse problema. O trabalho destaca um tipo específico de receptor cerebral como um alvo promissor e testável para futuras terapias de precisão.
Excesso de freio no cérebro
Nossos cérebros dependem de um equilíbrio delicado entre sinais de “vai” que excitam neurônios e sinais de “pare” que os acalmam. Na síndrome Dup15q, um trecho do cromossomo 15 é duplicado. Essa região inclui três genes que codificam partes de um receptor chave de “pare” no cérebro, chamado receptor GABAA, especialmente uma variante que contém uma subunidade chamada alfa-5. Os pesquisadores criaram camundongos com o mesmo tipo de duplicação e descobriram que esses animais produziram cerca de 50% a mais dos receptores contendo alfa-5 em regiões cerebrais importantes para memória, emoção e movimento, incluindo o hipocampo e o córtex. Múltiplos métodos — desde expressão gênica até imagem de receptores — convergiram na mesma conclusão: esse sistema de freio particular está excessivamente desenvolvido no modelo Dup15q.
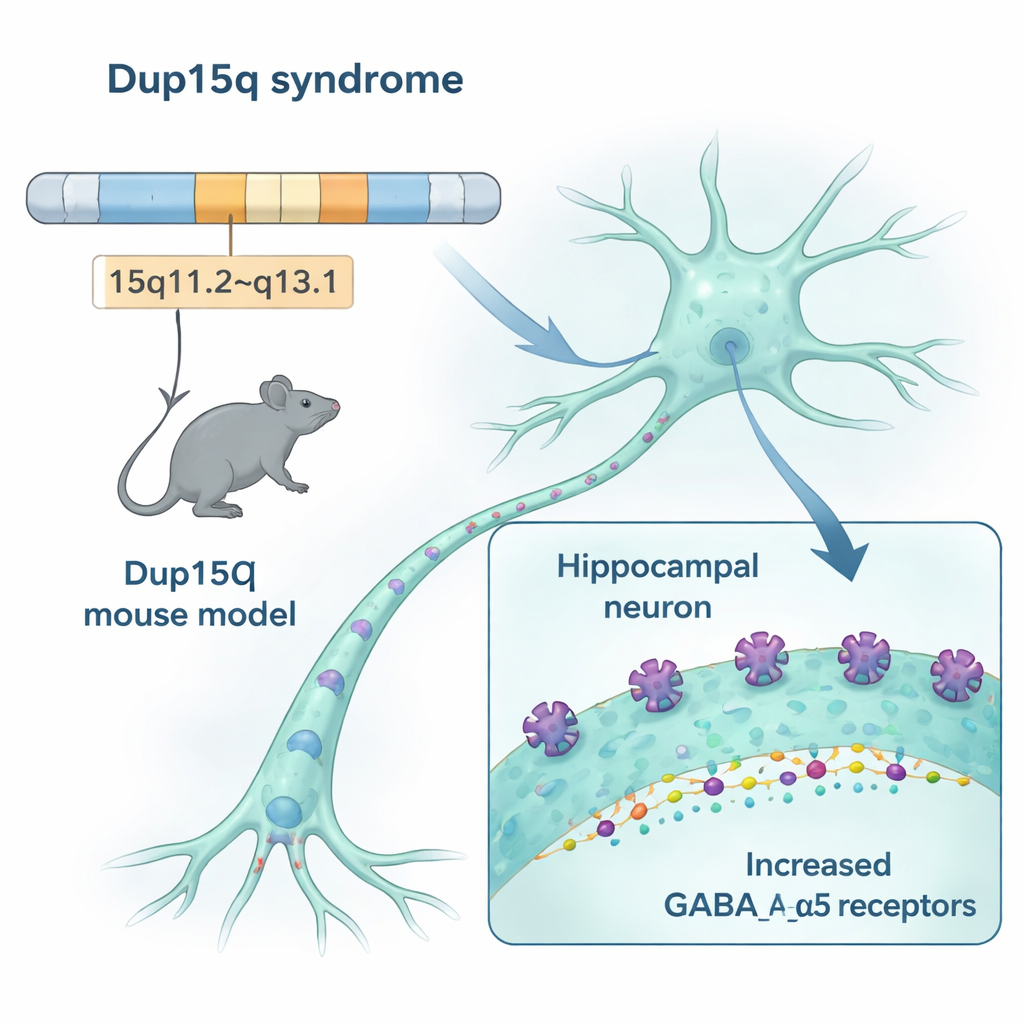
Como receptores extras alteram os sinais cerebrais
Ter mais receptores de inibição só importa se isso realmente muda como os circuitos disparam. Em fatias finas do hipocampo, a equipe mediu as pequenas correntes elétricas que neurônios inibitórios enviam a outras células. Nos camundongos Dup15q, essas correntes inibitórias ocorreram com maior frequência, sugerindo que os neurônios experimentavam um freio contínuo mais forte, mesmo que a amplitude de cada sinal individual não tenha mudado. Um teste separado do comportamento de circuito, chamado inibição por pulso pareado, também mostrou que as redes nesses camundongos eram mais fortemente amortecidas do que as de seus irmãos saudáveis. Em conjunto, os dados indicam que os receptores extras tornam os circuitos inibitórios mais dominantes, deslocando o equilíbrio para longe do processamento flexível de informação.
Comportamento e ondas cerebrais em camundongos afetados
Os cientistas então investigaram se essa fiação alterada se traduzia em comportamentos que ecoam sintomas humanos. Em uma série de testes, os camundongos Dup15q mostraram indícios de diferenças sociais e de comunicação e, de forma mais clara, dificuldade com flexibilidade cognitiva. Em uma tarefa no labirinto aquático, tanto camundongos normais quanto Dup15q aprenderam onde havia uma plataforma escondida. Mas quando a plataforma foi movida, os animais Dup15q foram lentos para abandonar a localização antiga e se adaptar à nova — um paralelo de laboratório às rotinas rígidas frequentemente observadas no autismo. A equipe também registrou sinais de eletroencefalografia (EEG), os ritmos somados de muitos neurônios. Como em pessoas com Dup15q, os camundongos exibiram atividade anormalmente forte na faixa beta, um ritmo rápido frequentemente aumentado por drogas que potencializam receptores GABAA, reforçando a ideia de que seu sistema inibitório estava hiperativo.
Um fármaco direcionado que afrouxa os freios
Para ver se podiam normalizar esse excesso de freio, os pesquisadores recorreram ao RO4938581, um composto experimental que enfraquece seletivamente receptores GABAA do tipo alfa-5 sem afetar outras formas. Em fatias do hipocampo, a droga reduziu a quantidade de transferência de carga inibitória em neurônios Dup15q, contrariando o freio excessivo. Administrado por via oral diariamente por várias semanas, o mesmo composto melhorou o desempenho dos animais na fase de reversão do labirinto aquático, permitindo que se ajustassem à plataforma movida de forma mais semelhante aos camundongos saudáveis. Também aproximou suas interações sociais do normal. Em gravações de EEG, uma dose aguda reduziu parcialmente a potência beta exagerada nos camundongos Dup15q, movendo seus ritmos cerebrais em direção ao padrão típico.
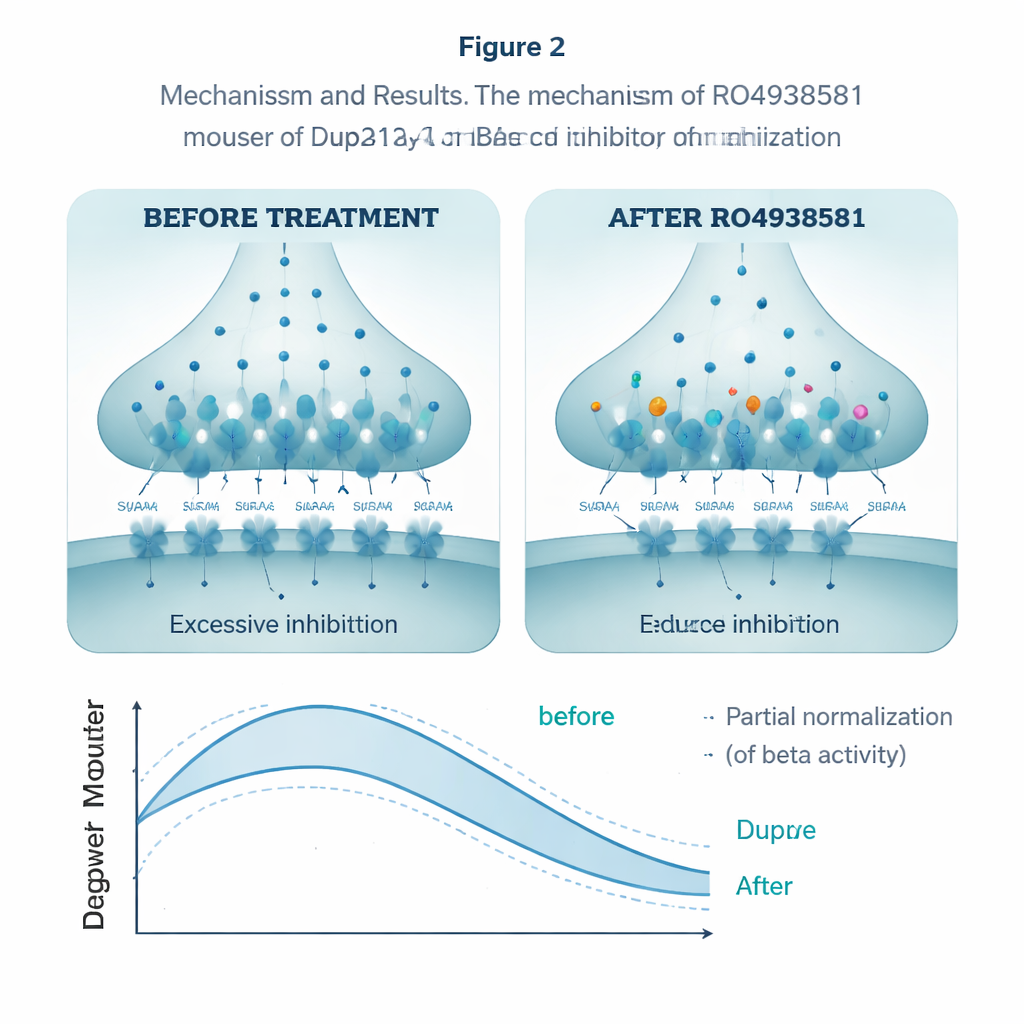
O que isso pode significar para tratamentos futuros
Para famílias que convivem com a síndrome Dup15q, esses achados não representam uma cura imediata, mas oferecem uma pista concreta. O trabalho identifica um subtipo específico de receptor — receptores GABAA que contêm a subunidade alfa-5 — como superproduzido e funcionalmente importante em um modelo animal relevante. Reduzir modestamente esse receptor com um modulador negativo como o RO4938581 não resolveu tudo, mas melhorou aprendizagem flexível, comportamento social e uma assinatura-chave no EEG. Essa combinação de mudanças no cérebro, no comportamento e em biomarcadores fortalece o argumento para testar fármacos mais seguros e aptos para humanos que visem a alfa-5 como tratamentos de precisão para Dup15q e possivelmente para condições neurodesenvolvimentais relacionadas.
Citação: Nakagawa, R., Nani, F., Hipp, J.F. et al. RO4938581, a GABAA-α5 negative allosteric modulator rescued behavioral and EEG phenotypes of a mouse model of Dup15q syndrome. Mol Psychiatry 31, 1351–1360 (2026). https://doi.org/10.1038/s41380-025-03247-y
Palavras-chave: síndrome Dup15q, receptor GABAA alfa-5, transtorno do neurodesenvolvimento, potência beta no EEG, modelo murino