Clear Sky Science · pt
Microfluídica inercial em cascata para enriquecimento em alta vazão e multiescala de células tumorais e aglomerados intactos visando diagnóstico aprimorado de malignidade
Por que ordenar células cancerosas em fluidos é importante
Quando o câncer se espalha, células tumorais frequentemente escapam para os fluidos que banham nossos órgãos. Em pessoas com câncer de pulmão, isso pode incluir o líquido que se acumula ao redor dos pulmões, chamado derrame pleural. Escondidas nesse fluido estão raras células tumorais individuais e aglomerados compactos de células. Esses aglomerados são considerados especialmente perigosos porque estão fortemente associados a doença agressiva e desfechos piores. Ainda assim, os métodos laboratoriais atuais têm dificuldade em isolar de maneira suave e eficiente tanto células únicas quanto aglomerados a partir de grandes volumes de fluido de pacientes. Este estudo apresenta uma nova tecnologia em chip que pode rapidamente e delicadamente separar essas células de derrames pleurais, abrindo caminho para diagnósticos de câncer mais confiáveis e melhor compreensão de como os tumores se espalham.
Um coador celular delicado em um chip
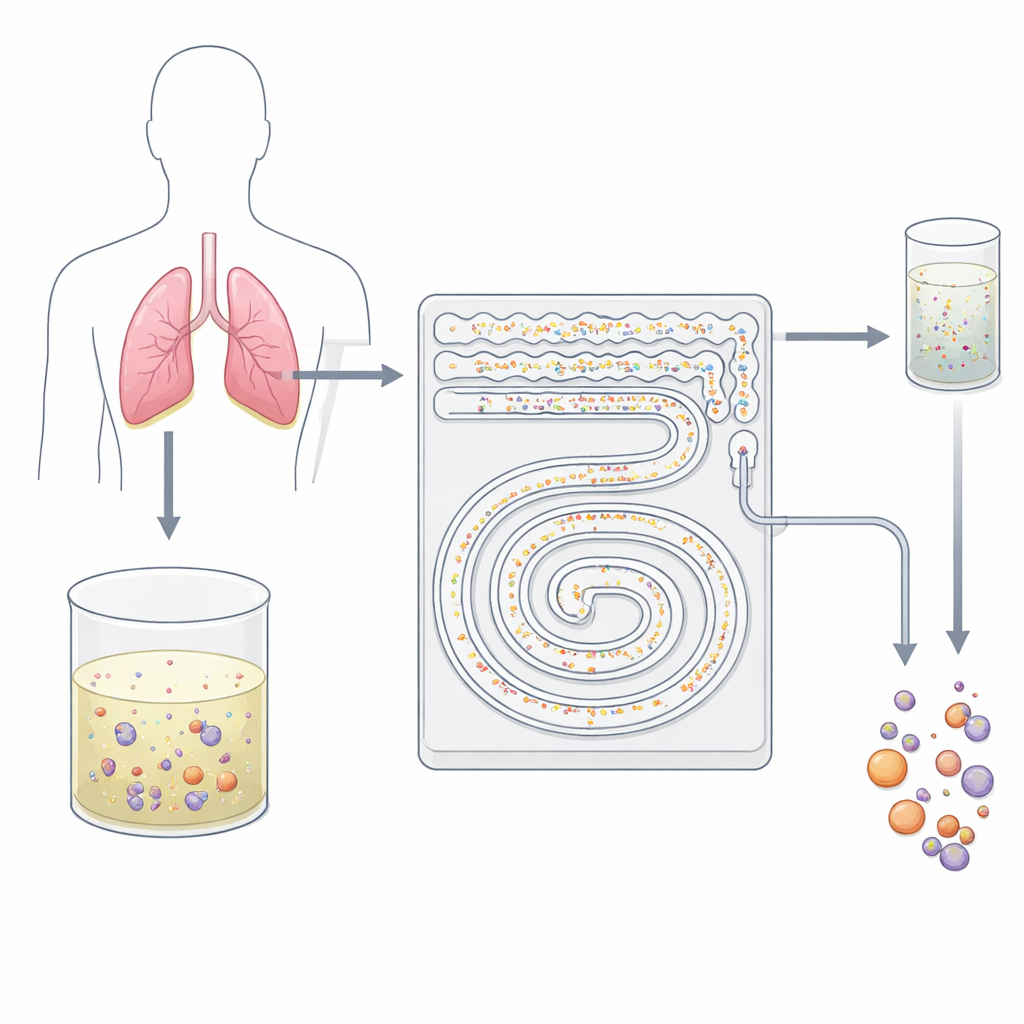
Os pesquisadores projetaram um dispositivo plástico do tamanho da palma da mão gravado com canais minúsculos que funcionam como um filtro inteligente de duas etapas. Em vez de usar anticorpos adesivos ou peneiramento agressivo, o chip depende do comportamento das células em fluxo rápido de líquido. À medida que o fluido passa por microcanais curvos, forças invisíveis empurram partículas de diferentes tamanhos para diferentes linhas de fluxo. A equipe tira proveito desse efeito, conhecido de forma geral como microfluídica inercial, para separar pequenas células sanguíneas de fundo de células tumorais maiores e seus aglomerados sem tocá-las ou rotulá-las. Como tudo acontece em um fluxo contínuo e fechado, o dispositivo consegue processar dezenas de mililitros de fluido em apenas minutos — algo que a citologia tradicional em lâminas não realiza facilmente.
Primeira etapa: desobstruindo a multidão
Na primeira fase do dispositivo, o derrame pleural — após remoção do excesso de líquido e ressuspensão das células — é impulsionado por uma matriz de canais serpentinos paralelos. Ali, o fluxo curvo e em redemoinho empurra pequenas células brancas em direção às paredes do canal, enquanto células tumorais maiores e aglomerados permanecem perto do centro do fluxo. As pequenas células são direcionadas para saídas de descarte, afinando dramaticamente o fundo. Essa etapa de alta vazão pode operar a cerca de 8 mililitros por minuto, o que significa que uma amostra clínica típica de 50 mililitros pode ser processada em aproximadamente seis minutos e meio sem entupimento. O que sai dessa primeira etapa é uma mistura muito mais limpa, enriquecida em células potencialmente malignas e pronta para uma separação mais refinada.
Segunda etapa: separando células únicas de aglomerados
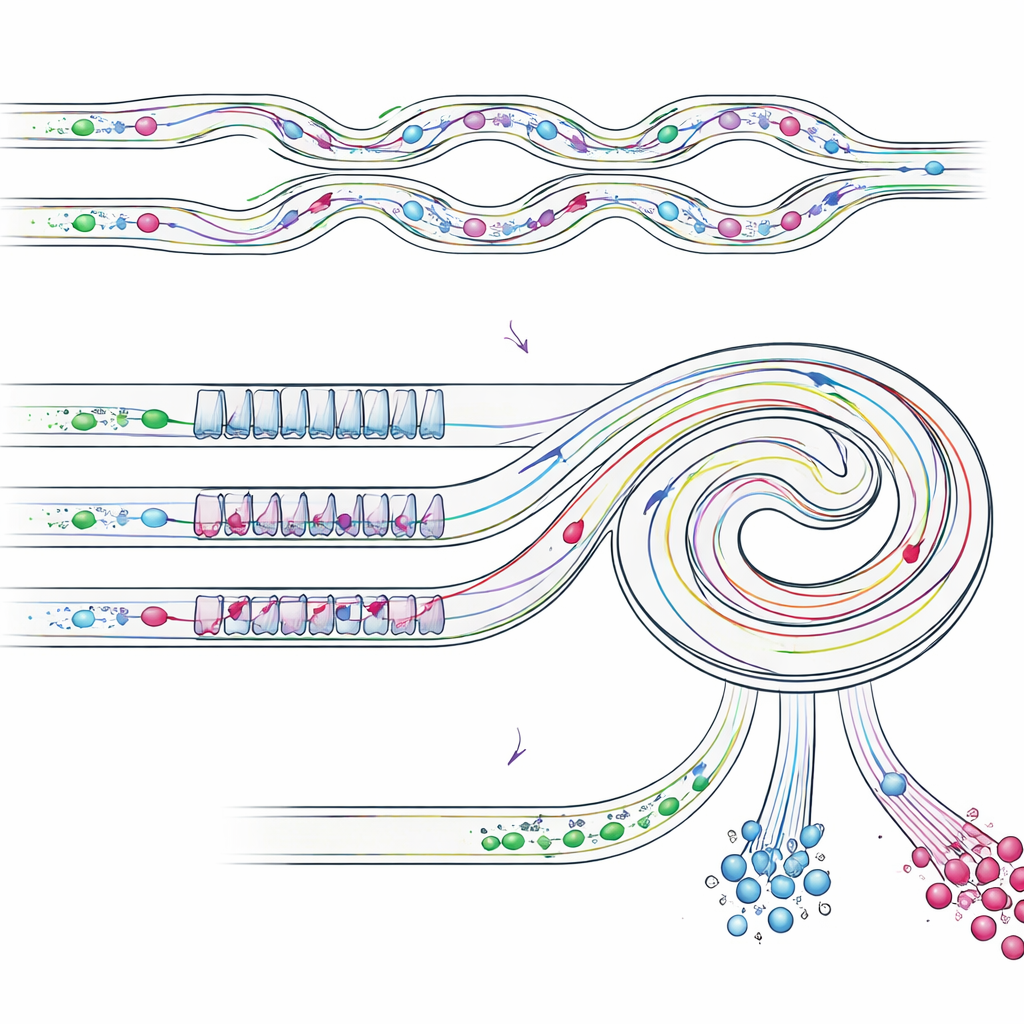
A amostra parcialmente enriquecida entra então em um canal espiral inclinado que inclui um padrão repetido de seções estreitas e largas. Nesta fase, várias forças de fluxo se equilibram de maneira diferente para objetos de tamanhos distintos, conduzindo-os para faixas separadas próximas à parede interna ou externa da espiral. Células tumorais individuais, menores, alinham-se em uma posição lateral, enquanto aglomerados mais volumosos migram para uma posição diferente, mais próxima à parede interna. Ao posicionar saídas nos pontos corretos, o chip divide fisicamente esses fluxos: uma saída coleta principalmente células tumorais únicas, outra recolhe aglomerados intactos, e outras saídas removem as células pequenas remanescentes. Importante: os aglomerados permanecem intactos, evitando os danos e a fragmentação frequentemente observados em métodos tradicionais de filtração.
Testando o dispositivo
Para verificar o desempenho do projeto, a equipe primeiro usou esferas plásticas de tamanhos conhecidos para imitar células sanguíneas, células tumorais individuais e aglomerados. Eles demonstraram que o chip em cascata recuperou mais de 87% das esferas “de célula única” e cerca de 92% das esferas “de aglomerado”, removendo a maior parte das esferas menores “de célula sanguínea”. Em seguida, passaram a testes com células reais de câncer de pulmão (células A549) misturadas com leucócitos. Nesses ensaios, o dispositivo recuperou cerca de 82% das células cancerosas no total, com aproximadamente 76% de pureza na fração enriquecida e quase 80% de pureza para os aglomerados celulares. Finalmente, processaram amostras reais de derrame pleural de três pacientes com câncer de pulmão. Partindo de fluidos nos quais células tumorais e aglomerados representavam menos de 1% de todas as células, o chip produziu frações em que células malignas únicas chegaram a cerca de 68% do total, e aglomerados corresponderam a cerca de 35% das células em uma saída dedicada.
O que isso pode significar para pacientes
Ao usar apenas fluxo de fluido e geometria de canais, este dispositivo pode rápida e suavemente extrair tanto células tumorais únicas quanto aglomerados intactos de grandes volumes de fluido de pacientes sem rótulos químicos ou instrumentos complexos. As células enriquecidas permanecem adequadas para testes padrões como coloração por imunofluorescência e microscopia, integrando-se sem atrito aos fluxos de trabalho hospitalares existentes. Embora o estudo atual tenha envolvido um número pequeno de pacientes e exija ensaios maiores para comprovar seu impacto no diagnóstico e no prognóstico, o trabalho demonstra um conceito poderoso: um “concentrador de células” rápido e sem rótulos que revela tanto a quantidade quanto o estado agrupado das células tumorais em derrames pleurais. A longo prazo, tais ferramentas podem afiar a avaliação de malignidade, orientar escolhas de tratamento personalizadas e oferecer uma janela mais clara sobre como os cânceres metastizam.
Citação: Zhu, Z., Ren, H., Zhang, Z. et al. Cascading inertial microfluidics for high-throughput, multi-scale enrichment of tumor cells and intact clusters towards enhanced malignancy diagnosis. Microsyst Nanoeng 12, 101 (2026). https://doi.org/10.1038/s41378-026-01235-y
Palavras-chave: biópsia líquida, separação celular microfluídica, aglomerados de células tumorais, derrame pleural, diagnóstico de câncer