Clear Sky Science · pt
Desenho de um sistema automatizado de microinjeção em lote de células baseado em pinças magnéticas para embriões de zebrafish
Por que ovos minúsculos de peixe importam
Antes que novos remédios ou terapias gênicas cheguem às pessoas, os cientistas costumam testá‑los em animais pequenos que se desenvolvem rapidamente. Embriões de zebrafish são preferidos porque são transparentes e se desenvolvem em velocidade, permitindo que os pesquisadores observem a formação de órgãos em tempo real. Mas, para alterar seus genes ou administrar fármacos, é preciso injetar cada ovo delicado com uma agulha microscópica — uma tarefa que costuma ser lenta, cansativa e fortemente dependente da habilidade humana. Este artigo apresenta um novo sistema robótico capaz de injetar automaticamente lotes de embriões de zebrafish de forma mais rápida, mais suave e mais confiável que um operador humano, abrindo caminho para experimentos maiores e mais consistentes.
Uma nova forma de manipular células frágeis
A microinjeção tradicional exige um operador treinado para guiar uma agulha de vidro sob um microscópio, localizar cada embrião, orientá‑lo corretamente e perfurá‑lo sem danificar estruturas vitais. Isso é especialmente difícil porque os embriões são esferas macias com regiões importantes que devem ser evitadas para mantê‑los vivos. Sistemas robóticos existentes ajudaram a automatizar o transporte e a perfuração, mas normalmente não conseguem controlar a rotação de cada embrião em três dimensões. Como resultado, a agulha pode entrar em ângulo arriscado, reduzindo a taxa de sobrevivência e limitando o número de embriões que podem ser processados de forma confiável. A equipe por trás deste estudo propôs construir uma plataforma totalmente integrada que transporte, rode, injete e libere embriões em sequência suave, sem trocas constantes de objetiva ou ajustes manuais.
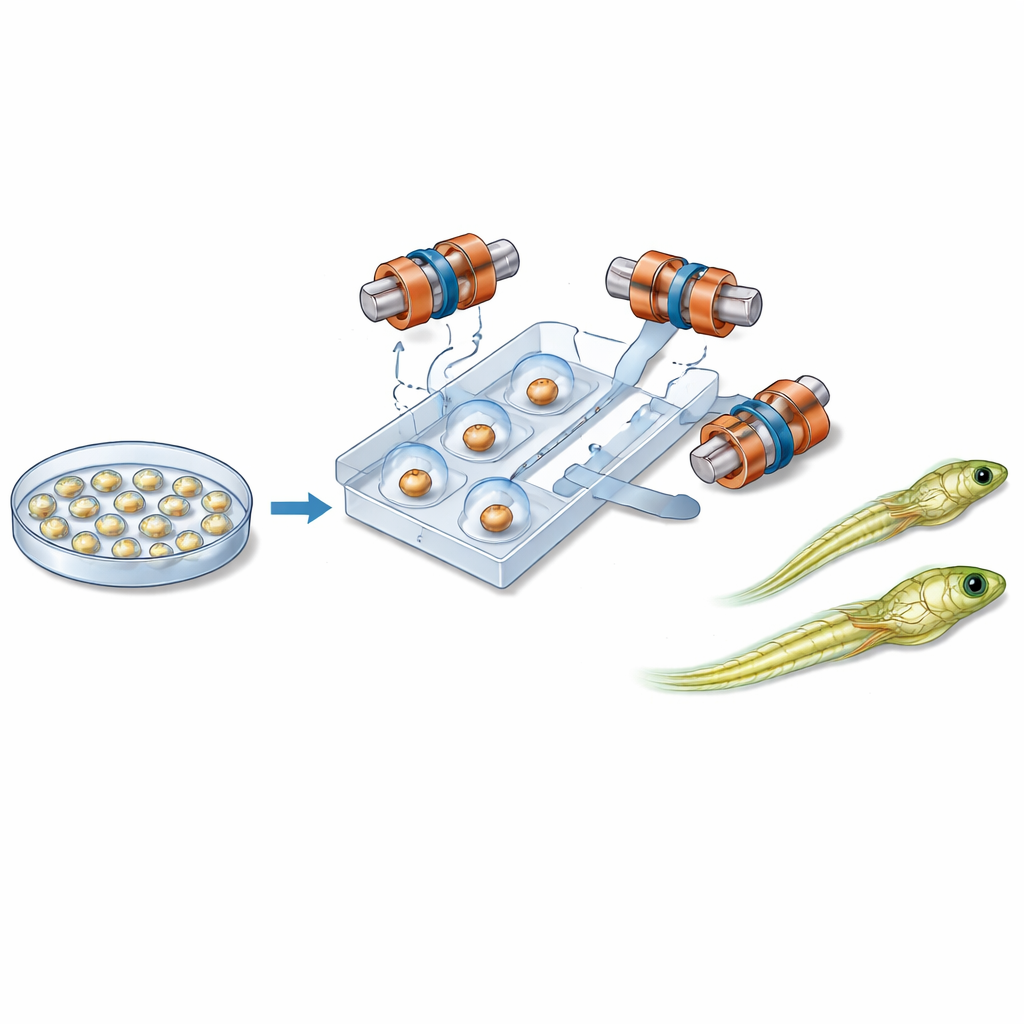
Ímãs, microcanais e controle delicado
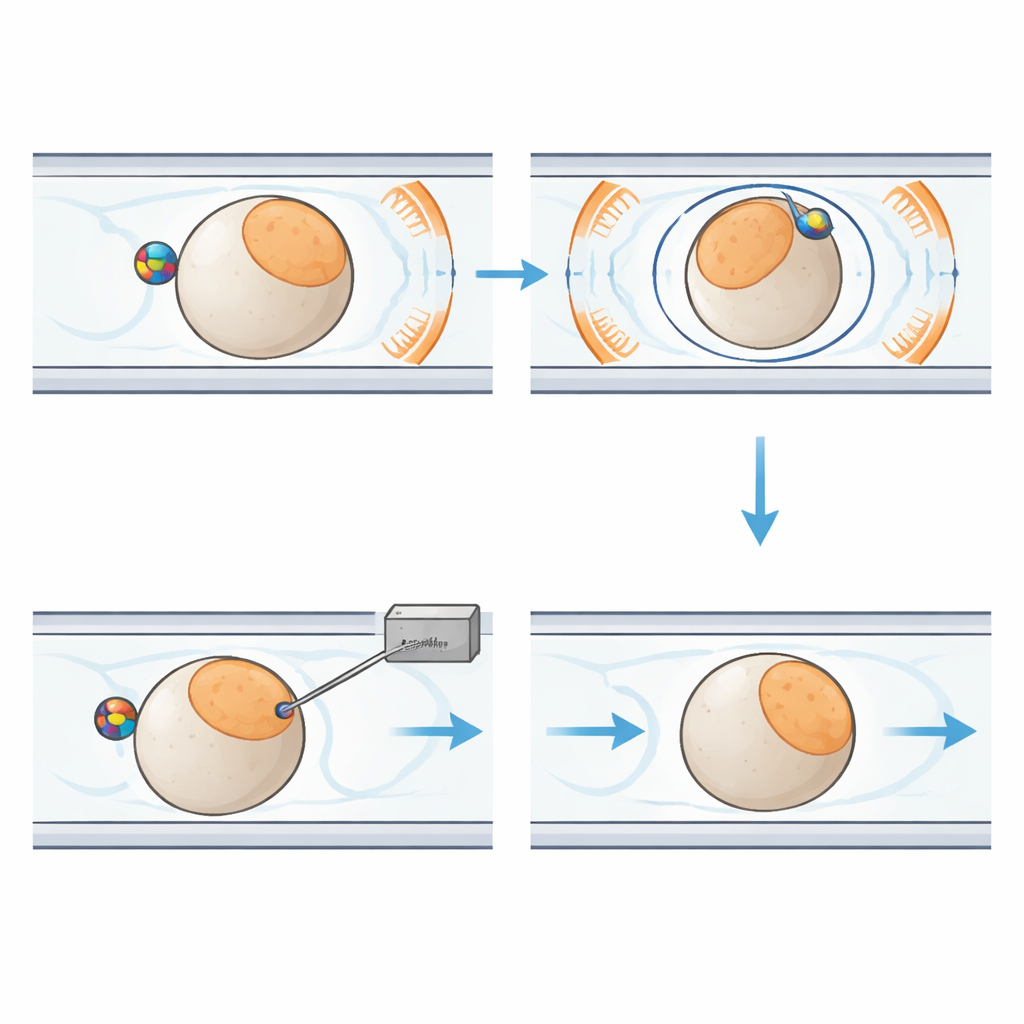
No cerne do novo sistema está um chip de plástico do tamanho da palma que contém canais estreitos que guiam embriões individuais ao longo de um trajeto fixo. Perto de cada embrião há uma pequena esfera magnética. Ao redor do chip, seis bobinas cuidadosamente dispostas geram um campo magnético uniforme em três dimensões. Ao variar a direção desse campo ao longo do tempo, o sistema faz a esfera girar. Graças ao atrito entre a esfera e a superfície do embrião, a célula inteira roda com ela, como duas engrenagens acopladas. Isso permite ao robô inclinar o embrião fora do plano de imagem ou girá‑lo dentro do plano até que a região sensível fique posicionada em segurança, longe da agulha que se aproxima. Líquido e pressão de ar suave movem e mantêm os embriões no lugar, enquanto um módulo separado controla a agulha de injeção e o fluxo minúsculo do material genético.
Ver claramente em um campo de visão minúsculo
Para tornar essa coreografia precisa possível, os pesquisadores também projetaram um avançado sistema de visão computacional, chamado rede de percepção para manipulação microscópica. Ele analisa imagens de uma câmera de microscópio em tempo real para localizar cada embrião, detectar a ponta fina da agulha e distinguir os dois “polos” opostos do ovo onde se encontram estruturas-chave do desenvolvimento. A rede usa técnicas modernas de aprendizado profundo — como caminhos duplos de extração de características, módulos de atenção que destacam detalhes importantes e fusão multi-escala da informação de imagem — para lidar com o mundo poluído e pouco iluminado dentro de um chip microfluídico. Em testes com milhares de imagens, ela detectou objetos e segmentou regiões do embrião com cerca de 98–99% de precisão, fornecendo o feedback confiável necessário para orientar tanto a rotação magnética quanto o posicionamento da agulha.
Comprovando que funciona em zebrafish vivos
A equipe comparou seu sistema automatizado com operadores humanos experientes usando 100 embriões de zebrafish cada. O robô completou as injeções em cerca de 33,8 segundos por embrião, mais de duas vezes mais rápido que o trabalho manual, e perfurou com sucesso todas as células. Também orientou cada embrião com um erro angular médio de apenas 2,1 graus, aproximadamente metade do erro dos operadores humanos. Mais importante, 88% dos embriões injetados pelo robô sobreviveram até eclodir como larvas, em comparação com 66% após injeção manual. Sob um microscópio de fluorescência, as larvas do sistema automatizado brilharam em verde, mostrando que o material genético introduzido foi incorporado e expresso conforme planejado. Ao rotacionar embriões magneticamente em vez de apertá‑los com ferramentas mecânicas, o sistema minimizou deformação e dano enquanto mantinha alto rendimento.
O que isso significa para estudos futuros
Em termos simples, este trabalho mostra que uma combinação cuidadosamente projetada de microcanais, controle magnético e análise de imagem inteligente pode injetar embriões frágeis de peixe mais rapidamente e com maior sobrevivência do que um operador habilidoso usando ferramentas tradicionais. Como o zebrafish é uma plataforma-chave para estudar desenvolvimento, doenças e efeitos de fármacos, um injetor confiável de alto rendimento pode acelerar triagens genéticas em larga escala e estudos biológicos de longa duração que antes eram limitados pelo trabalho manual. Com alterações apropriadas no projeto do chip e nas configurações de controle, a mesma estratégia poderia ser adaptada a outros tipos celulares e pequenos organismos, ajudando a transformar cirurgias celulares delicadas de uma arte praticada por poucos especialistas em um processo automatizado e padronizado.
Citação: Guo, X., Wang, F., Zhao, A. et al. Design of an automated cell batch microinjection system based on magnetic tweezers for zebrafish embryos. Microsyst Nanoeng 12, 113 (2026). https://doi.org/10.1038/s41378-026-01230-3
Palavras-chave: embriões de zebrafish, microinjeção, pinças magnéticas, microfluídica, manipulação robótica de células