Clear Sky Science · pt
Dispositivo microfluídico de camada única de fabricação rápida e baixo custo para foco hidrodinâmico tridimensional de alto rendimento
Por que reduzir fluxos minúsculos é importante
A medicina moderna depende cada vez mais de examinar enormes quantidades de células individuais, por exemplo para detectar células cancerosas na urina ou no sangue. Para fazer isso rápida e economicamente, as células costumam ser conduzidas por canais finíssimos em microchips, onde lasers ou câmeras as inspecionam. Mas para obter imagens nítidas e confiáveis em velocidades extremas, cada célula precisa passar por quase exatamente o mesmo ponto microscópico. Este artigo apresenta uma nova maneira de fabricar esses chips para que possam agrupar as células em um fluxo tridimensional estreito, mesmo em velocidades muito altas, usando um dispositivo mais rápido e barato de produzir do que os sistemas padrão atuais.
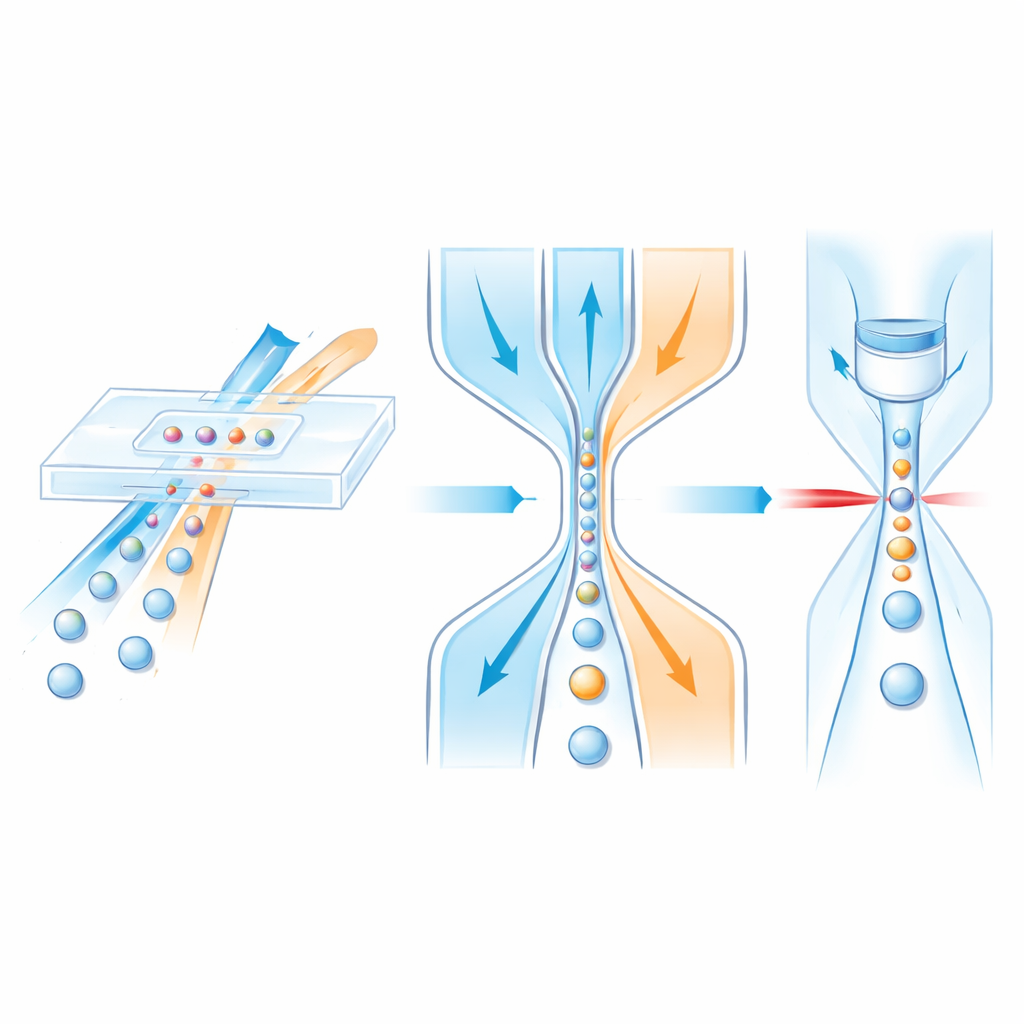
Guiando células com “faixas de tráfego” fluidas
No interior de um chip microfluídico, as células viajam em um fluxo central de amostra enquanto fluidos circundantes de revestimento (sheath) atuam como guard-rails invisíveis, comprimindo suavemente a amostra em direção ao centro. Projetos anteriores geralmente conseguiam focar as células apenas lateralmente, não verticalmente, ou dependiam de estruturas multicamadas complexas que são lentas e caras de fabricar. Os autores, em vez disso, projetam um canal de camada única que ainda alcança controle tridimensional completo. Primeiro, a amostra encontra um fluxo de revestimento vertical em uma junção em T inclinada que se estreita ao longo de seu comprimento. Devido ao formato do canal e à inércia dos líquidos em velocidades mais altas, o fluxo da amostra é empurrado para a metade superior do canal. Em seguida, dois revestimentos laterais correspondentes, mais a jusante, apertam da esquerda e da direita, pressionando a amostra já elevada em um filamento central estreito que atravessa uma janela de detecção.
Fabricando chips melhores em minutos, não horas
A maioria dos chips microfluídicos de pesquisa hoje é feita de silicone macio (PDMS) usando litografia suave, um processo que exige múltiplas etapas de aquecimento e cura e pode levar uma hora ou mais por dispositivo. O PDMS é fácil de moldar, mas se deforma sob alta pressão, fazendo com que os canais se expandam e o fluxo focado se espalhe. O novo dispositivo usa um plástico duro chamado acrilato de poliuretano (PUA), padronizado por um processo de “dupla transferência”. Primeiro, um molde de PDMS reutilizável com relevos dos canais é fundido a partir de um mestre de silício. O PUA líquido é então derramado nesse molde, curado sob luz ultravioleta e desmoldado para formar a camada do canal. Uma lâmina de vidro separada revestida com PUA serve como base. As duas superfícies de PUA são alinhadas, pressionadas e ligadas com outra breve exposição UV. Como cada etapa de cura leva apenas segundos e não é necessário cozimento prolongado, um chip completo pode ser produzido em cerca de cinco minutos, aproximadamente dez vezes mais rápido que os métodos tradicionais.
Testando o fluxo e domando a deformação
Para entender quão bem o projeto funciona, a equipe combina simulações computacionais com experimentos. Primeiro, eles simulam como a mudança nas vazões da amostra e dos revestimentos afeta a forma do núcleo focado. Os resultados mostram que aumentar os fluxos de revestimento vertical e lateral ajuda a reduzir tanto a altura quanto a largura da amostra, e que velocidades gerais maiores (número de Reynolds mais alto) melhoram ainda mais o foco. Em seguida, simulam como as paredes do canal se deformam quando feitas de PDMS macio versus PUA rígido. Em condições realistas de alta velocidade, as paredes de PDMS incham por mais de cem micrômetros, o suficiente para distorcer o fluxo a ponto da amostra se dividir e derivar em direção aos cantos. Em contraste, o PUA se deforma menos de cem nanômetros—efetivamente rígido nessa escala—portanto o fluxo focado mantém-se central e estreito mesmo sob alta pressão.
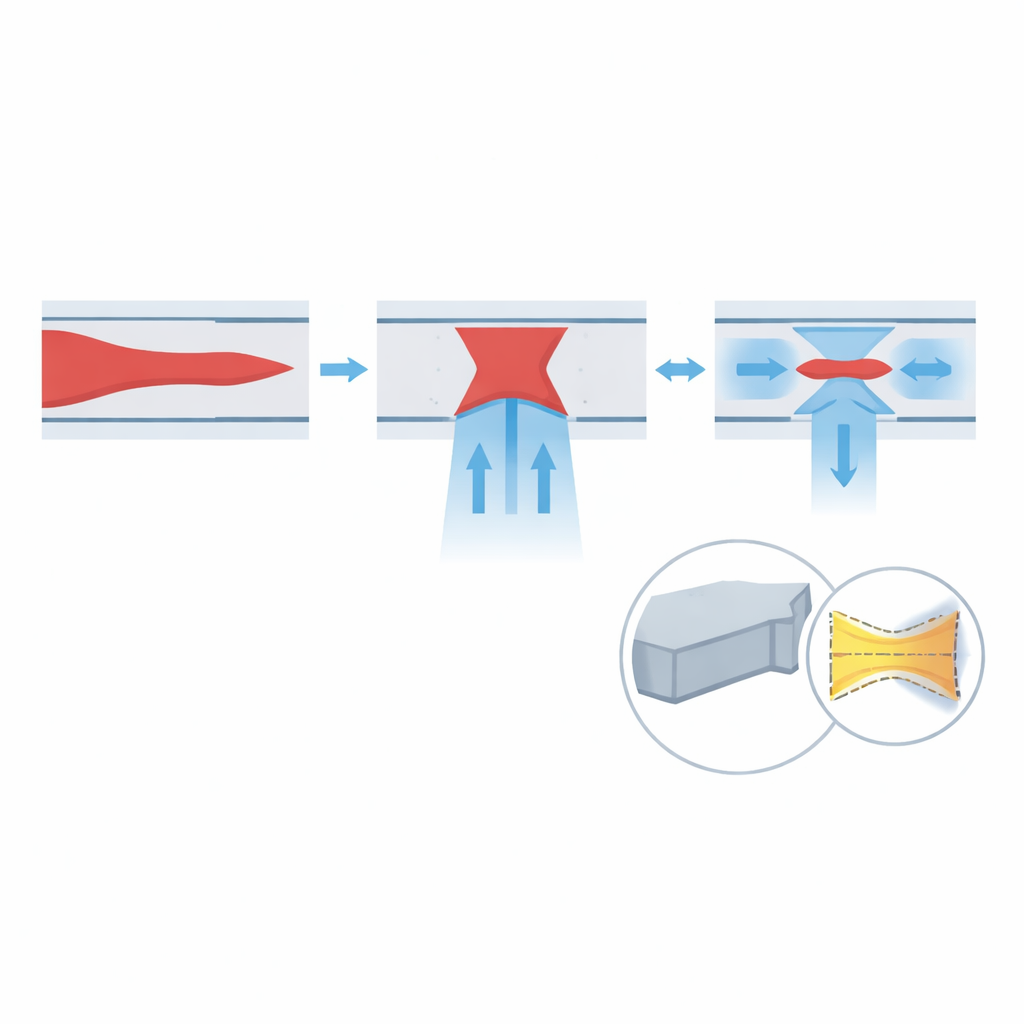
Observando células reais em velocidades extremas
Além de testes com corantes, os autores avaliam o dispositivo usando microscopia por esticamento temporal óptico (OTS), uma técnica que converte pulsos de laser ultrarrápidos em varreduras de linha rápidas, permitindo milhões de linhas por segundo. Eles passam amostras de urina tratadas de pacientes com câncer de bexiga pelo chip em vazões crescentes, enquanto o OTS registra imagens bidimensionais de cada célula que passa. Como o sistema óptico tem uma região focal muito fina, qualquer célula que se desvie para cima ou para baixo aparece borrada, fornecendo uma medida direta do foco vertical. Em velocidades de 3,3 a 16,7 metros por segundo, a fração de imagens nitidamente focadas sobe, alcançando 98,4% na maior velocidade testada. O foco lateral é avaliado medindo o quanto os centros das células se desviam do ponto médio do canal; esse deslocamento diminui com a velocidade, correspondendo a cerca de 95,0% de eficiência de foco lateral a 16,7 metros por segundo.
O que isso significa para futuras análises celulares
Em termos simples, os pesquisadores mostram que um chip plástico direto e de camada única pode conduzir células de forma confiável para um fluxo estreito e bem controlado em todas as direções, mesmo sob as exigentes condições necessárias para imageamento ultrarrápido. Ao combinar um material resistente à deformação com uma arranjamento inteligente de fluxos de revestimento, eles evitam os limites mecânicos dos dispositivos de silicone macio ao mesmo tempo em que encurtam dramaticamente o tempo de fabricação. Isso facilita a produção de muitos chips idênticos para uso clínico e industrial e a execução de testes em larga escala e alto rendimento em amostras reais de pacientes. Como resultado, a tecnologia oferece uma rota prática para ferramentas de triagem celular mais rápidas e precisas que podem beneficiar diagnósticos, monitoramento do câncer e outras aplicações que dependem de examinar de perto vastas quantidades de células individuais.
Citação: Yan, R., Wei, S., Weng, Y. et al. Rapid-manufacturing and cost-effective single-layer microfluidic device for high-throughput three-dimensional hydrodynamic focusing. Microsyst Nanoeng 12, 87 (2026). https://doi.org/10.1038/s41378-026-01212-5
Palavras-chave: citolatria microfluídica, foco hidrodinâmico 3D, análise de célula única em alto rendimento, chips microfluídicos de acrilato de poliuretano, microscopia por esticamento temporal óptico