Clear Sky Science · pt
Sistema robótico de transporte de células baseado em modelagem da resistência de micropipetas
Mover Células Minúsculas Sem um Microscópio
A biologia moderna frequentemente depende de uma tarefa surpreendentemente simples: apanhar uma única célula com um tubo de vidro e colocá‑la em outro lugar. Isso é essencial para tratamentos de fertilidade, congelamento de embriões, terapias baseadas em células e pesquisa básica. Ainda assim, hoje em dia isso quase sempre exige um microscópio volumoso e um operador humano altamente treinado observando cada movimento. Este artigo descreve um novo sistema robótico que pode mover células isoladas entre gotas de líquido sem qualquer visão microscópica, abrindo caminho para “fábricas de células” totalmente fechadas e automatizadas que podem trabalhar mais rápido, com menor custo e reduzindo danos a células delicadas.
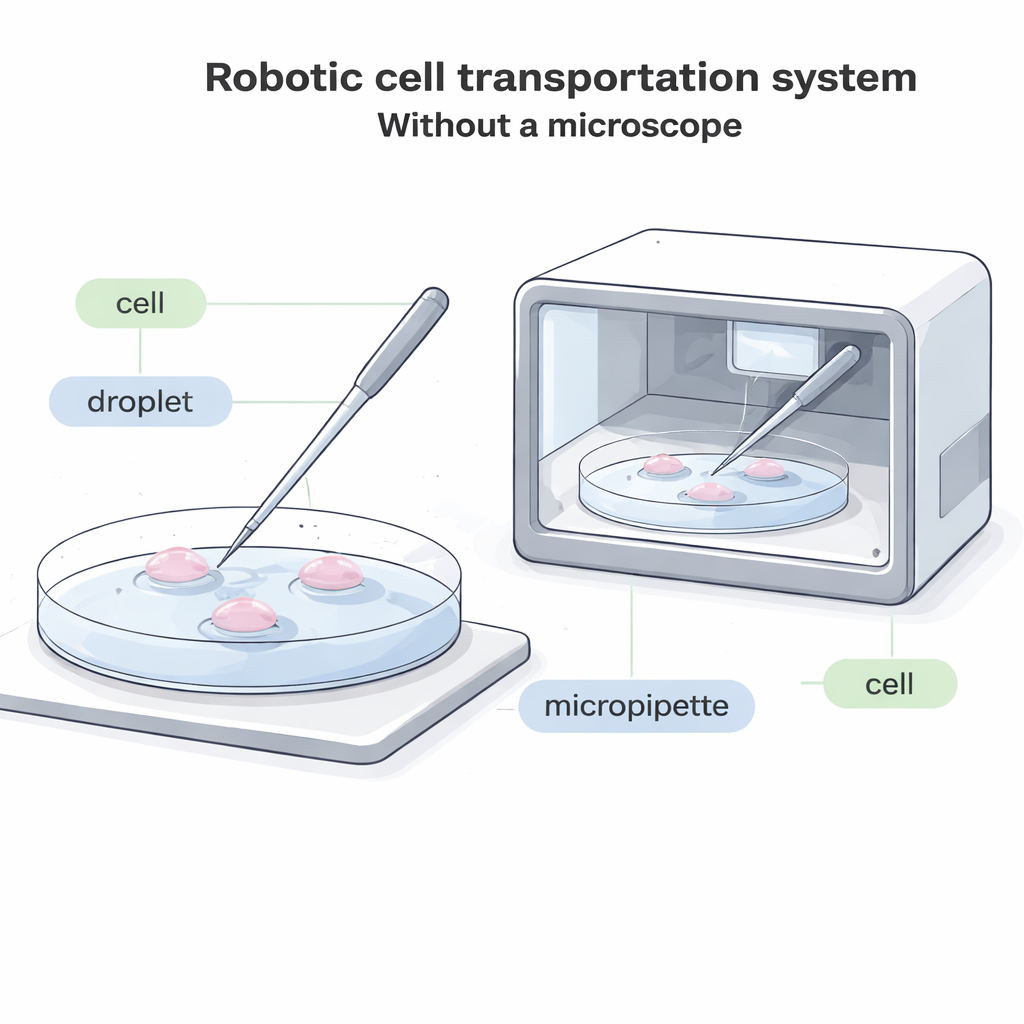
Por que a Transferência de Células Precisa de uma Reformulação
Em laboratórios atuais, um operador olha pelo microscópio e usa um tubo fino de vidro, chamado micropipeta, para pousar no fundo de uma placa, aspirar gentilmente uma célula, deslocá‑la para uma nova gota de fluido e então expulsá‑la. Esse processo é lento, exige muita atenção visual e é difícil de automatizar. Em muitos sistemas futuros — como dispositivos compactos e selados que cultivam embriões ou outras células dentro de uma caixa — simplesmente não há espaço para um microscópio tradicional. Em outros casos, as células são marcadas com corantes fluorescentes que podem desbotar ou ser danificados pela luz, de modo que minimizar observação microscópica intensa é importante. Sistemas “às cegas” existentes que não dependem de imagens só funcionam para células incomumente grandes, deixando a maioria dos tipos celulares sem uma boa solução automatizada.
Um Canudo Especial com uma Trava Integrada
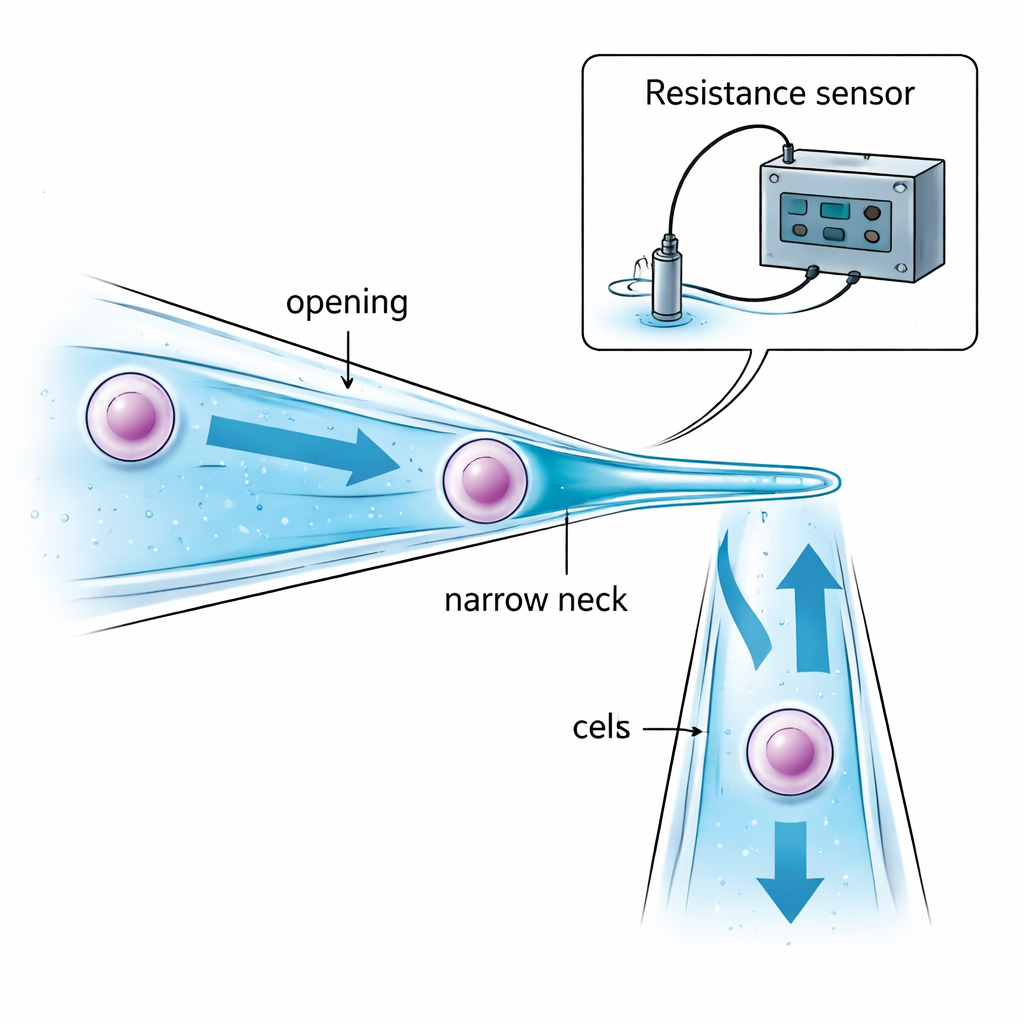
Os autores atacam o problema redesenhando a própria micropipeta. Em vez de um tubo de vidro reto com o mesmo diâmetro ao longo de todo o comprimento, eles criam uma micropipeta com pescoço estreito. Sua abertura é ligeiramente maior que a célula alvo para que a célula possa ser puxada para dentro. Mais adiante, o tubo afina suavemente até um “pescoço” menor que a célula. Quando a sucção puxa a célula em direção a essa constrição, a célula é parada e mantida no interior do tubo — em vez de ficar pendurada na ponta e exposta a óleo ou ar entre as gotas. A escolha cuidadosa do tamanho da abertura, do diâmetro do pescoço e da distância entre eles garante que a célula possa ser capturada com segurança sem ser excessivamente comprimida, e que apenas uma pequena quantidade de líquido seja transportada de uma gota para outra, reduzindo a contaminação.
Ouvindo Sinais Elétricos em vez de Olhar
Sem um microscópio, o robô ainda precisa saber três coisas: quando a ponta de vidro está suficientemente próxima do fundo da placa, quando a célula foi capturada com sucesso no pescoço e quando ela foi totalmente liberada na nova gota. A equipe resolve isso monitorando pequenas variações na resistência elétrica do líquido dentro e ao redor da micropipeta. À medida que a pipeta inclinada se aproxima do fundo da placa, a camada de líquido entre elas diminui e a resistência elétrica aumenta de forma previsível, sinalizando um pouso seguro pouco antes do contato. Quando uma célula bloqueia o pescoço estreito, o caminho elétrico através do líquido é constrito e a resistência salta repentinamente; quando a célula é empurrada para fora, a resistência cai com igual nitidez. Modelos matemáticos dessas resistências de “fenda”, “aspiração” e “injeção” permitem que um computador interprete esses sinais em tempo real e decida quando parar a sucção ou a pressão, tudo sem feedback visual.
Colocando o Robô à Prova
Para verificar se essa abordagem funciona na prática, os pesquisadores construíram um conjunto robótico completo que combina controle de movimento, controle de pressão, detecção de resistência e um computador host. Eles testaram em células cancerígenas pequenas conhecidas como células HeLa (cerca de 10 micrômetros de diâmetro) e em óvulos suínos muito maiores (aproximadamente 150 micrômetros). O sistema conseguiu detectar com confiabilidade o pouso, a captura e a liberação apenas a partir dos sinais de resistência em uma ampla gama de tamanhos de pipeta. Em comparações diretas, o robô transferiu células HeLa com taxa de sucesso de 90% — melhor que um método automatizado anterior baseado em visão — e transportou óvulos suínos com taxa de sucesso de 95%, superior a uma abordagem microscópica padrão. Os tempos de operação por célula foram semelhantes ou mais rápidos que os métodos controlados por humanos, principalmente porque o pescoço estreito elimina a necessidade de ajustes finos repetidos de sucção para posicionar a célula.
Preservando a Viabilidade das Células e Escalando
Qualquer assistente robótico em um laboratório de biologia deve evitar prejudicar as células que manipula. Após o transporte pelo novo sistema, tanto células HeLa quanto óvulos suínos foram cultivados por um dia e corados com um corante que acende apenas em células vivas. As taxas de sobrevivência do novo método foram equivalentes ou se aproximaram das observadas em transferências tradicionais guiadas por microscópio e de células controle não manipuladas, indicando que a compressão mecânica suave no pescoço estreito não reduz de forma perceptível a viabilidade celular quando os limites são definidos corretamente. Olhando para o futuro, os autores sugerem que a mesma detecção baseada em resistência e o controle de pressão podem ser incorporados em chips microfluídicos compactos. Isso permitiria que muitos canais operassem em paralelo, viabilizando sistemas de manuseio de células totalmente fechados e de alto rendimento, adequados para medicina reprodutiva automatizada, terapias celulares e dispositivos de cultura celular de longo prazo onde microscópios não cabem facilmente.
O que Isso Significa para o Trabalho Futuro com Células
Para não‑especialistas, a mensagem principal é que mover células individuais não precisa mais depender de alguém observando através de um microscópio. Ao modelar cuidadosamente um tubo de vidro e “ouvir” como a eletricidade flui pelo líquido ao redor, um robô pode perceber quando pousou, agarrou uma célula e a soltou — tudo no escuro e em espaços apertados. Isso torna muito mais prático projetar sistemas fechados e autônomos de cultivo celular que protegem amostras frágeis, simplificam fluxos de trabalho clínicos e aproximam a manipulação de células em nível laboratorial de uma operação automatizada em estilo de fábrica.
Citação: Zhao, Q., Liu, M., Zhu, R. et al. Robotic cell transportation system based on micropipette resistance modeling. Microsyst Nanoeng 12, 65 (2026). https://doi.org/10.1038/s41378-026-01193-5
Palavras-chave: manipulação de células, micropipeta, robótica, microfluídica, automação