Clear Sky Science · pt
Estratégias para controlar a organização espacial celular em sistemas microfisiológicos
Construindo Tecidos Minúsculos no Laboratório
Nossos órgãos funcionam tão bem porque suas células não estão distribuídas ao acaso—elas são cuidadosamente organizadas no espaço. Este artigo explora como cientistas estão aprendendo a recriar essa ordem intrincada dentro de “órgãos-em-chip” e outros tecidos miniaturizados cultivados em laboratório. Ao orientar onde diferentes células se situam e como interagem, os pesquisadores conseguem construir modelos mais realistas do coração, cérebro, intestino, vasos sanguíneos e até de ecossistemas humano–microbiano. Esses sistemas avançados prometem testes de drogas mais seguros, menos experimentos com animais e ferramentas melhores para estudar doenças e desenvolver tratamentos personalizados.
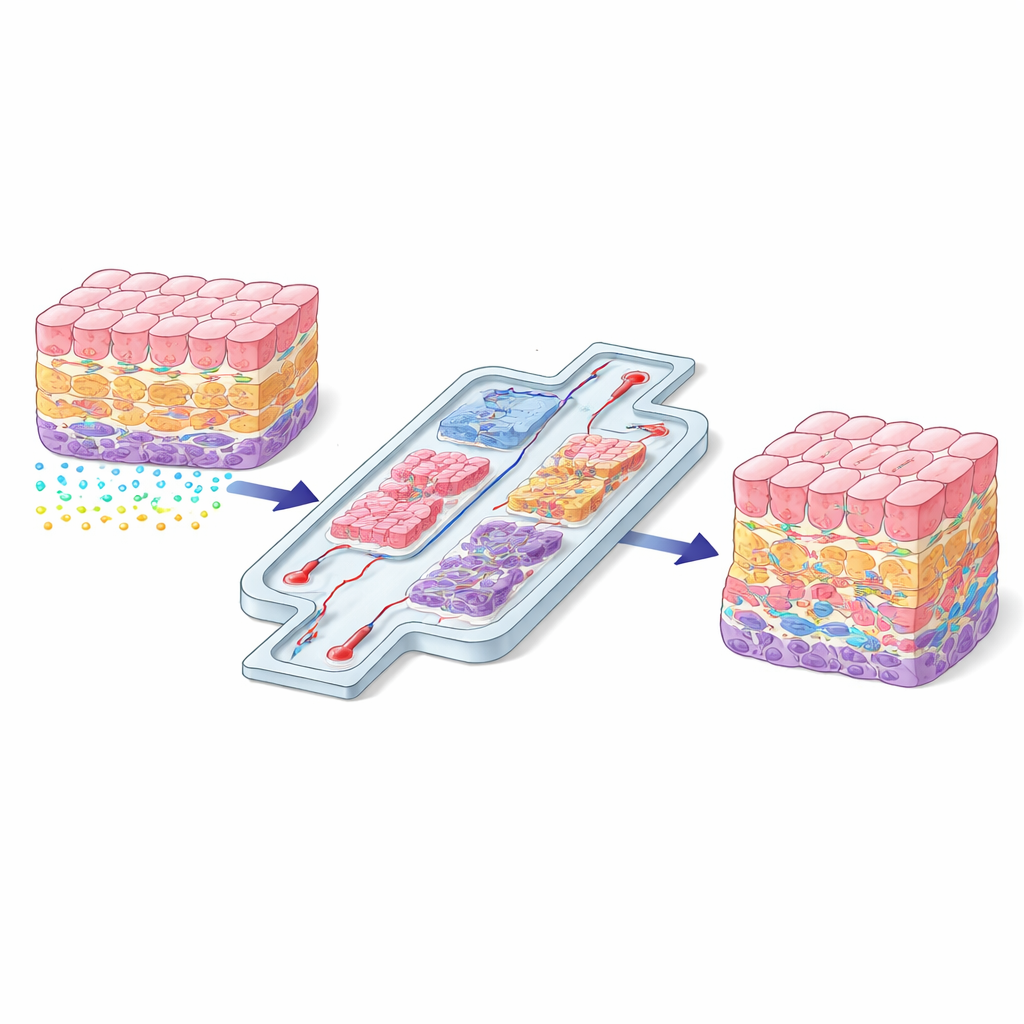
Por que a Posição Celular Importa
No interior do corpo, cada célula vive em um bairro específico com sua própria mistura de estruturas de suporte, sinais químicos e forças físicas. Uma célula hepática próxima a um vaso sanguíneo recebe sinais muito diferentes de uma célula enterrada mais profundamente no órgão. Essas diferenças de localização ajudam a determinar como as células crescem, em que se diferenciam e como respondem a lesões ou medicamentos. Quando os cientistas cultivam células em placas plásticas planas, essa “conversa” espacial se perde em grande parte, e as células frequentemente se comportam de maneira não natural. O artigo defende que recriar uma organização espacial realista não é uma melhoria opcional, mas uma exigência básica se os tecidos cultivados em laboratório devem imitar órgãos reais.
Du as Principais Formas de Organizar Células
Os autores agrupam as estratégias atuais em duas famílias amplas: controle direto e indireto. Métodos diretos colocam fisicamente células ou compartimentos exatamente onde são necessários. Exemplos incluem a bioimpressão 3D, que deposita camadas de células e géis macios como uma impressora 3D biológica; chips microfluídicos que moldam tecidos em câmaras e canais conectados; e métodos de aprisionamento físico que posicionam células usando luz, som, ímãs ou campos elétricos. Essas abordagens brilham quando a geometria precisa é crucial—como na recriação da barreira hematoencefálica, na parede estratificada de um vaso sanguíneo ou no caminho de fluxo do intestino ao fígado.
Deixando as Células Lerem seu Entorno
Métodos indiretos, em vez disso, remodelam o ambiente e deixam que as próprias células façam o resto. Aqui, os cientistas ajustam a “paisagem” que as células percebem: a composição do gel circundante, a rigidez e textura das superfícies, e gradientes de substâncias dissolvidas como fatores de crescimento ou fármacos. Moléculas de suporte dispostas cuidadosamente podem fazer com que certos tipos celulares se acomodem em regiões específicas. Hidrogéis inteligentes que amolecem ou liberam sinais quando as células os remodelam incentivam estruturas auto-organizadas, como redes vasculares ou cristas e vilosidades semelhantes às do intestino. Dispositivos microfluídicos podem gerar gradientes químicas estáveis que fazem com que células-tronco adotem identidades diferentes ao longo de um canal, ou que células tumorais e imunológicas migrem para zonas distintas, revelando como doenças se espalham.
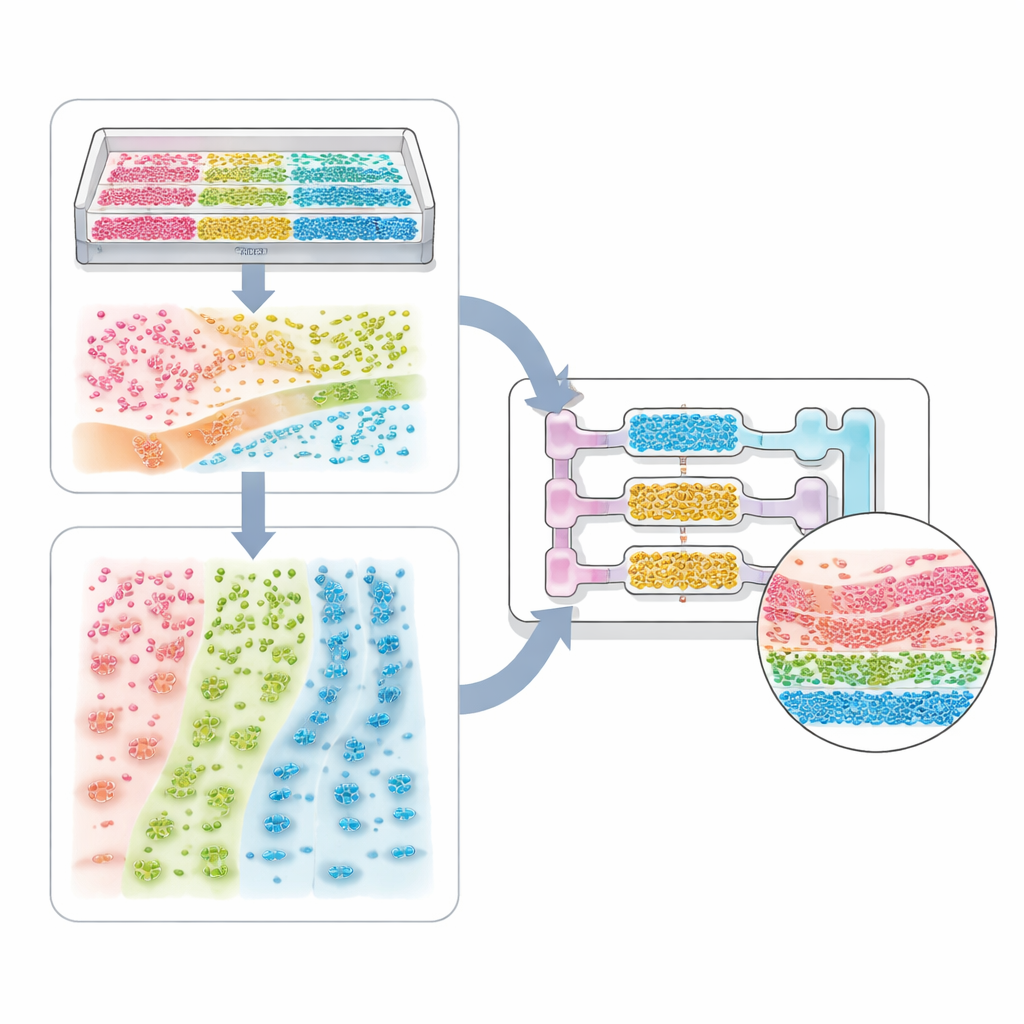
De Sistemas de Célula Única a Modelos de Corpo Inteiro
A revisão percorre um espectro de aplicações. No extremo mais simples estão sistemas de um único tipo celular, onde ranhuras padronizadas ou gradientes de rigidez podem fazer células cardíacas baterem em uníssono ou neurônios estenderem fibras alinhadas. Modelos de tecido mais complexos combinam vários tipos celulares—como células tumorais, células de suporte e células endoteliais—para formar esferoides e organoides com núcleos e cascas internas. Microcanais e bioimpressão então acrescentam limites e fluxo, permitindo recriar alvéolos pulmonares, filtros renais, zonas hepáticas e circuitos multi-órgãos que rastreiam como um medicamento é absorvido, transformado e eliminado. As mesmas ideias se estendem a sistemas hospedeiro–microbio, onde a disposição espacial de bactérias ao longo da parede intestinal, ou através de uma camada de muco, pode determinar se elas nos protegem ou causam doença.
Verificando se os Padrões são Reais
À medida que esses sistemas se tornam mais intrincados, os cientistas precisam de maneiras confiáveis de confirmar que as células acabam onde deveriam e se comportam conforme o esperado. O artigo destaca métodos de imagem que observam células vivas se moverem e mudarem ao longo do tempo, bem como técnicas avançadas de coloração e sequenciamento que mapeiam quais genes, proteínas e metabólitos aparecem em cada local. Sensores incorporados em chips podem monitorar oxigênio, nutrientes, ácidos e forças mecânicas, vinculando condições locais às respostas celulares. Juntas, essas ferramentas ajudam os pesquisadores a verificar que um projeto não é apenas convincente visualmente, mas funcionalmente fiel ao tecido real.
Para Onde Esse Trabalho Está Indo
Os autores concluem que os sistemas mais poderosos irão combinar estratégias diretas e indiretas: usar chips e bioimpressoras para definir a disposição geral e, em seguida, incorporar géis ajustáveis, texturas e gradientes que permitam que os tecidos amadureçam e se remodelam ao longo do tempo. Eles também observam obstáculos práticos—como escalar a fabricação, reduzir a variabilidade entre laboratórios e enfrentar questões éticas em torno de modelos complexos de tecido humano. Ainda assim, a mensagem é clara: dominar a organização espacial é a chave para transformar sistemas microfisiológicos em substitutos confiáveis de órgãos humanos, abrindo novas portas para estudar desenvolvimento, testar terapias e adaptar a medicina a pacientes individuais.
Citação: Truong, H.D., Ge, Z., Chng, E. et al. Strategies to control cellular spatial organization in microphysiological systems. Microsyst Nanoeng 12, 85 (2026). https://doi.org/10.1038/s41378-025-01141-9
Palavras-chave: organ-on-a-chip, organização espacial celular, bioimpressão 3D, modelos de tecido microfluídicos, sistemas microfisiológicos