Clear Sky Science · pt
Plataforma ponto de atendimento em um só tubo baseada em CRISPR para detecção rápida, específica e sensível de HPV 16 sem pré-amplificação
Por que detectar um único tipo de vírus é realmente importante
O câncer cervical está frequentemente associado à infecção por papilomavírus humanos (HPV), mas nem todos os tipos de HPV apresentam o mesmo risco. Por isso, os médicos precisam de testes que possam distinguir de forma confiável esses vírus muito semelhantes, especialmente o tipo de alto risco chamado HPV16. O desafio é que os testes genéticos atuais às vezes confundem parentes próximos, levando a alarmes falsos ou casos perdidos. Este estudo apresenta um novo método de teste que melhora substancialmente tanto a precisão quanto a praticidade, com o objetivo de levar a subtipagem precisa de HPV para clínicas e ambientes ponto de atendimento.
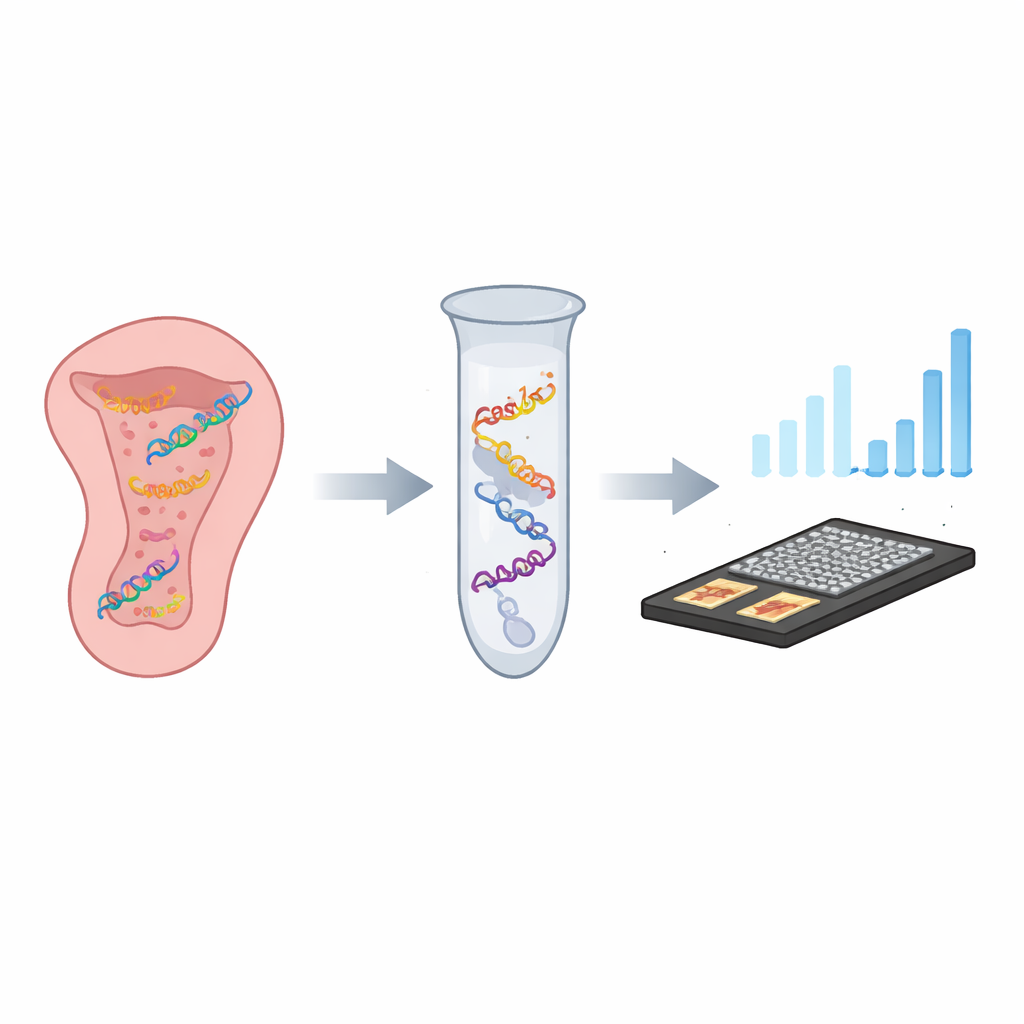
Uma trava molecular inteligente e sua chave
Os pesquisadores desenvolveram um teste em um único tubo que chamam de CASTSA, que combina duas ideias poderosas: a precisão do CRISPR, um sistema de direcionamento gênico adaptado de bactérias, e a capacidade de amplificação do PCR, o método padrão para copiar DNA. No CASTSA, uma proteína CRISPR chamada Cas12a é guiada até a sequência genética do HPV16 por um curto RNA “chave”. Quando encontra a correspondência exata mais um padrão curto adjacente que ela exige, a Cas12a corta o DNA viral em um ponto previsível. Esse corte cria uma extremidade solta característica em uma das fitas de DNA que serve como ponto de partida único para a amplificação. Outros tipos de HPV, mesmo com sequências muito semelhantes, ou não são cortados ou não geram o ponto de partida correto, de modo que não são amplificados.
Transformando um corte minúsculo em um sinal forte
Para converter esse corte do CRISPR em um sinal detectável, a equipe projetou um primer de DNA especial chamado primer terminal‑específico. Esse primer só se encaixa corretamente na fita gerada pelo corte da Cas12a, então se dobra sobre si mesmo como um grampo (hairpin) e ajuda a construir um molde estável para o PCR. Sequências adicionais de primers “universais” então se ligam e impulsionam uma reação convencional de PCR em tempo real. Crucialmente, a amplificação só ocorre se a Cas12a tiver feito seu trabalho primeiro e se o primer se dobrar corretamente, criando duas camadas de verificação. Essa arquitetura reduz fortemente a chance de que DNA parcialmente correspondente e não alvo seja amplificado acidentalmente, abordando uma fraqueza comum de testes CRISPR anteriores que dependiam de uma etapa separada de pré‑amplificação.
Tudo em um tubo, com menos erros
Um avanço prático importante é que o corte pelo CRISPR e a amplificação por PCR ocorrem juntos no mesmo tubo selado, evitando a necessidade de abrir tubos entre as etapas — uma fonte importante de contaminação em muitos procedimentos laboratoriais. Os autores ajustaram cuidadosamente as condições de reação, especialmente os níveis de magnésio, de modo que tanto a Cas12a quanto a enzima de cópia de DNA funcionem bem sem incentivar reações espúrias. Eles mostraram que sua configuração em um só tubo pode distinguir fielmente o HPV16 de vários outros tipos de alto risco, incluindo HPV18, 33, 45 e 52, mesmo que esses vírus compartilhem regiões genéticas altamente conservadas. Em comparação com o PCR em tempo real padrão sozinho, ou com testes CRISPR que primeiro amplificam o DNA e depois fazem a detecção CRISPR, o CASTSA produziu muitos menos sinais enganadores provenientes de tipos de HPV fora do alvo.
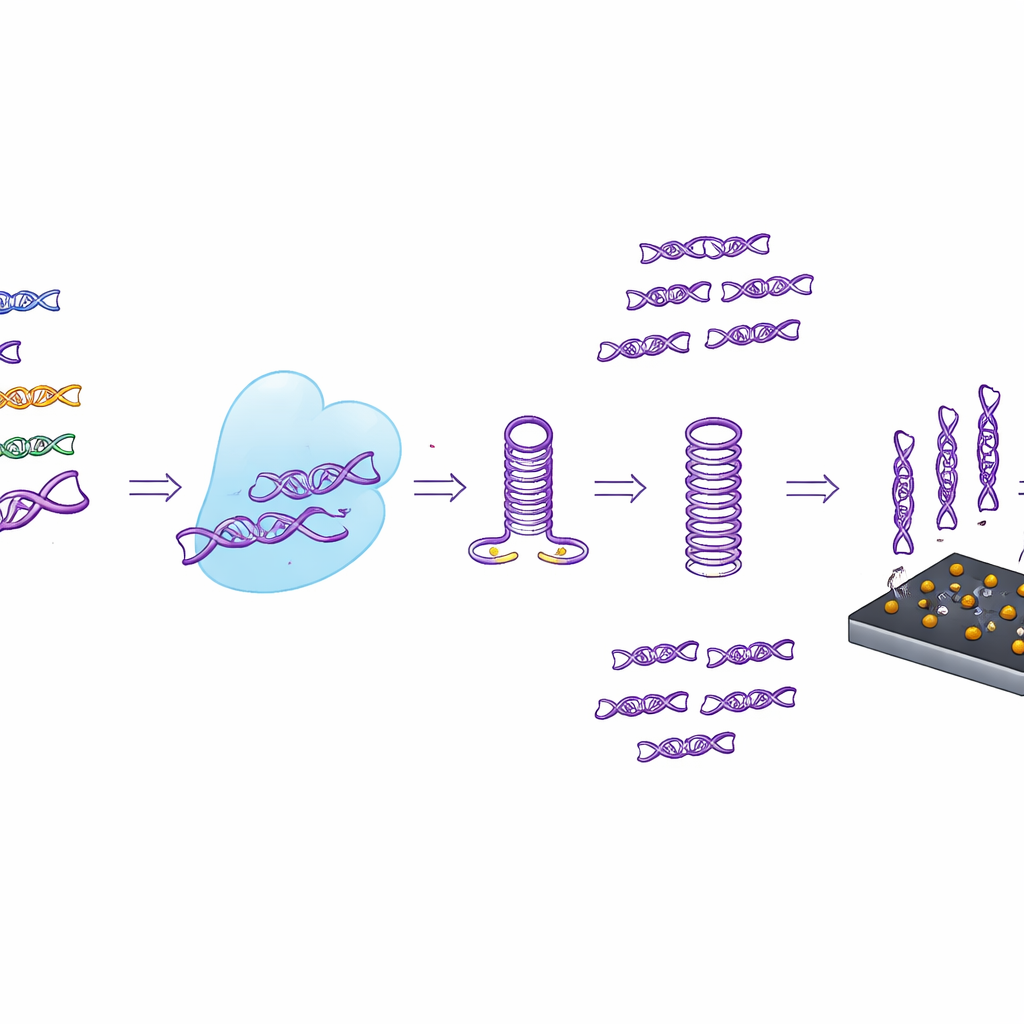
Do tubo de ensaio ao sensor portátil
Em vez de depender apenas de leituras por fluorescência, os pesquisadores também acoplaram o CASTSA a um sensor eletroquímico compacto feito de grafeno induzido por laser. Essa superfície de carbono porosa e altamente condutiva é decorada com nanopartículas de ouro que carregam fitas de captura projetadas para se ligar apenas aos produtos de amplificação CASTSA do HPV16. Quando esses produtos se prendem, a corrente elétrica através do sensor se altera de forma mensurável. Ao usar um arranjo de quatro eletrodos — três pontos de medição e um controle de fundo embutido — o dispositivo pode subtrair o ruído de aderências não específicas. Em testes, esse sistema integrado detectou tão poucos quanto 18 cópias do alvo HPV16 por reação, superando a sensibilidade da fluorescência isolada e mantendo excelente repetibilidade.
Como isso pode mudar os testes de HPV
Para avaliar o desempenho em condições reais, a equipe testou 20 amostras clínicas conhecidas por conter HPV16 e 10 amostras de doadores saudáveis. O CASTSA, tanto em sua forma por fluorescência quanto quando emparelhado com o sensor à base de grafeno, concordou completamente com os testes de PCR padrão do hospital. Ao mesmo tempo, mostrou capacidade superior de ignorar outros tipos de HPV de alto risco que comumente causam confusão. Para os pacientes, isso pode significar menos resultados ambíguos e decisões mais seguras sobre acompanhamento e tratamento. De modo mais amplo, a estratégia CASTSA — reconhecimento CRISPR primeiro, amplificação depois, tudo em um tubo selado — oferece um roteiro para testes genéticos altamente específicos e de baixa contaminação que poderiam ser adaptados a muitos patógenos e mutações, especialmente em cenários que exigem respostas rápidas e confiáveis.
Citação: Chen, Y., Chen, Y., Zhang, C. et al. One-pot CRISPR-based point of care platform for rapid, specific and sensitive detection of HPV 16 without pre-amplification. Microsyst Nanoeng 12, 81 (2026). https://doi.org/10.1038/s41378-025-01130-y
Palavras-chave: detecção de HPV16, diagnósticos CRISPR, testes baseados em PCR, biossensor eletroquímico, ensaio ponto de atendimento