Clear Sky Science · pt
Letalidade sintética da inibição de MCL-1 e terapia CAR-T em linfoma B agressivo
Por que isso importa para o tratamento do câncer
Os linfomas B agressivos são cânceres do sangue de crescimento rápido que frequentemente retornam após o tratamento. Mesmo abordagens novas e potentes, como a terapia CAR-T, que reprograma as células imunológicas do próprio paciente para atacar o câncer, falham em cerca de metade dos pacientes ao longo do tempo. Este estudo explora uma forma de transformar essa vulnerabilidade em vantagem: usar um fármaco que mira uma proteína-chave de sobrevivência nas células do linfoma para tanto matar tumores quanto tornar as células remanescentes mais fáceis de serem eliminadas pelas células CAR-T.
O problema das células de linfoma persistentes
Os linfomas B agressivos costumam ser impulsionados pela atividade excessiva de um gene chamado MYC, que faz as células se dividirem rapidamente e também as ajuda a se esconder do sistema imune. Tratamentos padrão e até a terapia CAR-T podem deixar pequenos bolsões de células de linfoma que toleram drogas e posteriormente causam recidiva. Essas células “persistentes” e resistentes vivem em um bairro tumoral lotado de células imunes supressoras que mantêm as células T assassinas à distância. Os autores se perguntaram se bloquear MCL-1, uma proteína da qual as células do linfoma dependem para evitar a autodestruição, poderia expor uma fraqueza oculta nesse sistema.
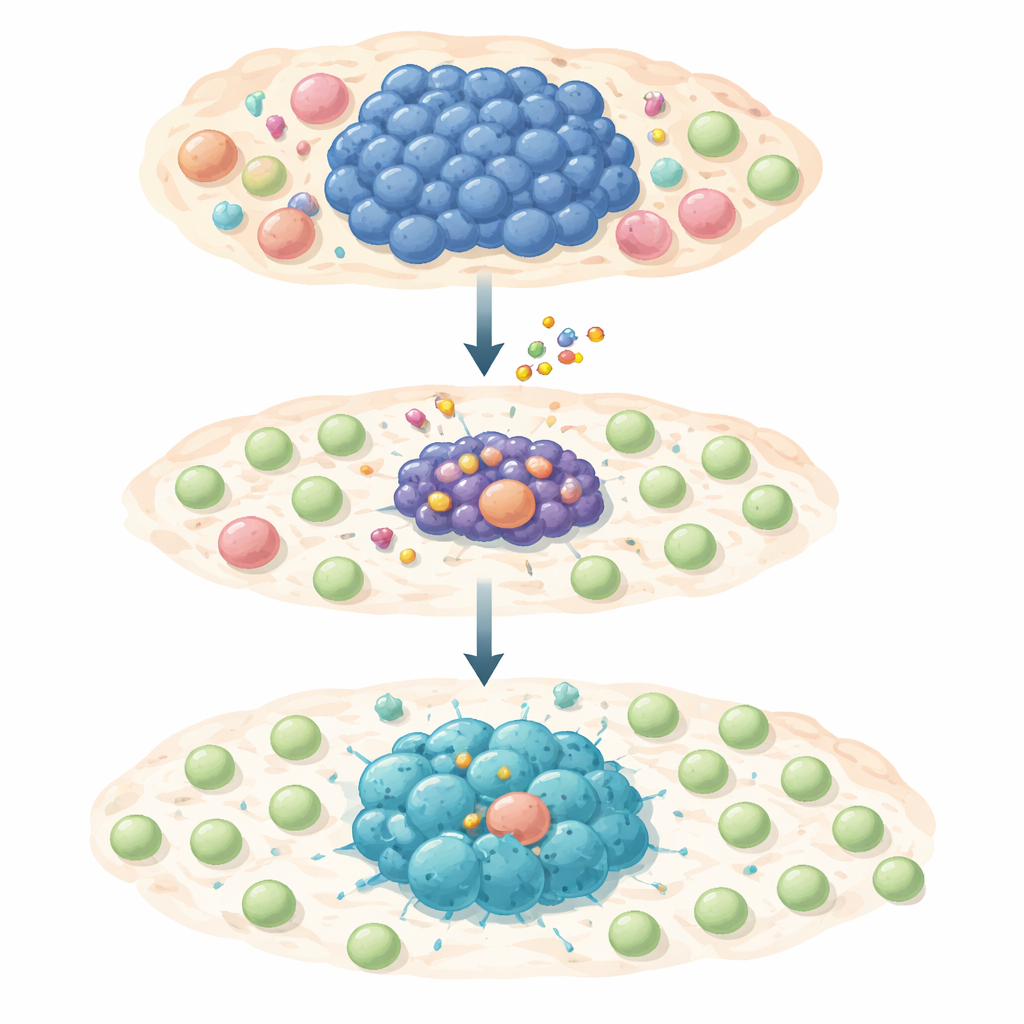
Um ataque em dois passos contra a sobrevivência e o esconderijo tumoral
A equipe testou um fármaco seletivo bloqueador de MCL-1, S63845, em um grande painel de linhagens de células humanas de linfoma que dependem de MYC. A maioria dessas células cancerosas foi altamente sensível ao fármaco e sofreu morte programada quando MCL-1 foi bloqueado. No entanto, uma pequena fração sobreviveu à exposição de curto ou longo prazo e tornou-se tolerante ao medicamento ou totalmente resistente. Quando os pesquisadores examinaram esses sobreviventes em detalhe, descobriram que a atividade de MYC havia sido atenuada enquanto outra molécula, STAT1, e sua via associada de alarme por interferon foram ativadas. Essa mudança ligou genes que impulsionam sinais inflamatórios e quimiocinas — “sinais de fumaça” moleculares que podem atrair células T para a região tumoral.
Reacendendo o bairro imune
Para ver como isso ocorre em um organismo vivo, os autores trataram camundongos com linfomas dirigidos por MYC com uma baixa dose do inibidor de MCL-1. O fármaco reduziu a carga tumoral enquanto poupava células B normais, mas seu impacto foi além da simples redução do volume tumoral. Tumores tratados mostraram mais células T CD4 e CD8, menos células T exauridas, menos células T reguladoras e menos células mieloides supressoras — todos sinais de um ambiente mais favorável ao sistema imune. Sequenciamento de RNA em célula única do tumor e das células circundantes confirmou que as células de linfoma residuais tinham MYC reduzido, STAT1 aumentado e sinais mais fortes de interferon e inflamação, enquanto o tecido ao redor foi repovoado por células T ativas e células natural killer em vez de células supressoras.
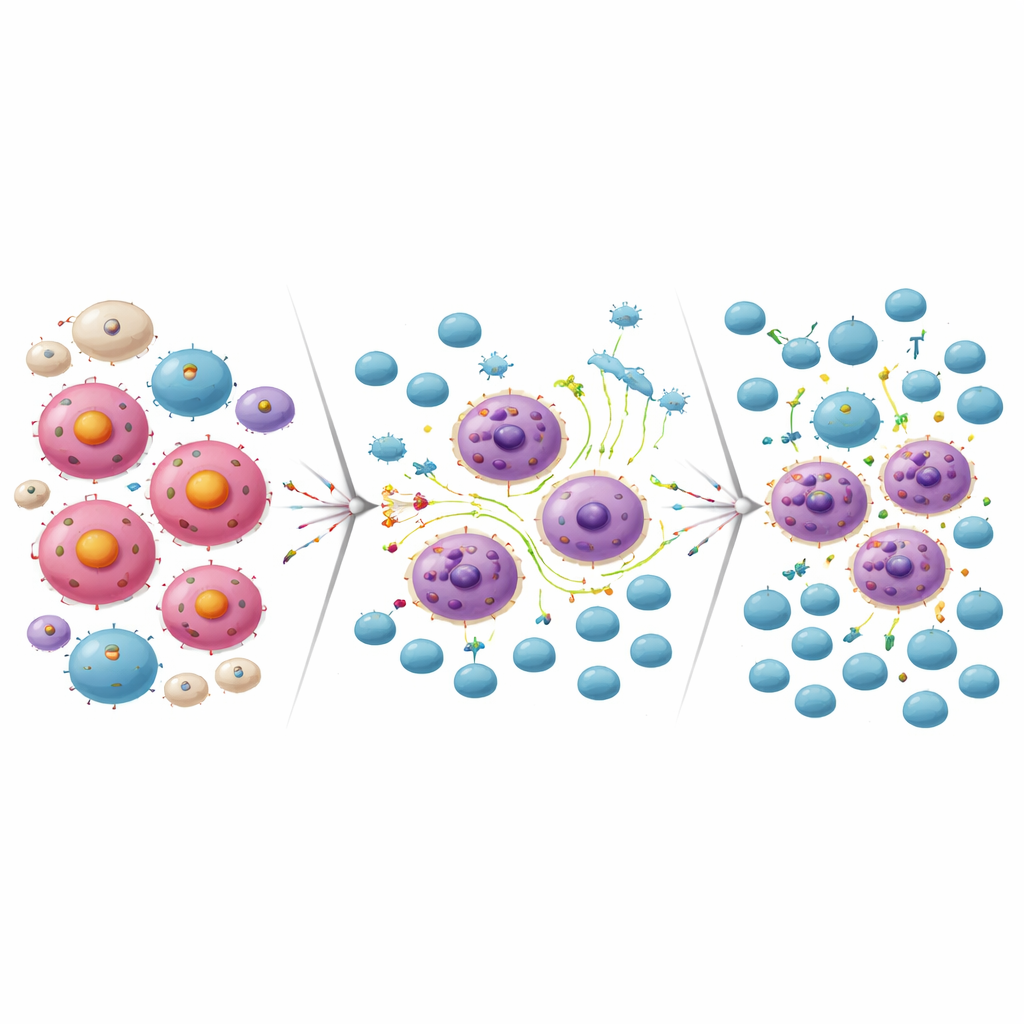
Transformando resistência em oportunidade para células CAR-T
O mesmo reprogramação inflamatória que ajudou algumas células de linfoma a sobreviver ao bloqueio de MCL-1 também as tornou mais vulneráveis ao ataque imune. Em laboratório, células CAR-T direcionadas ao CD19 mataram de forma eficiente células de linfoma que haviam se tornado resistentes ao fármaco contra MCL-1. Por outro lado, células de linfoma que se tornaram resistentes à terapia CAR-T anti-CD19 foram altamente sensíveis ao inibidor de MCL-1. Quando os pesquisadores combinaram uma dose subletal do fármaco de MCL-1 com células CAR-T em cultura celular, os dois tratamentos juntos eliminaram muito mais células de linfoma do que qualquer um isoladamente. Em modelos murinos, administrar o inibidor de MCL-1 seguido por células CAR-T CD19 levou à quase completa eliminação tumoral e a sobrevivência significativamente mais longa em comparação com tratamentos únicos.
Um golpe em dois tempos com potencial curativo
Em termos simples, o estudo sugere uma estratégia de “um‑dois”. Primeiro, um fármaco bloqueador de MCL-1 derruba a maior parte do linfoma e força as células cancerosas sobreviventes a entrarem em um estado inflamatório e altamente visível que atrai células T e remove suas defesas imunes. Segundo, células CAR-T CD19 exploram essa fraqueza recém-exposta para erradicar a doença remanescente. Ao atingir tanto a fiação interna de sobrevivência do tumor quanto seu bairro protetor, essa abordagem combinada pode reduzir recidivas e aproximar os linfomas B agressivos de remissões duradouras.
Citação: Gao, J., Zhao, X., Yin, Q. et al. Synthetic lethality of MCL-1 inhibition and CAR-T therapy in aggressive B-cell lymphoma. Leukemia 40, 638–648 (2026). https://doi.org/10.1038/s41375-026-02884-8
Palavras-chave: Linfoma B, Terapia CAR-T, Inibição de MCL-1, Microambiente tumoral, Resistência a medicamentos