Clear Sky Science · pt
Repressão do miR-29 via MYC leva ao aumento da sinalização CD40 em linfoma folicular transformado
Quando a conversa entre células fica perigosa
O linfoma folicular é um câncer de sangue de crescimento lento que pode permanecer silencioso por anos, mas em alguns pacientes ele muda de marcha de forma súbita e torna-se uma doença agressiva e com risco de vida. Este estudo faz uma pergunta simples, porém crucial: o que muda dentro dessas células cancerosas, e em seu entorno celular, para acionar essa transição? Ao acompanhar tanto os genes das células tumorais quanto pequenos reguladores de RNA ao longo dessa transição, os pesquisadores revelam um circuito de controle oculto que ajusta o quanto as células tumorais respondem à ajuda de células imunes vizinhas — e mostram que quando esse circuito falha, o câncer fica mais difícil de tratar.
Um câncer discreto que às vezes acelera
O linfoma folicular surge de células B, as células do sistema imune que normalmente produzem anticorpos. A maioria dos pacientes convive com uma forma indolente, ou lenta, da doença, mas a cada ano uma fração dos casos se transforma em um linfoma agressivo que se comporta de maneira mais próxima ao linfoma difuso de grandes células B. Mutações genéticas haviam sido associadas a essa mudança, mas não explicavam tudo. As células tumorais vivem em um microambiente rico, cheio de células T auxiliares e outros parceiros imunes, trocando sinais constantemente. Os autores suspeitaram que pequenas moléculas regulatórias chamadas microRNAs, que afinam o uso dos genes, poderiam ser a chave para como as células cancerosas se adaptam a esse entorno mutável e fazem o salto para um estado mais perigoso.
Os freios de RNA pequenos desaparecem
Para testar essa ideia, a equipe realizou o primeiro perfil pareado de RNAs mensageiros e microRNAs em amostras emparelhadas retiradas dos mesmos pacientes antes e depois da transformação. Comparando 11 amostras de linfoma folicular com suas 11 contrapartes transformadas, eles encontraram mais de mil genes e 19 microRNAs que mudaram. Uma família se destacou: os três membros da família miR-29 foram consistentemente reduzidos em tumores transformados. Em trabalhos anteriores em outros cânceres hematológicos, o miR-29 atuava como um freio ao crescimento e à sobrevivência celular. Aqui, sua perda emergiu como uma marca da transformação, sugerindo que a redução dessa família de microRNAs poderia liberar vias promotoras de crescimento nas células do linfoma.
Um sinal reforçado vindo das células auxiliares
Ao analisar os dados de expressão gênica, os pesquisadores descobriram que os tumores transformados apresentavam um forte aumento na atividade da via CD40, uma rota de sinalização que é ativada quando uma célula T auxiliar se engaja com uma célula B. Em linfonodos saudáveis e no linfoma folicular indolente, essa interação ajuda as células B a crescer e sobreviver de maneira controlada. Surpreendentemente, nas amostras transformadas, genes relacionados ao CD40 foram ativados em cerca de 90% dos casos, mesmo que o número total de células T nas áreas tumorais fosse na verdade menor. Análises em célula única confirmaram que um subconjunto de células T ainda fornecia o sinal ativador do CD40, mas as próprias células do linfoma pareciam ter se tornado muito mais sensíveis a esse sinal.
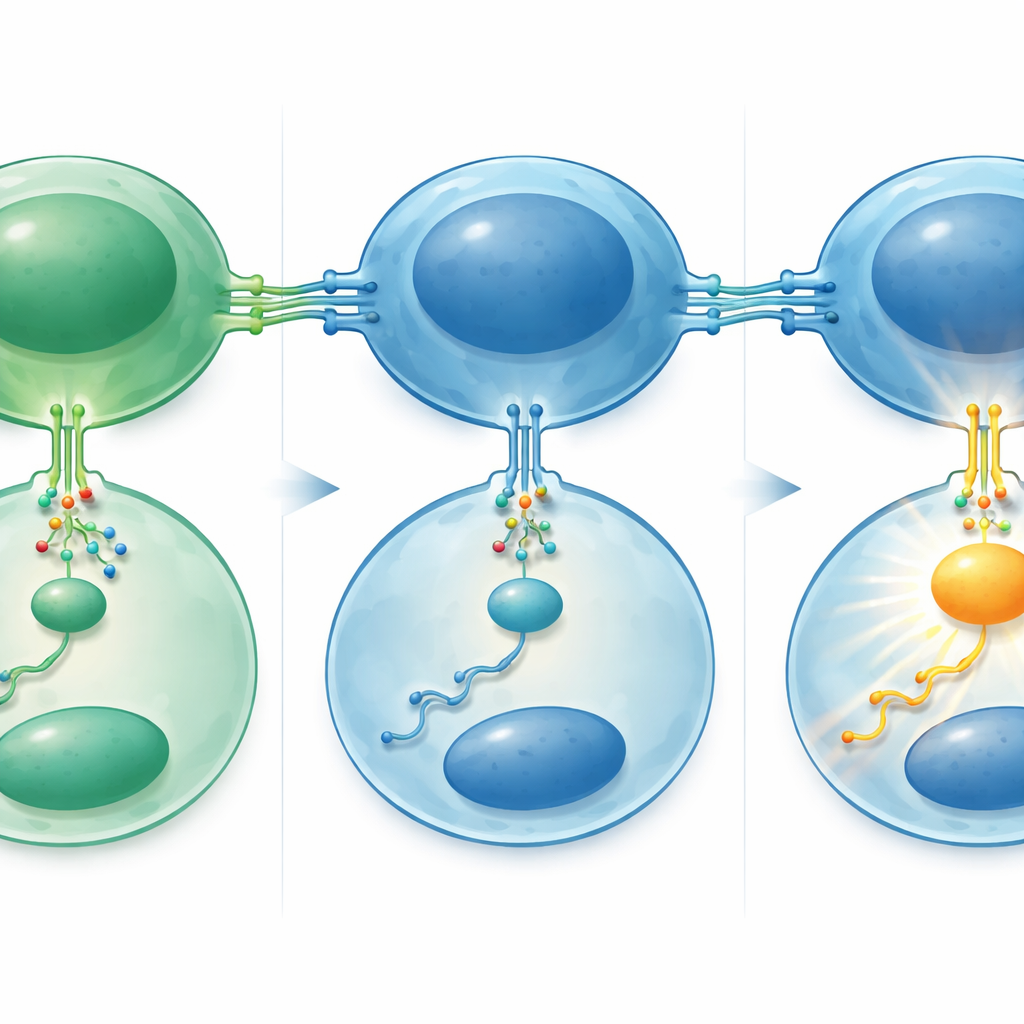
Como um circuito em três etapas amplifica o crescimento
Os autores então montaram o circuito molecular por trás dessa sensibilidade aumentada. Experimentos de laboratório mostraram que o miR-29 normalmente mantém em cheque os níveis de uma proteína chamada TRAF4 dentro das células B; TRAF4 é um adaptador interno que ajuda a transmitir o sinal do CD40 para o interior da célula. Quando os níveis de miR-29 foram aumentados experimentalmente em linhagens de linfoma, os níveis de TRAF4 caíram e as células responderam menos à estimulação por CD40, com ativação mais fraca da sinalização downstream e proliferação mais lenta. Nas amostras de pacientes, apareceu o padrão oposto: tumores transformados e linfomas foliculares de grau mais elevado tinham mais TRAF4 e taxas de divisão celular mais altas. Outro ator importante, a conhecida proteína promotora de câncer MYC, situou-se a montante. Os níveis e a atividade de MYC aumentaram durante a transformação, e demonstrou-se que MYC se liga diretamente às regiões de DNA que controlam o miR-29, atuando como um interruptor que reduz essa família de microRNAs.
O que isso significa para os pacientes
Juntando essas peças, o estudo delineia uma cadeia de três etapas: a ativação de MYC suprime o miR-29, a perda de miR-29 libera o freio sobre o TRAF4, e o excesso de TRAF4 torna as células do linfoma hiper-responsivas aos sinais CD40 das poucas células T auxiliares remanescentes. Essa “ajuda” amplificada impulsiona maior crescimento e sobrevivência, contribuindo para a transformação. Clinicamente, pacientes cujos tumores apresentavam níveis mais baixos de miR-29 — especialmente o membro miR-29c — tendiam a ter sobrevida mais curta e recidivas mais rápidas, achados confirmados em um ensaio de tratamento independente. Como o miR-29 pode ser medido de forma confiável mesmo em amostras de biópsia antigas e preservadas, e como drogas que mimetizam o miR-29 ou bloqueiam a sinalização CD40 já estão sendo exploradas, este trabalho aponta para novas formas de identificar pacientes com linfoma folicular de alto risco e de conceber tratamentos que cortem a conversa perigosa entre células tumorais e seus vizinhos imunes.
Citação: Filip, D., Litzmanova, K., Michaelou, A. et al. Repression of miR-29 via MYC leads to increased CD40 signaling in transformed follicular lymphoma. Leukemia 40, 759–772 (2026). https://doi.org/10.1038/s41375-026-02868-8
Palavras-chave: linfoma folicular, microRNA, sinalização CD40, MYC, microambiente tumoral