Clear Sky Science · pt
A perda de CHEK2 confere resistência à quimioterapia às células-tronco hematopoéticas
Por que algumas células sanguíneas resistem à quimioterapia
À medida que os tratamentos contra o câncer melhoram e mais pessoas sobrevivem à quimioterapia e à radiação, os médicos vêm descobrindo um efeito colateral inesperado: anos depois, muitos sobreviventes carregam bolsões de células sanguíneas geneticamente alteradas que dominaram partes da medula óssea durante a terapia. Este artigo investiga uma pergunta direta por trás desse mistério: por que certas células-tronco sanguíneas mutantes resistem melhor a medicamentos oncológicos agressivos do que células normais, e o que isso significa para o risco futuro de leucemia e para as escolhas de tratamento?
A evolução oculta dentro da nossa medula óssea
Nosso sistema sanguíneo é constantemente renovado por um pequeno reservatório de células-tronco na medula óssea. Ao longo da vida, essas células acumulam gradualmente alterações aleatórias no DNA. Quando uma célula-tronco com uma alteração vantajosa ganha uma vantagem de sobrevivência, ela pode gerar um grande “clone” de células descendentes, um processo chamado hematopoese clonal. Isso é surpreendentemente comum em adultos mais velhos e tem sido associado não apenas a cânceres sanguíneos, mas também a doenças cardíacas e outras condições relacionadas à idade. As terapias contra o câncer adicionam um estresse intenso a esse sistema, matando muitas células e favorecendo involuntariamente aqueles raros mutantes que resistem melhor ao dano no DNA.
Um interruptor de segurança que vira problema durante o tratamento
O foco aqui é um gene chamado CHEK2, que atua como parte da circuitaria celular de detecção de danos. Em células saudáveis, o CHEK2 ajuda a detectar DNA quebrado, pausar a divisão celular e, se o dano for muito grande, acionar a autodestruição. Usando uma triagem em larga escala com nocaute de genes em células de leucemia, os pesquisadores desativaram sistematicamente milhares de genes para ver quais perdas ajudavam as células a sobreviver aos medicamentos quimioterápicos tradicionais que danificam o DNA. O CHEK2 destacou-se rapidamente: quando desativado, as células tinham muito mais probabilidade de sobreviver ao tratamento com drogas como cisplatina e melfalona. Sem esse interruptor de segurança, células danificadas continuavam a se dividir em vez de parar ou morrer.
Células-tronco mutantes que se recusam a desistir
Para ir além das linhagens celulares, a equipe engenheirou camundongos cujas células-tronco e progenitoras formadoras de sangue não possuíam Chek2. Em condições normais, esses camundongos produziam sangue de maneira perfeitamente ordinária, sugerindo que o gene não é essencial para a formação diária do sangue. Isso mudou quando os animais receberam doses repetidas de quimioterapia. Nesse contexto estressante, as células-tronco e progenitoras precoces deficientes em Chek2 foram muito menos depletadas que suas contrapartes normais e gradualmente passaram a dominar grande parte do sistema sanguíneo. Essas células sobreviventes carregavam mais marcas de lesão no DNA do que as células normais, ainda assim persistiram e reconstituíram a medula óssea, ilustrando uma troca preocupante: resistência ao tratamento ao custo de portar cicatrizes genéticas extras.
Quando os medicamentos contra leucemia alimentam clones resistentes
O estudo também investigou se medicamentos mais recentes e “mais suaves” usados para distúrbios da medula óssea, conhecidos como agentes hipometilantes, criam pressões semelhantes. Esses fármacos, incluindo azacitidina e decitabina, são geralmente vistos como medicamentos epigenéticos que afrouxam marcas químicas no DNA. Os autores descobriram que, na verdade, eles também causam uma forma distinta de dano ao DNA ao aprisionar uma enzima chamada DNMT1 diretamente no DNA. Em culturas mistas de células normais e deficientes em CHEK2, e em células-tronco de camundongo cultivadas fora do corpo, esse dano novamente favoreceu os mutantes, que escaparam da parada do ciclo celular e da morte. Quando um composto separado que bloqueia DNMT1, mas não danifica o DNA, foi adicionado, a vantagem dos mutantes CHEK2 desapareceu em grande parte, ressaltando que é a lesão no DNA — e não a desmetilação em si — que seleciona esses clones resistentes.
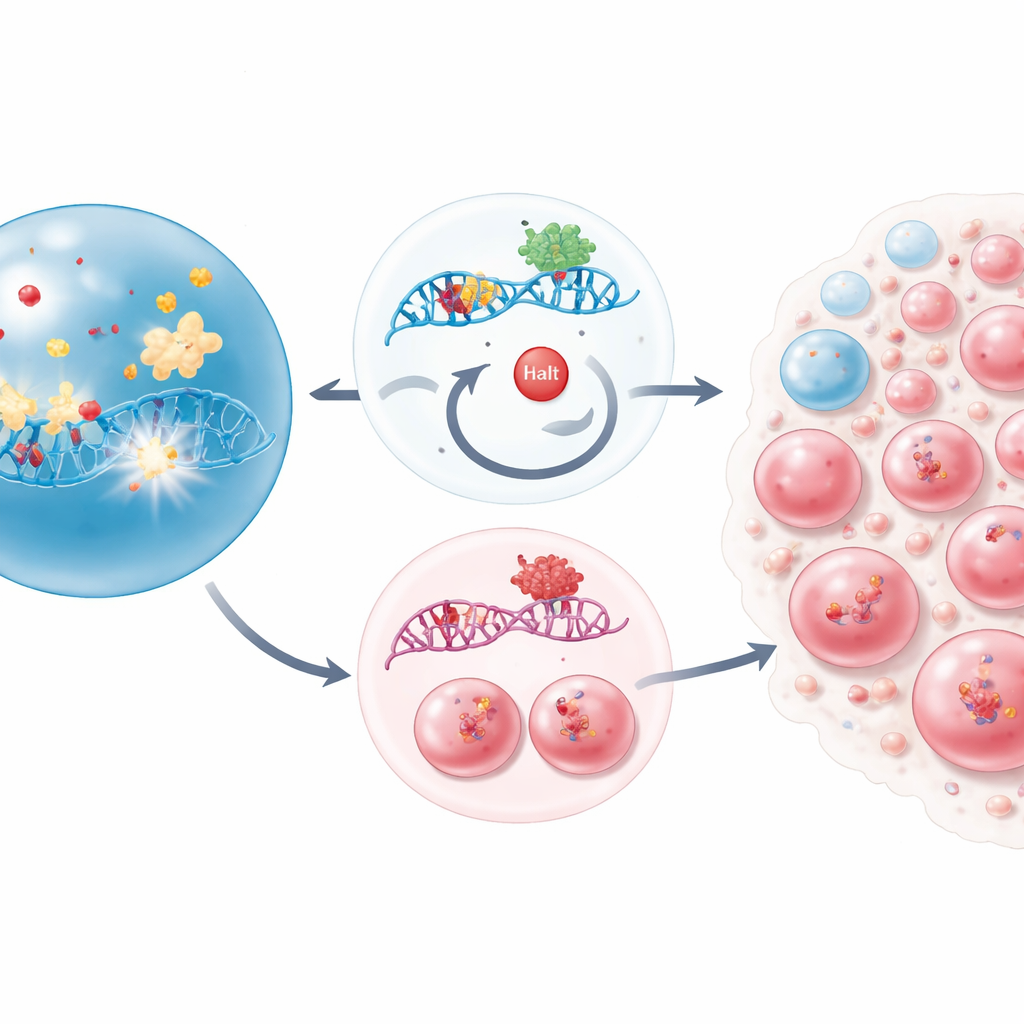
O que isso significa para pacientes e cuidados futuros
Em conjunto, o trabalho pinta um quadro vívido de como um único interruptor de segurança danificado em células-tronco sanguíneas pode remodelar silenciosamente o sistema sanguíneo após a terapia contra o câncer. A perda de CHEK2 permite que as células-tronco resistam tanto a quimioterapias clássicas quanto a medicamentos amplamente usados para a medula óssea, sobrevivam com dano persistente no DNA e se expandam em clones dominantes. Para os pacientes, isso ajuda a explicar por que certas mutações em genes de reparo do DNA são frequentemente encontradas no sangue anos após o tratamento e podem prenunciar leucemias relacionadas à terapia. Compreender que medicamentos específicos podem, involuntariamente, favorecer essas células mutantes sugere que planos de tratamento futuros, e talvez novas terapias direcionadas, precisarão levar em conta o “ecossistema” genético da medula óssea de um paciente, e não apenas o câncer em tratamento.
Citação: Zhou, J., Hu, T., Li, D. et al. CHEK2 loss endows chemotherapy resistance to hematopoietic stem cells. Leukemia 40, 511–521 (2026). https://doi.org/10.1038/s41375-025-02850-w
Palavras-chave: hematopoese clonal, CHEK2, resistência à quimioterapia, resposta ao dano no DNA, células-tronco hematopoéticas